Alosetron (Lotronex) foi aprovado para comercialização pela FDA em fevereiro de 2000, mas foi retirado do mercado em novembro de 2000, devido a sérios efeitos colaterais gastrointestinais com risco de vida. Em junho de 2002, foi aprovado novamente pela FDA para comercialização, mas de forma restrita como parte de um programa patrocinado por uma empresa farmacêutica para gerenciar os riscos associados ao tratamento. O uso de alosetrom é permitido apenas entre mulheres com síndrome do intestino irritável (SII) grave, com predominância de diarreia, que não responderam ao tratamento convencional para a síndrome do intestino irritável.
A declaração oficial original da FDA emitida quando o alosetron foi originalmente retirado está abaixo.
-- Editor médico, MedicineNet.com
28 de novembro de 2000--GLAXO WELLCOME DECIDE RETIRAR LOTRONEX DO MERCADOTGlaxo Wellcome, de Research Triangle Park, Carolina do Norte, informou à FDA que retirará voluntariamente os comprimidos de Lotronex (cloridrato de alosetron) do mercado. Lotronex é um medicamento de prescrição aprovado para tratar a síndrome do intestino irritável (SII) em mulheres. A FDA está aconselhando os pacientes que tomam Lotronex a entrar em contato com seus profissionais de saúde para discutir alternativas de tratamento.
A ação da empresa segue uma reunião realizada hoje cedo com a Food and Drug Administration (FDA), onde a agência discutiu com a Glaxo Wellcome opções de gerenciamento de risco que incluíam restringir a distribuição do medicamento ou retirada de marketing.
A ação de hoje segue as análises da FDA dos relatórios pós-comercialização de eventos adversos graves, que incluíram 5 notificações de morte em pacientes tomando Lotronex.
Especificamente, a FDA tem se preocupado com casos relatados de danos intestinais resultantes da redução do fluxo sanguíneo para o intestino (colite isquêmica) e intestinos severamente obstruídos ou rompidos (complicações de constipação grave).
Em 10 de novembro de 2000, a FDA recebeu e revisou um total de 70 casos de eventos adversos pós-comercialização graves, incluindo 49 casos de colite isquêmica e 21 casos de constipação grave. Dos 70 casos, 34 resultaram em internação sem cirurgia, 10 resultaram em procedimentos cirúrgicos e três resultaram em óbito. A FDA recebeu dois relatórios adicionais de morte que a agência não classificou como casos de colite isquêmica ou complicações graves de constipação.
A FDA tem monitorado de perto a droga desde a aprovação em 9 de fevereiro de 2000. Antes da aprovação, quatro casos de colite isquêmica foram observados em estudos clínicos e foram discutidos em novembro de 1999 em uma reunião do Comitê Consultivo de Medicamentos Gastrointestinais da FDA. Esses casos foram transitórios, de natureza leve a moderada e reversíveis com a descontinuação do medicamento.
Entre a aprovação e 1º de junho de 2000, a FDA recebeu sete notificações pós-comercialização de complicações graves da constipação. Isso resultou na hospitalização de seis pacientes, três dos quais necessitaram de cirurgia. Durante o mesmo período, a FDA recebeu oito notificações pós-comercialização de colite isquêmica. Isso resultou em quatro internações, quatro procedimentos endoscópicos e nenhuma cirurgia.
Em 27 de junho de 2000, a FDA convocou uma reunião do comitê consultivo público onde foram discutidas as opções de gerenciamento de risco em resposta aos relatos de eventos adversos graves. Nenhuma morte foi relatada até essa data. O consenso dos membros do comitê consultivo foi que médicos e pacientes devem ser informados sobre os eventos adversos potencialmente graves associados ao Lotronex.
Após a reunião, a FDA atualizou a rotulagem do profissional de saúde para o Lotronex e exigiu que o patrocinador do medicamento, Glaxo Wellcome, distribuísse um Guia de Medicação que alertava diretamente os pacientes sobre os riscos associados ao medicamento. Além disso, a pedido da FDA, a Glaxo Wellcome emitiu cartas "Dear Healthcare Professional" e "Dear Pharmacist" para aconselhar esses grupos sobre as novas informações importantes.
A FDA continuou a receber relatórios de eventos adversos graves de colite isquêmica e complicações de constipação associadas ao Lotronex. Além disso, a FDA recebeu relatos de morte e complicações mais graves de colite isquêmica que exigiram transfusão de sangue ou cirurgia.
Ao concluir suas análises recentes dos 70 casos, a visão da FDA sobre as opções incluía a retirada do mercado ou um programa restrito de distribuição de medicamentos. O programa restrito de distribuição de medicamentos forneceria:(1) uso seguro de Lotronex em pacientes devidamente informados, (2) acesso contínuo a Lotronex por pacientes gravemente debilitados com SII sob condições monitoradas de perto e (3) pesquisa clínica contínua sobre os benefícios, riscos, e uso seguro e adequado de Lotronex. A FDA reconheceu que os outros tratamentos disponíveis para IBS podem oferecer alívio inadequado de uma condição que pode ser severamente incapacitante para alguns pacientes.
Ao final da reunião de hoje, a Glaxo Wellcome informou à FDA que retirará voluntariamente o Lotronex do mercado.
Para obter mais informações sobre este assunto, visite a página da Internet Lotronex Information criada pelo Centro de Avaliação e Pesquisa de Medicamentos da FDA. A URL é www.fda.gov/cder/drug/infopage/lotronex/lotronex.htm.
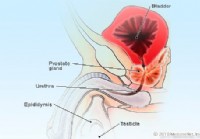 Prostatite vs. HBP (aumento da próstata):qual é a diferença?
Prostatite vs. HBP (aumento da próstata):qual é a diferença?
 O que o Dr. Tom O'Bryan me ensinou sobre distúrbios relacionados ao glúten
O que o Dr. Tom O'Bryan me ensinou sobre distúrbios relacionados ao glúten
 O microbioma humano corta os glicanos da mucosa,
O microbioma humano corta os glicanos da mucosa,
 Distúrbios digestivos:o que o tipo e a cor do seu cocô significam
Distúrbios digestivos:o que o tipo e a cor do seu cocô significam
 A superbactéria E. coli se espalhando por falta de higiene do banheiro,
A superbactéria E. coli se espalhando por falta de higiene do banheiro,
 Diário de cura da dieta SCD de Steve:Semana 25 – Refeições legais de SCD rápidas e fáceis
Diário de cura da dieta SCD de Steve:Semana 25 – Refeições legais de SCD rápidas e fáceis
 O que fazer durante um surto de IBS
6 estratégias para gerenciar um surto de IBS Se você está vivendo com a Síndrome do Intestino Irritável (SII), é provável que você tenha experimentado um “surto” – onde seus sintomas pioram significa
O que fazer durante um surto de IBS
6 estratégias para gerenciar um surto de IBS Se você está vivendo com a Síndrome do Intestino Irritável (SII), é provável que você tenha experimentado um “surto” – onde seus sintomas pioram significa
 O que causa o vômito? 7 razões e como facilitar isso
Quais são as sete causas mais comuns de vômito? Enjoo matinal na gravidez é uma causa comum de vômito. O vômito é um reflexo dirigido pelo cérebro em direção aos intestinos para reverter seus movi
O que causa o vômito? 7 razões e como facilitar isso
Quais são as sete causas mais comuns de vômito? Enjoo matinal na gravidez é uma causa comum de vômito. O vômito é um reflexo dirigido pelo cérebro em direção aos intestinos para reverter seus movi
 Agricultor vs. Peixe selvagem:qual é melhor para um intestino saudável?
Quando você pensa em uma refeição “saudável”, o que vem à mente? Quando penso em comida saudável, sempre imagino um filé de salmão rosa brilhante. Algo que se parece com isso: Mas o peixe é semp
Agricultor vs. Peixe selvagem:qual é melhor para um intestino saudável?
Quando você pensa em uma refeição “saudável”, o que vem à mente? Quando penso em comida saudável, sempre imagino um filé de salmão rosa brilhante. Algo que se parece com isso: Mas o peixe é semp