Approvazione FDA di Bosulif di Pfizer per il trattamento della leucemia mieloide cronica (LMC)
Di Daniel J. DeNoon
WebMD Health News
Recensione di Louise Chang, MD
7 settembre 2012 -- La FDA ha approvato Bosulif di Pfizer per il trattamento della leucemia mieloide cronica (LMC) per le persone che non rispondono o che non possono tollerare altri trattamenti.
La LMC è una malattia relativamente rara. Colpisce circa 5.400 persone all'anno. La maggior parte delle persone ha una mutazione rara, soprannominata la mutazione Philadelphia, che fa sì che il midollo osseo produca troppo enzima tirosin-chinasi. Bosulif inibisce questo enzima.
Altri farmaci approvati per la LMC - Gleevec e Tasigna di Novartis e Sprycel di Bristol-Myers Squibb - inibiscono la tirosina chinasi in altri modi.
"Con l'approvazione degli inibitori della tirosin-chinasi, stiamo assistendo a miglioramenti nel trattamento della LMC sulla base di una migliore comprensione delle basi molecolari della malattia", ha affermato Richard Pazdur, MD, direttore dell'ufficio dei prodotti ematologici e oncologici della FDA. in un comunicato stampa.
Negli studi clinici, il 55% dei pazienti con LMC precedentemente trattati con Gleevec o altri farmaci ha riportato un normale emocromo senza segni di leucemia entro le prime 48 settimane di trattamento con Bosulif.
Gli effetti collaterali più comuni di Bosulif sono diarrea, nausea, bassi livelli di piastrine nel sangue, vomito, dolore addominale, eruzioni cutanee, anemia, febbre e affaticamento.
 La scienza del sidro di fuoco e degli Oxymels per il miglioramento della salute
La scienza del sidro di fuoco e degli Oxymels per il miglioramento della salute
 L'ipotiroidismo ti sta causando una bassa energia?
L'ipotiroidismo ti sta causando una bassa energia?
 Lezioni importanti da un giorno nella vita di Steve:il buono, il cattivo e il brutto
Lezioni importanti da un giorno nella vita di Steve:il buono, il cattivo e il brutto
 Trattamento del reflusso acido nei neonati e nei bambini
Trattamento del reflusso acido nei neonati e nei bambini
 La medicina sta cambiando... Questo è il futuro della salute
La medicina sta cambiando... Questo è il futuro della salute
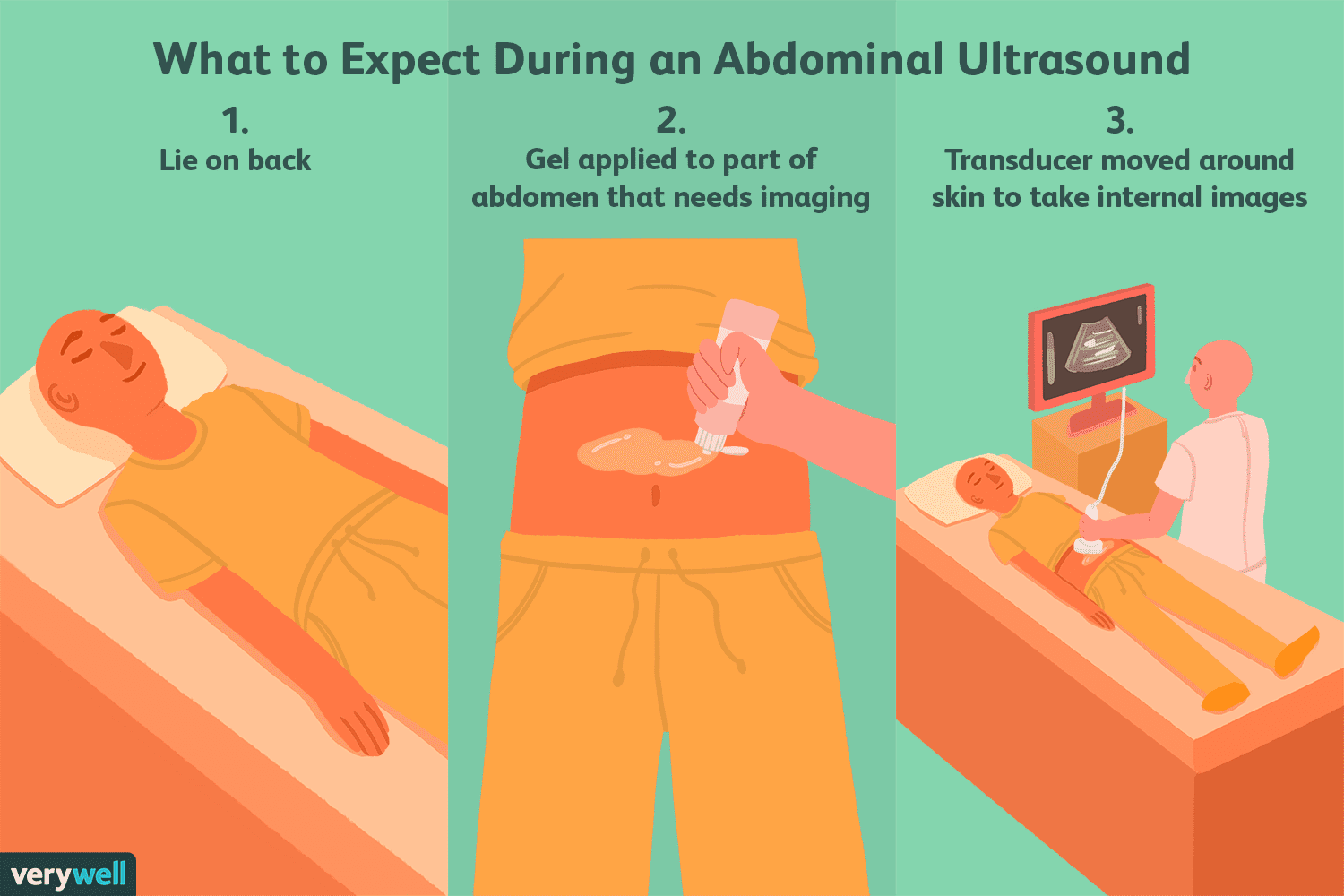 Che cos'è un ultrasuono addominale?
Che cos'è un ultrasuono addominale?
 I batteri intestinali possono predire il rischio di ipertensione polmonare
Un team di ricercatori ha scoperto che la microflora dei batteri nellintestino degli esseri umani potrebbe contribuire allo sviluppo dellipertensione arteriosa polmonare (PAH). Lo studio intitolato, P
I batteri intestinali possono predire il rischio di ipertensione polmonare
Un team di ricercatori ha scoperto che la microflora dei batteri nellintestino degli esseri umani potrebbe contribuire allo sviluppo dellipertensione arteriosa polmonare (PAH). Lo studio intitolato, P
 Che cos'è l'oncogenesi?
Loncogenesi è il complesso processo in più fasi mediante il quale le cellule normali si trasformano in cellule cancerose, portando alla crescita del cancro nel corpo. Implica cambiamenti genetici in u
Che cos'è l'oncogenesi?
Loncogenesi è il complesso processo in più fasi mediante il quale le cellule normali si trasformano in cellule cancerose, portando alla crescita del cancro nel corpo. Implica cambiamenti genetici in u
 GI Doctor Near Me – Trova un gastroenterologo locale
Trova il migliore Medico GI vicino a me Se hai cercato medico GI vicino a me di quanto sei arrivato nel posto giusto per le risposte a tutte le tue domande. Cercare i servizi di trattamento di un med
GI Doctor Near Me – Trova un gastroenterologo locale
Trova il migliore Medico GI vicino a me Se hai cercato medico GI vicino a me di quanto sei arrivato nel posto giusto per le risposte a tutte le tue domande. Cercare i servizi di trattamento di un med