FDA-godkendelse af Pfizer's Bosulif til behandling af kronisk myelogen leukæmi (CML)
Af Daniel J. DeNoon
WebMD Health News
Anmeldt af Louise Chang, MD
7. september 2012 -- FDA har godkendt Pfizer's Bosulif til behandling af kronisk myelogen leukæmi (CML) for mennesker, der ikke reagerer på eller ikke kan tolerere andre behandlinger.
CML er en relativt sjælden sygdom. Det rammer omkring 5.400 mennesker om året. De fleste mennesker har en sjælden mutation, kaldet Philadelphia-mutationen, som får knoglemarven til at lave for meget tyrosinkinase-enzym. Bosulif hæmmer dette enzym.
Andre lægemidler godkendt til CML -- Gleevec og Tasigna fra Novartis og Sprycel fra Bristol-Myers Squibb -- hæmmer tyrosinkinase på andre måder.
"Med godkendelsen af tyrosinkinasehæmmere ser vi forbedringer i behandlingen af CML baseret på en bedre forståelse af det molekylære grundlag for sygdommen," sagde Richard Pazdur, MD, direktør for FDA's kontor for hæmatologi og onkologiprodukter. i en pressemeddelelse.
I kliniske forsøg vendte 55 % af CML-patienter, der tidligere var behandlet med Gleevec eller andre lægemidler, tilbage til normale blodtal uden tegn på leukæmi inden for de første 48 ugers behandling med Bosulif.
De mest almindelige bivirkninger ved Bosulif er diarré, kvalme, lave blodpladeniveauer, opkastning, mavesmerter, udslæt, anæmi, feber og træthed.
 rektal blødning og inflammatorisk tarmsygdom
Et af de mange symptomer på inflammatorisk tarmsygdom (IBD) er blødning. Der kan forekomme blod i eller på afføringen, eller nogle mennesker kan til tider slet ikke tage afføring og blot sende blod.
rektal blødning og inflammatorisk tarmsygdom
Et af de mange symptomer på inflammatorisk tarmsygdom (IBD) er blødning. Der kan forekomme blod i eller på afføringen, eller nogle mennesker kan til tider slet ikke tage afføring og blot sende blod.
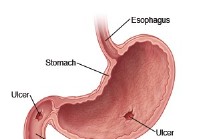 Mavesår
Dette udtryk refererer til både mave- og duodenalsårsygdom. Mavesår sygdom (PUD) er karakteriseret ved en defekt i mave- eller duodenalslimhinden, der strækker sig gennem muscularis slimhinden ind i d
Mavesår
Dette udtryk refererer til både mave- og duodenalsårsygdom. Mavesår sygdom (PUD) er karakteriseret ved en defekt i mave- eller duodenalslimhinden, der strækker sig gennem muscularis slimhinden ind i d
 Oprettelse af fællesskab i 2015
Mit hjerte hamrede... jeg var så spændt. Og så med ét blik på skærmen, var det hele væk. Jeg var sur. Der er ikke noget mere frustrerende end at møde op til en klasse og indse, at du allerede vidste
Oprettelse af fællesskab i 2015
Mit hjerte hamrede... jeg var så spændt. Og så med ét blik på skærmen, var det hele væk. Jeg var sur. Der er ikke noget mere frustrerende end at møde op til en klasse og indse, at du allerede vidste