Door Salynn Boyles
WebMD Health News
Beoordeeld door Louise Chang, MD
19 september 2012 -- Een experimentele pil is veelbelovend voor de behandeling van multiple sclerose.
In twee late-fase studies die verschijnen in The New England Journal of Medicine , het medicijn BG-12 (dimethylfumaraat) verminderde terugvallen met ongeveer de helft bij patiënten met de meest voorkomende vorm van MS.
Indien goedgekeurd door de FDA, zal BG-12, dat wordt ontwikkeld door medicijnmaker Biogen Idec, het derde orale medicijn worden voor mensen met multiple sclerose.
De tweede -- Sanofi Aventis' pil Aubagio -- kreeg vorige week goedkeuring van de FDA.
"Dit is een opwindende tijd in de ontwikkeling van nieuwe medicijnen voor MS, vooral gezien het feit dat we een paar decennia geleden nog geen effectieve behandelingen hadden", zegt Timothy Coetzee, PhD, Chief Research Officer van de National MS Society.
Multiple sclerose is een chronische ziekte waarbij het immuunsysteem de isolatie aanvalt die de zenuwvezels van de hersenen en het ruggenmerg omhult en beschermt.
Bij het meest voorkomende type ervaren mensen sporadische aanvallen of opflakkeringen van symptomen die vervolgens worden gevolgd door perioden van remissie. Symptomen zijn onder meer gevoelloosheid, vermoeidheid, problemen met het gezichtsvermogen, spasmen en problemen met blaas- en darmcontrole.
Mensen met deze "relapsing-remitting" vorm van MS waren de doelgroep voor het nieuwe orale medicijn.
De twee nieuw gepubliceerde onderzoeken werden gefinancierd door de fabrikant van het medicijn.
Bij één patiënt met relapsing-remitting disease die tweemaal daags BG-12 gebruikten, was het aantal recidieven gedurende twee jaar behandeling met 44% verminderd. In de tweede studie was de terugvalvermindering in dezelfde periode 53%.
De meest voorkomende bijwerkingen van de behandeling waren blozen en maagproblemen zoals diarree en buikpijn. Maar de meeste patiënten ondervonden minder van deze voorvallen na de eerste maand van de behandeling.
Tweemaal daagse behandeling was ook gekoppeld aan een vermindering van 71% van nieuwe hersenlaesies geassocieerd met MS in een van de onderzoeken, geleid door neuroloog Robert J. Fox, MD, die het Cleveland Clinic Mellen Center for Multiple Sclerosis leidt.
Fox heeft gediend als een betaalde Biogen Idec-consultant voor projecten die geen verband houden met de BG-12-studie.
"Naar mijn mening biedt BG-12 een zeer sterke combinatie van (effectiviteit), veiligheid en verdraagbaarheid", zegt hij.
Coetzee zegt dat het nog maar de vraag is of de nieuwe orale medicijnen de standaard eerstelijns injecteerbare behandelingen zullen vervangen.
"Mijn gok is dat de injectables een belangrijke behandelingsoptie zullen blijven", zegt hij. "Hoe meer opties we hebben, hoe beter."
Dat komt omdat sommige mensen niet reageren op bepaalde behandelingen of ze niet kunnen verdragen.
Eerder dit jaar diende Biogen een verzoek in bij de FDA om BG-12 in de VS op de markt te brengen. Een woordvoerster van het bedrijf zegt dat het bureau tegen het einde van het jaar uitspraak kan doen over het verzoek.
 Oude microbiomen van primaten kunnen meer informatie opleveren over menselijke ontwikkeling
Oude microbiomen van primaten kunnen meer informatie opleveren over menselijke ontwikkeling
 Hoe u uw diarree zo snel mogelijk kunt stoppen
Hoe u uw diarree zo snel mogelijk kunt stoppen
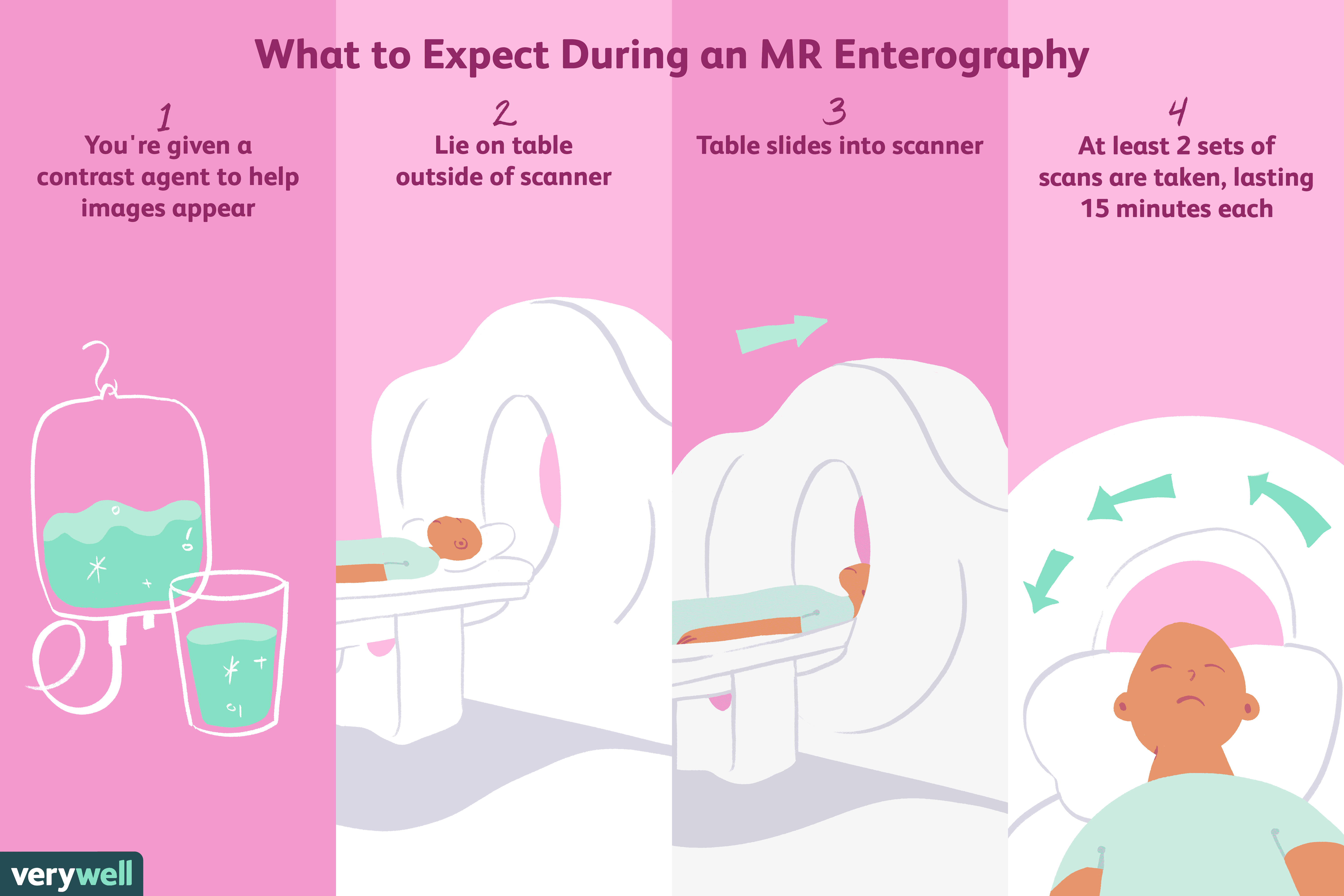 Wat is magnetische resonantie-enterografie?
Wat is magnetische resonantie-enterografie?
 Wat betekent groene ontlasting? Kleurenkaart ontlasting
Wat betekent groene ontlasting? Kleurenkaart ontlasting
 Nieuwe WGO-richtlijnen:hoe uw dieet u kan helpen om voor uw darmflora te zorgen
Nieuwe WGO-richtlijnen:hoe uw dieet u kan helpen om voor uw darmflora te zorgen
 Hepatitis C:laat je testen. Laat je behandelen.
Hepatitis C:laat je testen. Laat je behandelen.
 Wanneer moet u naar een zorgverlener voor buikpijn
Buikpijn is een relatief veel voorkomend symptoom dat vaak geen behandeling behoeft. Maar buikpijn kan een symptoom zijn van een ernstige aandoening waarvoor medische hulp en in sommige gevallen zelfs
Wanneer moet u naar een zorgverlener voor buikpijn
Buikpijn is een relatief veel voorkomend symptoom dat vaak geen behandeling behoeft. Maar buikpijn kan een symptoom zijn van een ernstige aandoening waarvoor medische hulp en in sommige gevallen zelfs
 Colitis ulcerosa:symptomen, dieet, behandeling, oorzaken
Wat is colitis ulcerosa? Colitis ulcerosa is een ziekte waarbij sprake is van chronische ontsteking van de binnenwand van de dikke darm. De ontsteking kan ervoor zorgen dat het slijmvliesweefsel af
Colitis ulcerosa:symptomen, dieet, behandeling, oorzaken
Wat is colitis ulcerosa? Colitis ulcerosa is een ziekte waarbij sprake is van chronische ontsteking van de binnenwand van de dikke darm. De ontsteking kan ervoor zorgen dat het slijmvliesweefsel af
 Lap-Band Surgery:Overzicht
Lapband-chirurgie, of maagbanding, is een soort bariatrische (gewichtsverlies) procedure. De operatie werkt door een strakke, verstelbare band rond het bovenste deel van de maag te plaatsen om het org
Lap-Band Surgery:Overzicht
Lapband-chirurgie, of maagbanding, is een soort bariatrische (gewichtsverlies) procedure. De operatie werkt door een strakke, verstelbare band rond het bovenste deel van de maag te plaatsen om het org