Par Salynn Boyles
Actualités WebMD sur la santé
Examiné par Louise Chang, MD
19 septembre 2012 -- Une pilule expérimentale semble prometteuse pour le traitement de la sclérose en plaques.
Dans deux études de phase tardive publiées dans The New England Journal of Medicine , le médicament BG-12 (fumarate de diméthyle) a réduit les rechutes de moitié environ chez les patients atteints de la forme la plus courante de SEP.
S'il est approuvé par la FDA, le BG-12, développé par le fabricant de médicaments Biogen Idec, deviendra le troisième médicament oral pour les personnes atteintes de sclérose en plaques.
La seconde, la pilule Aubagio de Sanofi Aventis, a obtenu l'approbation de la FDA la semaine dernière.
"C'est une période passionnante dans le développement de nouveaux médicaments pour la SEP, surtout si l'on considère le fait que nous n'avions aucun traitement efficace il y a quelques décennies à peine", déclare Timothy Coetzee, PhD, directeur de la recherche de la National MS Society.
La sclérose en plaques est une maladie chronique dans laquelle le système immunitaire attaque l'isolant qui recouvre et protège les fibres nerveuses du cerveau et de la moelle épinière.
Avec le type le plus courant, les gens subissent des attaques sporadiques ou des poussées de symptômes qui sont ensuite suivies de périodes de rémission. Les symptômes comprennent des engourdissements, de la fatigue, des problèmes de vision, des spasmes et des problèmes de contrôle de la vessie et des intestins.
Les personnes atteintes de cette forme de SEP "récurrente-rémittente" étaient le groupe cible du nouveau médicament oral.
Les deux essais récemment publiés ont été financés par le fabricant du médicament.
Dans l'un d'entre eux, les patients atteints d'une maladie récurrente-rémittente qui prenaient du BG-12 deux fois par jour présentaient une réduction de 44 % des rechutes sur deux ans de traitement. Dans la deuxième étude, la réduction des rechutes sur la même période était de 53 %.
Les effets secondaires les plus courants associés au traitement étaient les bouffées vasomotrices et les problèmes d'estomac tels que la diarrhée et les douleurs abdominales. Mais la plupart des patients ont connu moins de ces événements après le premier mois de traitement.
Un traitement biquotidien a également été associé à une réduction de 71 % des nouvelles lésions cérébrales associées à la SEP dans l'une des études, dirigée par le neurologue Robert J. Fox, MD, qui dirige le Cleveland Clinic Mellen Center for Multiple Sclerosis.
Fox a été consultant rémunéré de Biogen Idec pour des projets sans rapport avec l'étude BG-12.
"À mon avis, BG-12 offre une très bonne combinaison d'(efficacité), de sécurité et de tolérabilité", déclare-t-il.
Coetzee dit qu'il reste à voir si les nouveaux médicaments oraux remplaceront les traitements injectables standard de première ligne.
"Je suppose que les injectables resteront une option de traitement importante", dit-il. "Plus nous avons d'options, mieux c'est."
En effet, certaines personnes ne répondent pas à certains traitements ou ne les tolèrent pas.
Plus tôt cette année, Biogen a déposé une demande auprès de la FDA pour commercialiser le BG-12 aux États-Unis. Une porte-parole de la société a déclaré que l'agence pourrait statuer sur la demande d'ici la fin de l'année.
 Granola maison pour les tripes
Granola maison pour les tripes
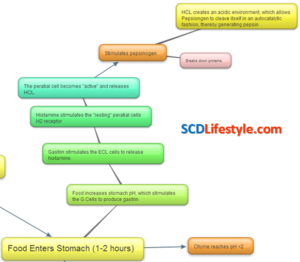 4 erreurs courantes de chlorhydrate de bétaïne
4 erreurs courantes de chlorhydrate de bétaïne
 L'ultime guide-cadeau pour des intestins sains
L'ultime guide-cadeau pour des intestins sains
 Désimpact numérique et comment c'est fait
Désimpact numérique et comment c'est fait
 Des scientifiques repèrent des gènes derrière la maladie de Crohn et la colite ulcéreuse
Des scientifiques repèrent des gènes derrière la maladie de Crohn et la colite ulcéreuse
 brochettes de poulet yakitori avec riz au chou-fleur arc-en-ciel
brochettes de poulet yakitori avec riz au chou-fleur arc-en-ciel
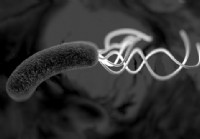 La controverse H. Pylori :provoque-t-elle vraiment des brûlures d'estomac, un reflux acide et un RGO ?
Cette petite bactérie… Il infecte plus de 50 % de la population mondiale. Lancez une pièce et cest la probabilité quelle vive dans votre tube digestif en ce moment. Mais est-ce que ça te fait mal ?
La controverse H. Pylori :provoque-t-elle vraiment des brûlures d'estomac, un reflux acide et un RGO ?
Cette petite bactérie… Il infecte plus de 50 % de la population mondiale. Lancez une pièce et cest la probabilité quelle vive dans votre tube digestif en ce moment. Mais est-ce que ça te fait mal ?
 Les critères de Rome pour le syndrome du côlon irritable (IBS)
Le syndrome du côlon irritable (IBS) est largement classé comme une condition dexclusion. En dautres termes, le SII est généralement diagnostiqué après que toutes les autres causes de symptômes, telle
Les critères de Rome pour le syndrome du côlon irritable (IBS)
Le syndrome du côlon irritable (IBS) est largement classé comme une condition dexclusion. En dautres termes, le SII est généralement diagnostiqué après que toutes les autres causes de symptômes, telle
 Troubles digestifs :23 mythes et faits sur la constipation
Les selles quotidiennes sont-elles normales ? Cest un mythe que tout le monde devrait avoir une selle quotidienne. Les résultats détudes montrent que certaines personnes bougent jusquà 3 fois par jo
Troubles digestifs :23 mythes et faits sur la constipation
Les selles quotidiennes sont-elles normales ? Cest un mythe que tout le monde devrait avoir une selle quotidienne. Les résultats détudes montrent que certaines personnes bougent jusquà 3 fois par jo