 Bild på en man med bukspottkörtelcancer av iStock
Bild på en man med bukspottkörtelcancer av iStock Bukspottkörtelcancer orsakar vanligtvis inte symtom förrän den har vuxit, så den diagnostiseras oftast i avancerade stadier snarare än tidigt i sjukdomsförloppet. I vissa fall kan gulsot (en gulaktig missfärgning av huden och ögonvitorna) utan smärta vara ett tidigt tecken på cancer i bukspottkörteln. Andra symtom som kan uppstå vid mer avancerad sjukdom är:
Blek avföring, ryggsmärtor, buksmärtor, mörk urin, bukuppblåsthet, diarré och förstorade lymfkörtlar i nacken kan också förekomma.
Läs mer om symtom på pankreascancer »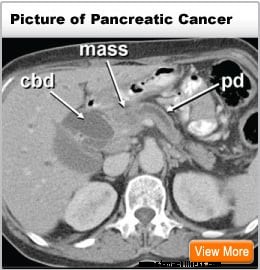
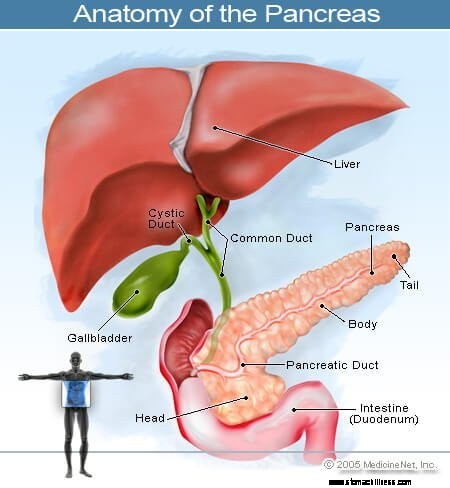 Cancer som börjar i bukspottkörteln kallas pankreascancer. Denna bild av bukspottkörteln visar dess placering på baksidan av buken, bakom magen.
Cancer som börjar i bukspottkörteln kallas pankreascancer. Denna bild av bukspottkörteln visar dess placering på baksidan av buken, bakom magen. Bukspottkörteln är ett hormonproducerande organ i buken som sitter framför ryggraden ovanför naveln. Den utför två huvudfunktioner:
Enzymerna hjälper matsmältningen genom att hacka proteiner, fetter och kolhydrater i mindre delar så att de lättare kan tas upp av kroppen och användas som byggstenar för vävnader och för energi. Enzymer lämnar bukspottkörteln via ett system av rör som kallas "kanaler" som förbinder bukspottkörteln med tarmarna där enzymerna blandas med intagen mat.
Bukspottkörteln sitter djupt i buken och är i nära anslutning till många viktiga strukturer som tunntarmen (tolvfingertarmen) och gallgångarna, samt viktiga blodkärl och nerver.
Varje sekund av varje dag i vår kropp sker en massiv process av förstörelse och reparation. Människokroppen består av biljoner celler och varje dag slits miljarder celler ut eller förstörs. Varje gång kroppen tillverkar en ny cell för att ersätta en som håller på att slitas ut, försöker kroppen göra en perfekt kopia av cellen som dör, vanligtvis genom att låta liknande friska celler dela sig i två celler eftersom den döende cellen hade ett jobb att göra , och den nytillverkade cellen måste kunna utföra samma funktion. Trots anmärkningsvärt eleganta system på plats för att redigera bort fel i denna process, gör kroppen tiotusentals misstag dagligen vid normal celldelning, antingen på grund av slumpmässiga fel eller från miljöpåverkan i kroppen. De flesta av dessa misstag korrigeras, eller så leder misstaget till att den nytillverkade cellen dör, och ytterligare en ny cell görs då. Ibland görs ett misstag som, snarare än att hämma cellens förmåga att växa och överleva, tillåter den nytillverkade cellen att växa på ett oreglerat sätt. När detta inträffar blir den cellen en cancercell som kan dela sig oberoende av de kontroller och balanser som styr normal celldelning. Cancercellen förökar sig och en cancerös eller malign tumör utvecklas.
Tumörer delas in i två kategorier:"godartade" tumörer och "maligna" eller cancerösa tumörer. Vad är skillnaden? Svaret är att en godartad tumör växer endast i den vävnad som den uppstår från. Godartade tumörer kan ibland växa sig ganska stora eller växa snabbt och orsaka allvarliga symtom. Till exempel kan ett myom i en kvinnas livmoder orsaka blödning eller smärta, men det kommer aldrig att resa utanför livmodern, invadera omgivande vävnader eller växa som en ny tumör någon annanstans i kroppen (metastaserad). Fibroider, som alla godartade tumörer, saknar kapacitet att sprida celler i blodet och lymfsystemet och kan inte resa till andra platser i kroppen och växa. En cancer kan å andra sidan tappa celler från den ursprungliga tumören som kan sväva som maskrosfrön i vinden genom blodomloppet eller lymfan, landa i vävnader på avstånd från tumören och utvecklas till nya tumörer i andra delar av kroppen. Denna process, som kallas metastas, är det avgörande kännetecknet för en cancertumör. Bukspottkörtelcancer är tyvärr en särskilt bra modell för denna process. Bukspottkörtelcancer kan metastasera tidigt till andra organ på detta sätt. De kan också växa och invadera intilliggande strukturer direkt, vilket ofta omöjliggör kirurgiskt avlägsnande av tumören.
Cancer är namngiven av de vävnader från vilka den primära tumören uppstår. Därför är en lungcancer som går till levern inte en "levercancer" utan beskrivs som metastaserad lungcancer och en patient med en bröstcancer som sprider sig till hjärnan beskrivs inte som att ha en "hjärntumör" utan snarare som att ha metastaserande bröstcancer.


Vad är Polycythemia Vera?
Läs mer om
En cancer som utvecklas i bukspottkörteln delas in i två huvudkategorier:(1) cancer i den endokrina bukspottkörteln (den del som gör insulin och andra hormoner) kallas "öcell" eller "pankreatiska neuroendokrina tumörer eller PNET" och (2) cancerformer av den exokrina bukspottkörteln (den del som gör enzymer). Öcellscancer är sällsynt och växer vanligtvis långsamt jämfört med exokrina pankreascancer. Öcellstumörer frisätter ofta hormoner i blodomloppet och kännetecknas ytterligare av de hormoner de producerar (insulin, glukagon, gastrin och andra hormoner). Cancer i den exokrina bukspottkörteln (exokrina cancerformer) utvecklas från cellerna som kantar systemet av kanaler som levererar enzymer till tunntarmen och kallas vanligtvis pankreasadenokarcinom. Skivepitelcancer i bukspottkörteln är sällsynt. Adenokarcinom i bukspottkörteln omfattar nästan alla bukspottkörtelcancer och är huvudämnet för denna översikt.
Celler som kantar kanalerna i den exokrina bukspottkörteln delar sig snabbare än vävnaderna som omger dem. Av skäl som vi inte förstår kan dessa celler göra ett misstag när de kopierar sitt DNA när de delar sig för att ersätta andra döende celler. På detta sätt kan en onormal cell göras. När en onormal duktalcell börjar dela sig på ett oreglerat sätt kan en tillväxt bildas som består av celler som ser onormalt ut och fungerar. De onormala förändringarna som kan kännas igen under mikroskopet kallas "dysplasi". Ofta kan dysplastiska celler genomgå ytterligare DNA-misstag med tiden och bli ännu mer onormala. När dessa dysplastiska celler invaderar genom väggarna i kanalen varifrån de kommer in i den omgivande vävnaden, har dysplasin blivit en cancer.
I en studie publicerad 2016 rapporterade forskare analys av generna i 456 pankreatiska duktala adenokarcinom. Efterföljande expressionsanalys av dessa adenokarcinom gjorde att de kunde definieras i fyra subtyper. Dessa undertyper har inte tidigare kunnat urskiljas. Undertyperna inkluderar:
Dessa nya fynd kan göra det möjligt för framtida cancerpatienter att behandlas mer specifikt beroende på deras undertyp och, förhoppningsvis, mer effektivt. Till exempel kan den immunogena subtypen möjligen svara på terapi där immunsystemet omkonstrueras för att attackera dessa typer av cancerceller.
Bukspottkörtelcancer ska inte förväxlas med termen pankreatit. Pankreatit definieras helt enkelt som inflammation i bukspottkörteln och orsakas huvudsakligen av alkoholmissbruk och/eller gallstensbildning (ca 80% till 90%). Ändå är kronisk pankreatit associerad med pankreascancer.
Omkring 53 670 fall av cancer i bukspottkörteln inträffar årligen i USA. De flesta som utvecklar bukspottkörtelcancer gör det utan några predisponerande riskfaktorer. Den kanske största riskfaktorn är dock stigande ålder; att vara över 60 år utsätter en individ för en större risk. Sällan kan det finnas familjära eller ärftliga genetiska syndrom som härrör från genetiska mutationer som går i familjer och sätter individer i högre risk, såsom BRCA-2 och, i mindre utsträckning, BRCA-1 genmutationer. Familjesyndrom är ovanligt, men det är viktigt att meddela en läkare om någon annan i familjen har fått diagnosen cancer, särskilt cancer i bukspottkörteln. Dessutom tros vissa beteenden eller tillstånd något öka en individs risk för att utveckla bukspottkörtelcancer. Till exempel kan afroamerikaner löpa större risk, liksom individer med nära familjemedlemmar som tidigare har diagnostiserats med cancer i bukspottkörteln. Andra beteenden eller tillstånd som kan utsätta människor för risk inkluderar tobaksanvändning, fetma, en stillasittande livsstil, en historia av diabetes, kronisk pankreasinflammation (pankreatit) och en fet (eller västerländsk) kost. Tidigare magoperationer kan öka risken måttligt, liksom vissa kroniska infektioner som hepatit B och H. pylori (en bakteriell infektion i magslemhinnan). Vissa läkemedel (sitagliptin [Januvia], exenatid [Byetta], liraglutid [Victoza] och metformin och sitagliptin [Janumet]) har kopplats till utvecklingen av cancer i bukspottkörteln. Vissa typer av cystor i bukspottkörteln kan sätta individer i riskzonen att utveckla bukspottkörtelcancer. Några forskare föreslår att dricka kaffe och läsk ökar risken för cancer i bukspottkörteln. När cancer i bukspottkörteln börjar, börjar den vanligtvis i cellerna som kantar bukspottkörtelns kanaler och kallas adenokarcinom i bukspottkörteln eller exokrin cancer i bukspottkörteln . Trots de associerade riskerna som nämns ovan, finns ingen identifierbar orsak hos de flesta människor som utvecklar cancer i bukspottkörteln.
Genom att klicka på "Skicka" godkänner jag MedicineNets villkor och sekretesspolicy. Jag samtycker också till att ta emot e-postmeddelanden från MedicineNet och jag förstår att jag kan välja bort MedicineNet-prenumerationer när som helst.
Eftersom bukspottkörteln ligger djupt i magen framför ryggraden, växer bukspottkörtelcancer ofta tyst i månader innan den upptäcks. Tidiga cancersymptom och/eller första tecken kan vara frånvarande eller ganska subtila. Lättare identifierbara symtom utvecklas när tumören växer sig stor nog att trycka på andra närliggande strukturer, såsom nerver (som orsakar generaliserad smärta och/eller ryggsmärta), tarmarna (vilket påverkar aptiten och orsakar illamående tillsammans med viktminskning), eller gallgångar (som orsakar gulsot eller gulfärgning av huden och kan orsaka aptitlöshet och klåda). Symtom hos kvinnor skiljer sig sällan från dem hos män. När tumören väl sprider cancerceller i blod- och lymfsystemet och metastaserar, uppstår vanligtvis ytterligare symtom, beroende på platsen för metastasen. Frekventa metastaser för cancer i bukspottkörteln inkluderar levern, lymfkörtlarna och bukslemhinnan (kallas bukhinnan; ascitesvätska kan ackumuleras vid metastaserad pankreascancer). Tyvärr hittas de flesta cancerformer i bukspottkörteln efter att cancern har vuxit eller utvecklats bortom bukspottkörteln eller har spridit sig till andra ställen.
I allmänhet kan tecknen och symtomen på pankreascancer produceras av exokrina eller endokrina cancerceller. Många av tecknen och symtomen på exokrin pankreascancer beror på blockering av kanalen som går genom bukspottkörteln från levern som transporterar galla till tarmen. Symtom på exokrin pankreascancer inkluderar
Tecken och symtom på endokrina pankreascancer är ofta relaterade till överskottet av hormoner som de producerar och följaktligen till en mängd olika symtom. Sådana symtom är relaterade till hormonerna och är följande:
Icke-fungerande neuroendokrina tumörer gör inte överskott av hormoner men kan växa sig stora och spridas ut ur bukspottkörteln. Symtomen kan då vara som vilken som helst av de endokrina pankreascancer som beskrivs ovan.
De flesta människor behöver inte screenas för cancer i bukspottkörteln, och de tester som finns tillgängliga för screening är ofta komplexa, riskfyllda, dyra eller okänsliga i cancerns tidiga faser. De som kan kvalificera sig har vanligtvis en uppsättning faktorer som ökar risken för bukspottkörtelcancer, såsom bukspottkörtelcystor, första gradens släktingar med bukspottkörtelcancer eller en historia av genetiska syndrom associerade med bukspottkörtelcancer. De flesta screeningtester består av datortomografi, ultraljud, magnetisk resonans kolangiopankreatografi (MRCP), endoskopisk retrograd kolangiopankreatografi (ERCP) eller endoskopisk ultraljud. Tyvärr är tidig upptäckt av cancer i bukspottkörteln svårt eftersom få eller inga symtom är närvarande.
De flesta personer med cancer i bukspottkörteln går först till sin primärvårdsläkare och klagar på ospecifika symtom (se avsnittet symtom ovan). Vissa varningstecken inkluderar smärta, gastrointestinala symtom, viktminskning, trötthet och ökad bukvätska. Dessa besvär utlöser en utvärdering som ofta inkluderar en fysisk undersökning (vanligtvis normal), blodprover, röntgenstrålar och ett ultraljud. Om bukspottkörtelcancer är närvarande är sannolikheten för att ett ultraljud avslöjar en abnormitet i bukspottkörteln cirka 75 %. Om ett problem identifieras eller misstänks, utförs ofta en datortomografi (CT) som nästa steg i utvärderingen; vissa läkare föredrar en MRT. Om en bukspottkörtelmassa ses väcker det misstanken om bukspottkörtelcancer och en läkare gör sedan en biopsi för att ge en diagnos.
Olika strategier kan användas för att utföra en biopsi av den misstänkta cancern. Ofta kommer en nålbiopsi av levern genom bukväggen (perkutan leverbiopsi) att användas om det visar sig att cancern har spridits till levern. Om tumören förblir lokaliserad till bukspottkörteln, utförs vanligen biopsi av bukspottkörteln direkt med hjälp av en CT. En direkt biopsi kan också göras via ett endoskop som sätts ner i halsen och in i tarmarna. En kamera på spetsen av endoskopet gör att endoskopisten kan föra fram endoskopet i tarmen. En ultraljudsapparat i spetsen av endoskopet lokaliserar området i bukspottkörteln som ska biopsieras, och en biopsinål förs genom en arbetskanal i endoskopet för att få vävnad från den misstänkta cancern. I slutändan är en vävnadsdiagnos det enda sättet att ställa diagnosen med säkerhet, och teamet av läkare arbetar för att få en vävnadsdiagnos på enklast möjliga sätt.
Förutom röntgenundersökningar kan misstanke om cancer i bukspottkörteln uppstå från höjningen av en "tumörmarkör", ett blodprov som kan vara onormalt högt hos personer med cancer i bukspottkörteln. Den tumörmarkör som oftast förknippas med cancer i bukspottkörteln kallas CA19-9. Det släpps ofta ut i blodomloppet av cancerceller i bukspottkörteln och kan vara förhöjt hos patienter som nyligen har upptäckt att de har cancer i bukspottkörteln. Tyvärr, även om CA19-9-testet är cancerrelaterat, är det inte specifikt för cancer i bukspottkörteln. Andra cancerformer såväl som vissa godartade tillstånd kan orsaka förhöjda CA 19-9. Ibland (cirka 20 % av tiden) kommer CA19-9 att vara på normala nivåer i blodet trots en bekräftad diagnos av pankreascancer, så tumörmarkören är inte perfekt. Det kan dock vara bra att följa under sjukdomsförloppet eftersom dess uppgång och fall kan korrelera med cancerns tillväxt och hjälpa till att vägleda lämplig terapi.
När cancer i bukspottskörteln väl har diagnostiserats är den "iscensatt". Bukspottkörtelcancer delas in i fyra stadier där steg 1 är det tidigaste stadiet (stadium 0 räknas inte) och stadium IV är det mest avancerade (metastaserande sjukdom). Följande är stadierna av pankreascancer enligt National Cancer Institute:
Steg 0 :Cancer finns endast i slemhinnan i bukspottkörtelns kanaler. Steg 0 kallas också carcinoma in situ.
Steg I :Cancer har bildats och finns endast i bukspottkörteln.
Steg II :Cancer kan ha spridit sig eller avancerat till närliggande vävnader och organ och lymfkörtlar nära bukspottkörteln.
Steg III :Cancer har spridit sig eller utvecklats till de stora blodkärlen nära bukspottkörteln och kan ha spridit sig till närliggande lymfkörtlar.
Steg IV :Cancer kan vara av vilken storlek som helst och har spridit sig till avlägsna organ, såsom levern, lungan och bukhålan. Det kan också ha spridit sig till organ och vävnader nära bukspottkörteln eller till lymfkörtlar. Detta stadium har också kallats slutstadiet pankreascancer.
Till skillnad från många cancerformer grupperas patienter med cancer i bukspottkörteln vanligtvis i tre kategorier, de med lokal sjukdom, de med lokalt avancerad, icke-opererbar sjukdom och de med metastaserande sjukdom. Initial terapi skiljer sig ofta åt för patienter i dessa tre grupper.
Patienter med stadium I och stadium II cancer tros ha lokal eller "resekterbar" cancer (cancer som kan avlägsnas helt med en operation). Patienter med cancer i stadium III har "lokalt avancerad, ooperbar" sjukdom. I den här situationen har möjligheten till bot gått förlorad men lokala behandlingar som strålterapi är fortfarande alternativ. Hos patienter med stadium IV bukspottkörtelcancer rekommenderas oftast kemoterapi som ett sätt att kontrollera symtomen relaterade till cancern och förlänga livet. Nedan kommer vi att gå igenom vanliga behandlingar för de tre grupperna av cancer i bukspottkörteln (resektabel, lokalt avancerad inoperabel och metastaserad pankreascancer).
If a pancreatic cancer is found at an early stage (stage I and stage II) and is contained locally within or around the pancreas, surgery may be recommended (resectable pancreatic cancer). Surgery is the only potentially curative treatment for pancreatic cancer. The surgical procedure most commonly performed to remove a pancreatic cancer is a Whipple procedure (pancreatoduodenectomy or pancreaticoduodenectomy). It often comprises removal of a portion of the stomach, the duodenum (the first part of the small intestine), pancreas, a portion of the main bile duct, lymph nodes, and gallbladder. It is important to be evaluated at a hospital with lots of experience performing pancreatic cancer surgery because the operation is a big one, and evidence shows that experienced surgeons better select people who can get through the surgery safely and also better judge who will most likely benefit from the operation. In experienced hands, the mortality from the surgery itself is less than 4%.
After the Whipple surgery, patients typically spend about one week in the hospital recovering from the operation. Complications from the surgery can include blood loss (anemia), leakage from the reconnected intestines or ducts, or slow return of bowel function. Recovery to presurgical health often can take several months.
After patients recover from a Whipple procedure for pancreatic cancer, treatment to reduce the risk of the cancer returning is a standard recommendation. This treatment, referred to as "adjuvant therapy (chemotherapy)," has proven to lower the risk of recurrent cancer. Typically, physicians recommend six months of adjuvant chemotherapy, sometimes with radiation incorporated into the treatment plan.
Some patients with pancreatic cancer experience blockage of bile and/or pancreas ducts and thus may need a surgeon to place a stent to allow drainage through the stent.
Unfortunately, only about 20 people out of 100 diagnosed with pancreatic cancer are found to have a tumor that is amenable to surgical resection or is borderline resectable. The rest have pancreatic tumors that are too locally advanced to completely remove or have metastatic spread at the time of diagnosis. Even among patients whose cancers are amenable to surgery, statistical data suggest that only 20% live 5 years. Most pancreatic cancer patients do not qualify for a pancreas transplant because of their advanced disease; most pancreas transplants are done in patients with diabetes that results from the removal of the endocrine portion of the pancreas and not for pancreatic cancer. Consequently, remission rates are fair to poor.
If a pancreatic cancer is found when it has grown into important local structures but not yet spread to distant sites, this is described as locally advanced, unresectable (inoperable) pancreatic cancer (stage III). The standard of care in the United States for the treatment of locally advanced cancer is a combination of low-dose chemotherapy given simultaneously with radiation treatments to the pancreas and surrounding tissues. Radiation treatments are designed to lower the risk of local growth of the cancer, thereby minimizing the symptoms that local progression causes (back or belly pain, nausea, loss of appetite, intestinal blockage, jaundice). Radiation treatments are typically given Monday through Friday for about five weeks. Chemotherapy given concurrently (at the same time; FOLFOX combination therapy) may improve the effectiveness of the radiation and may lower the risk for cancer spread outside the area where the radiation is delivered. When the radiation is completed and the patient has recovered, more chemotherapy often is recommended. Recently, newer forms of radiation delivery (proton therapy, stereotactic radiosurgery, gamma knife radiation, Nanoknife, CyberKnife radiation) have been utilized in locally advanced pancreatic cancer with varying degrees of success, but these treatments can be more toxic and are, for now, largely experimental; individuals should discuss with their doctors what treatment(s) are best for their condition.
Once a pancreatic cancer has spread beyond the vicinity of the pancreas and involves other organs, it has become a problem through the system. As a result, a systemic treatment is most appropriate and chemotherapy (for example, nab-paclitaxel [Abraxane] in combination with gemcitabine [Gemzar]) is recommended. Chemotherapy travels through the bloodstream and goes anywhere the blood flows and, as such, treats most of the body. It can attack a cancer that has spread through the body wherever it is found. In metastatic pancreatic cancer, chemotherapy is recommended for individuals healthy enough to receive it. It has been proven to both extend the lives of patients with pancreatic cancer and to improve their quality of life. These benefits are documented, but unfortunately the overall benefit from chemotherapy in pancreatic cancer treatment is modest and chemotherapy prolongs life for the average patient by only a few months. Chemotherapy options for patients with pancreatic cancer vary from treatment with a single chemotherapy agent like Tarceva or Onivyde to treatment with as many as two or three chemotherapy agents or immunotherapy agents given together (for example, capecitabine plus ruxolitinib). The aggressiveness of the treatment is determined by the cancer doctor (medical oncologist) and by the overall health and strength of the individual patient.
Side effects of treatment for pancreatic cancer vary depending on the type of treatment. For example, radiation treatment (which is a local treatment) side effects tend to accumulate throughout the course of radiation therapy and include fatigue, nausea, and diarrhea. Chemotherapy side effects depend on the type of chemotherapy given (less aggressive chemotherapy treatments typically cause fewer side effects whereas more aggressive combination regimens are more toxic) and can include fatigue, loss of appetite, change in taste, hair loss (although not usually), and lowering of the immune system with risk for infections (immunosuppression). While these lists of side effects may seem worrisome, radiation doctors (radiation oncologists) and medical oncologists have much better supportive medications than they did in years past to control any nausea, pain, diarrhea, or immunosuppression related to treatment. The risks associated with pancreatic cancer treatment must be weighed against the inevitable and devastating risks associated with uncontrolled pancreatic cancer and, if the treatments control progression of the cancer, most patients feel better on treatment than they otherwise would.
Pancreatic cancer is a difficult disease. Even for surgically resectable (and therefore potentially curable) pancreatic tumors, the risk of cancer recurrence and subsequent death remains high. Consequently, the prognosis of pancreatic cancer usually ranges from fair to poor. Only about 20% of patients undergoing a Whipple procedure for potentially curable pancreatic cancer live five years, with the rest surviving on average less than two years. For patients with incurable (locally advanced unresectable or metastatic) pancreatic cancer, survival is even shorter; typically, it is measured in months. With metastatic disease (stage IV), the average survival is just over six months. The American Cancer Society statistics suggest that for all stages of pancreatic cancer combined, the one-year survival rate is 20% and the mortality rate is 80%, while the five-year survival rate is 6% with a mortality rate of 94%. These rates are mainly based on patients diagnosed between 1985 and 2004 and are representative of those patients according to the American Cancer Society (ACS). These data-based survival rates are what are available currently, but they are only estimates and are not predictive about what may happen to each individual. Currently, the ACS advises patients to discuss their individual situation and prognosis with their treatment team of physicians. Doctors around the world continue to study pancreatic cancer and strive to improve treatments, but progress has been difficult to achieve.
Doctors and researchers all over the world are hard at work developing better treatments for pancreatic cancer. Cooperative cancer research led by centers of excellence in this country and many others continue daily to test new surgical techniques, radiation strategies, chemotherapy agents, and alternative therapies in an effort to improve care. Given the slow progress experienced over the last quarter century, many doctors feel that every eligible patient with pancreatic cancer should be offered enrollment in a research trial. New cytotoxic combinations of drugs are being tried in clinical trials. For example, Folfirinox, a new combination regimen consisting of four different chemicals has shown increased survival times for patients in clinical trials. In addition, patients who received one of two vaccines, GVAX and CRS-207, showed about a doubling of survival time compared to patients that did not receive the vaccine; this vaccine protocol is still undergoing clinical trials. For a complete list of clinical trials in pancreatic cancer treatment, please check online at http://www.cancer.gov.
Complimentary or alternative medicine is of unclear benefit in pancreatic cancer treatment. No specific complimentary or alternative therapy has been proven beneficial, but many adjunctive treatments have been tried. Compounds such as curcumin, the principle ingredient in turmeric, have shown efficacy in nonhuman research and are being tested in clinical trials in pancreatic cancer. Given the modest benefit derived from chemotherapy and radiation in this disease, alternative approaches in the treatment of pancreatic cancer in conjunction with (rather than instead of) standard treatment is warranted.
At this time, there is no known surveillance strategy to reduce the risk of pancreatic cancer for the general population. With only 48,900 new diagnoses a year, screening blood tests or X-rays have never been proven to be cost effective or beneficial. Additionally, doctors do not routinely screen individuals with family members diagnosed with pancreatic cancer aside from the rare instance where a known genetic risk factor is present. Some researchers suggest vitamin D blood levels above 40 ng/ml may reduce the risk of pancreatic cancer.
There are many fine organizations helping to provide support for individuals and families battling pancreatic cancer. Many hospitals provide support networks utilizing the expertise of trained social workers with experience in caring for people with cancer. Additionally, the Pancreatic Cancer Action Network (PANCAN) and the American Cancer Society both provide information and support for people living with pancreatic cancer. Visit their web sites at http://www.pancan.org and http://www.cancer.org. Diet recommendations can be found at ACS Guidelines on Nutrition and Physical Activity for Cancer Prevention.
Again, both PANCAN and the American Cancer Society are excellent resources for additional information regarding pancreatic cancer. The American Society of Clinical Oncology web site (http://www.cancer.net) also boasts a wealth of information for patients, family members, and professionals interesting in learning more about this disease. November is Pancreatic Awareness Month with the goal to make pancreas care an everyday event (http://daysofyear.com/pancreatic-cancer-awareness-month/).
 Hur kan jag förbättra min maghälsa?
Under de senaste åren har forskare lärt sig att ett hälsosamt matsmältningssystem är viktigt för den allmänna hälsan. Din matsmältningskanal bearbetar maten du äter så att du kan använda den för energ
Hur kan jag förbättra min maghälsa?
Under de senaste åren har forskare lärt sig att ett hälsosamt matsmältningssystem är viktigt för den allmänna hälsan. Din matsmältningskanal bearbetar maten du äter så att du kan använda den för energ
 SCD Frittata (enkelt och snabbt)
När livet ger dig citroner gör du lemonad... eller hur? Vad sägs om en SCD-frittata. Jag försökte hjälpa till att rädda miljön genom att bara ta en papperspåse i kassan (glömde mina återanvändbara).
SCD Frittata (enkelt och snabbt)
När livet ger dig citroner gör du lemonad... eller hur? Vad sägs om en SCD-frittata. Jag försökte hjälpa till att rädda miljön genom att bara ta en papperspåse i kassan (glömde mina återanvändbara).
 Prova dessa 5 läckra UltraInflamX Plus 360°®-recept
För personer som kan behöva avancerat stöd för näringsbrister på grund av malabsorption, UltraInflamX Plus 360°® är ett medicinskt livsmedel som erbjuder stöd för näringshantering av nedsatt tarmfunkt
Prova dessa 5 läckra UltraInflamX Plus 360°®-recept
För personer som kan behöva avancerat stöd för näringsbrister på grund av malabsorption, UltraInflamX Plus 360°® är ett medicinskt livsmedel som erbjuder stöd för näringshantering av nedsatt tarmfunkt