 Slika muškarca s rakom gušterače, iStock
Slika muškarca s rakom gušterače, iStock Rak gušterače obično ne uzrokuje simptome dok ne naraste, pa se najčešće dijagnosticira u uznapredovalim stadijima, a ne u ranom tijeku bolesti. U nekim slučajevima, žutica (žućkasta promjena boje kože i bjeloočnica) bez boli može biti rani znak raka gušterače. Ostali simptomi koji se mogu pojaviti kod uznapredovale bolesti su:
Mogu biti prisutni i blijeda stolica, bol u leđima, bol u trbuhu, tamna mokraća, nadutost u trbuhu, proljev i povećani limfni čvorovi na vratu.
Pročitajte više o simptomima raka gušterače »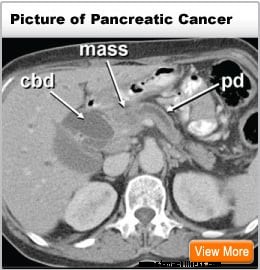
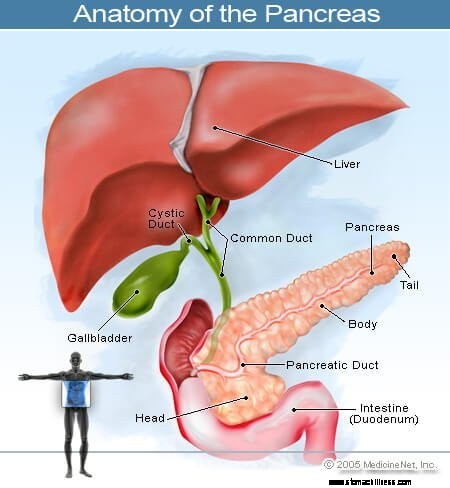 Rak koji počinje u pankreasu naziva se rak gušterače. Ova slika gušterače pokazuje njezin položaj u stražnjem dijelu trbuha, iza želuca.
Rak koji počinje u pankreasu naziva se rak gušterače. Ova slika gušterače pokazuje njezin položaj u stražnjem dijelu trbuha, iza želuca. Gušterača je organ koji proizvodi hormone u trbuhu koji se nalazi ispred kralježnice iznad razine pupka. Obavlja dvije glavne funkcije:
Enzimi pomažu probavi usitnjavajući bjelančevine, masti i ugljikohidrate na manje dijelove kako bi ih tijelo lakše apsorbiralo i koristilo kao gradivni blokovi za tkiva i energiju. Enzimi napuštaju gušteraču putem sustava cijevi zvanih "vodovi" koji povezuju gušteraču s crijevima gdje se enzimi miješaju s progutanom hranom.
Gušterača se nalazi duboko u abdomenu i u neposrednoj je blizini mnogih važnih struktura kao što su tanko crijevo (duodenum) i žučni kanali, kao i važne krvne žile i živci.
Svake sekunde svakog dana u našem tijelu događa se masivni proces uništenja i popravka. Ljudsko tijelo se sastoji od trilijuna stanica i svaki dan se milijarde stanica troše ili uništavaju. Svaki put kada tijelo napravi novu stanicu da zamijeni onu koja se istroši, tijelo pokušava napraviti savršenu kopiju stanice koja odumire, obično tako što se slične zdrave stanice dijele na dvije stanice jer je ta stanica koja umire imala posao. , a novoizrađena ćelija mora biti sposobna obavljati istu funkciju. Unatoč izvanredno elegantnim sustavima za uređivanje pogrešaka u ovom procesu, tijelo dnevno čini desetke tisuća pogrešaka u normalnoj diobi stanica bilo zbog slučajnih pogrešaka ili zbog pritiska okoline unutar tijela. Većina ovih pogrešaka se ispravlja ili greška dovodi do smrti novonastale ćelije, a zatim se stvara još jedna nova stanica. Ponekad se napravi pogreška koja, umjesto da inhibira sposobnost stanice da raste i preživi, dopušta novonastaloj stanici da raste na nereguliran način. Kada se to dogodi, ta stanica postaje stanica raka koja se može dijeliti neovisno o provjerama i ravnotežama koje kontroliraju normalnu diobu stanica. Stanica raka se umnožava i nastaje kancerogen ili maligni tumor.
Tumori spadaju u dvije kategorije:"benigni" tumori i "maligni" ili kancerozni tumori. Koja je razlika? Odgovor je da benigni tumor raste samo u tkivu iz kojeg nastaje. Benigni tumori ponekad mogu narasti prilično veliki ili brzo rasti i uzrokovati teške simptome. Na primjer, fibroid u ženskoj maternici može uzrokovati krvarenje ili bol, ali nikada neće izaći izvan maternice, zahvatiti okolna tkiva ili rasti kao novi tumor drugdje u tijelu (metastazirati). Fibroidi, kao i svi benigni tumori, nemaju sposobnost izbacivanja stanica u krv i limfni sustav i ne mogu putovati na druga mjesta u tijelu i rasti. Rak, s druge strane, može izbaciti stanice iz izvornog tumora koje mogu plutati poput sjemenki maslačka na vjetru kroz krvotok ili limfne kanale, slijetajući u tkiva udaljena od tumora, razvijajući se u nove tumore u drugim dijelovima tijela. Ovaj proces, koji se naziva metastaza, je definirajuća karakteristika kancerogenog tumora. Rak gušterače je, nažalost, posebno dobar model za ovaj proces. Rak gušterače može rano metastazirati u druge organe na ovaj način. Također mogu rasti i izravno napadati susjedne strukture, često onemogućujući kirurško uklanjanje tumora.
Rakovi se nazivaju prema tkivima iz kojih nastaje primarni tumor. Dakle, rak pluća koji putuje u jetru nije "rak jetre", već se opisuje kao metastatski rak pluća, a pacijent s rakom dojke koji se širi na mozak ne opisuje se kao da ima "tumor na mozgu", već kao da ima metastatski rak dojke.


Što je policitemija vera?
Saznajte više na
Rak koji se razvija unutar gušterače spada u dvije glavne kategorije:(1) karcinomi endokrinog gušterače (dio koji stvara inzulin i druge hormone) nazivaju se "stanice otočića" ili "neuroendokrini tumori gušterače ili PNET" i (2) karcinomi egzokrine gušterače (dio koji stvara enzime). Rak otočnih stanica je rijedak i obično raste sporo u usporedbi s egzokrinim karcinomom gušterače. Tumori otočnih stanica često otpuštaju hormone u krvotok, a dodatno ih karakteriziraju hormoni koje proizvode (inzulin, glukagon, gastrin i drugi hormoni). Rak egzokrine gušterače (egzokrini karcinomi) razvijaju se iz stanica koje oblažu sustav kanala koji isporučuju enzime u tanko crijevo i obično se nazivaju adenokarcinomi gušterače. Karcinom skvamoznih stanica gušterače je rijedak. Adenokarcinom gušterače obuhvaća većinu svih duktalnih karcinoma gušterače i glavni je predmet ovog pregleda.
Stanice koje oblažu kanale u egzokrinom pankreasu dijele se brže od tkiva koje ih okružuje. Iz razloga koje mi ne razumijemo, ove stanice mogu pogriješiti kada kopiraju svoju DNK dok se dijele kako bi zamijenile druge umiruće stanice. Na taj se način može napraviti abnormalna stanica. Kada se abnormalna duktalna stanica počne dijeliti na nereguliran način, može nastati rast koji se sastoji od stanica abnormalnog izgleda i funkcioniranja. Abnormalne promjene koje se mogu prepoznati pod mikroskopom nazivaju se "displazija". Često displastične stanice mogu tijekom vremena pretrpjeti dodatne DNK pogreške i postati još abnormalnije. Kada te displastične stanice prodiru kroz zidove kanala iz kojeg nastaju u okolno tkivo, displazija je postala rak.
U studiji objavljenoj 2016., istraživači su izvijestili o analizi gena u 456 duktalnih adenokarcinoma gušterače. Naknadna analiza ekspresije ovih adenokarcinoma omogućila je njihovo definiranje u četiri podtipa. Ovi podtipovi nisu ranije bili razaznati. Podtipovi uključuju:
Ova nova otkrića mogu omogućiti da se budući pacijenti s rakom liječe konkretnije ovisno o njihovoj podtipi i, nadamo se, učinkovitije. Na primjer, imunogeni podtip bi mogao reagirati na terapiju u kojoj je imunološki sustav rekonstruiran da napadne ove vrste stanica raka.
Rak gušterače ne smije se miješati s pojmom pankreatitis. Pankreatitis se jednostavno definira kao upala gušterače i uglavnom je uzrokovan zlouporabom alkohola i/ili stvaranjem žučnih kamenaca (oko 80% do 90%). Ipak, kronični pankreatitis povezan je s rakom gušterače.
Godišnje se u Sjedinjenim Državama dogodi oko 53.670 slučajeva raka gušterače. Većina ljudi koji razviju rak gušterače to čine bez ikakvih predisponirajućih čimbenika rizika. Međutim, možda najveći čimbenik rizika je starenje; biti stariji od 60 godina stavlja pojedinca u veći rizik. Rijetko mogu postojati obiteljski ili nasljedni genetski sindromi koji proizlaze iz genetskih mutacija koje se javljaju u obiteljima i dovode pojedince u veći rizik, kao što su BRCA-2 i, u manjoj mjeri, mutacije gena BRCA-1. Obiteljski sindromi su neobični, ali važno je obavijestiti liječnika ako je još nekome u obitelji dijagnosticiran rak, posebno rak gušterače. Osim toga, smatra se da određena ponašanja ili stanja neznatno povećavaju rizik pojedinca za razvoj raka gušterače. Na primjer, Afroamerikanci mogu biti pod većim rizikom kao i pojedinci s članovima bliske obitelji kojima je prethodno dijagnosticiran rak gušterače. Ostala ponašanja ili stanja koja mogu dovesti ljude u opasnost uključuju pušenje, pretilost, sjedilački način života, povijest dijabetesa, kroničnu upalu gušterače (pankreatitis) i masnu (ili zapadnjačku) prehranu. Prethodna operacija želuca može umjereno povećati nečiji rizik, kao i određene kronične infekcije kao što su hepatitis B i H. pylori (bakterijska infekcija sluznice želuca). Određeni lijekovi (sitagliptin [Januvia], eksenatid [Byetta], liraglutid [Victoza] i metformin i sitagliptin [Janumet]) povezani su s razvojem raka gušterače. Neke vrste cista gušterače mogu izložiti pojedince riziku od razvoja raka gušterače. Nekoliko istraživača sugerira da pijenje kave i gaziranih pića povećava rizik od raka gušterače. Kada rak gušterače počne, obično počinje u stanicama koje oblažu kanale gušterače i naziva se adenokarcinom gušterače ili ekzokrini rak gušterače . Unatoč gore navedenim povezanim rizicima, kod većine ljudi koji razviju rak gušterače nije pronađen nikakav prepoznatljiv uzrok.
Klikom na "Pošalji" prihvaćam MedicineNet Uvjete i odredbe i Politiku privatnosti. Također se slažem s primanjem e-poruka od MedicineNeta i razumijem da se mogu odbiti od pretplate na MedicineNet u bilo kojem trenutku.
Budući da se gušterača nalazi duboko u trbuhu ispred kralježnice, rak gušterače često tiho raste mjesecima prije nego što se otkrije. Rani simptomi raka i/ili prvi znakovi mogu biti odsutni ili prilično suptilni. Lakše prepoznatljivi simptomi se razvijaju kada tumor naraste dovoljno da pritisne druge obližnje strukture, kao što su živci (što uzrokuje generaliziranu bol i/ili bol u leđima), crijeva (koja utječe na apetit i uzrokuje mučninu zajedno s gubitkom težine) ili žučnih puteva (što uzrokuje žuticu ili žutilo kože i može uzrokovati gubitak apetita i svrbež). Simptomi kod žena rijetko se razlikuju od onih u muškaraca. Nakon što tumor izbaci stanice raka u krv i limfni sustav i metastazira, obično se javljaju dodatni simptomi, ovisno o mjestu metastaze. Česta mjesta metastaza raka gušterače uključuju jetru, limfne čvorove i sluznicu abdomena (naziva se peritoneum; ascitna tekućina može se akumulirati u metastatskom karcinomu gušterače). Nažalost, većina karcinoma gušterače nalazi se nakon što je rak narastao ili napredovao izvan pankreasa ili je metastazirao na druga mjesta.
Općenito, znakove i simptome raka gušterače mogu proizvesti egzokrine ili endokrine stanice raka. Mnogi znakovi i simptomi egzokrinog karcinoma gušterače rezultat su začepljenja kanala koji putuje kroz gušteraču od jetre noseći žuč do crijeva. Simptomi egzokrinog karcinoma gušterače uključuju
Znakovi i simptomi endokrinog karcinoma gušterače često su povezani s viškom hormona koji oni proizvode i posljedično s nizom različitih simptoma. Takvi simptomi povezani su s hormonima i su sljedeći:
Nefunkcionalni neuroendokrini tumori ne stvaraju višak hormona, ali mogu narasti i proširiti se iz gušterače. Simptomi tada mogu biti poput bilo kojeg od gore opisanih endokrinih karcinoma gušterače.
Većina ljudi ne mora biti podvrgnuta probiru na rak gušterače, a testovi dostupni za probir često su složeni, rizični, skupi ili neosjetljivi u ranim fazama raka. Oni koji se mogu kvalificirati obično imaju niz čimbenika koji povećavaju rizik od raka gušterače, kao što su ciste gušterače, srodnici u prvom stupnju s rakom gušterače ili povijest genetskih sindroma povezanih s rakom gušterače. Većina testova probira sastoji se od CT skeniranja, ultrazvuka, magnetske rezonancije kolangiopankreatografije (MRCP), endoskopske retrogradne kolangiopankreatografije (ERCP) ili endoskopskog ultrazvuka. Nažalost, rano je otkrivanje raka gušterače teško jer je prisutno malo ili nimalo simptoma.
Većina ljudi s karcinomom gušterače prvo ode svom liječniku primarne zdravstvene zaštite žaleći se na nespecifične simptome (vidi gornji dio o simptomima). Neki znakovi upozorenja uključuju bol, gastrointestinalne simptome, gubitak težine, umor i povećanu količinu tekućine u trbuhu. Ove tegobe pokreću evaluaciju često uključujući fizički pregled (obično normalan), krvne pretrage, rendgenske snimke i ultrazvuk. Ako je prisutan rak gušterače, vjerojatnost da će ultrazvuk otkriti abnormalnost u gušterači je oko 75%. Ako je problem identificiran ili postoji sumnja, često se kao sljedeći korak u evaluaciji provodi kompjuterizirana tomografija (CT); neki kliničari preferiraju MRI. Ako se vidi masa gušterače, to izaziva sumnju na rak gušterače i liječnik tada obavlja biopsiju kako bi se postavila dijagnoza.
Različite strategije mogu se koristiti za izvođenje biopsije sumnjivog karcinoma. Često će se koristiti biopsija jetre iglom kroz trbušnu stijenku (perkutana biopsija jetre) ako se čini da se rak proširio na jetru. Ako tumor ostane lokaliziran na gušterači, biopsija gušterače se obično izvodi izravno uz pomoć CT-a. Izravna biopsija također se može napraviti putem endoskopa koji se stavlja u grlo i u crijeva. Kamera na vrhu endoskopa omogućuje endoskopistu da napreduje endoskopom unutar crijeva. Ultrazvučni uređaj na vrhu endoskopa locira područje gušterače za biopsiju, a igla za biopsiju prolazi kroz radni kanal u endoskopu kako bi se dobilo tkivo iz sumnjivog karcinoma. U konačnici, dijagnoza tkiva jedini je način da se dijagnoza postavi sa sigurnošću, a liječnički tim radi na dobivanju dijagnoze tkiva na najlakši mogući način.
Osim radioloških pretraga, sumnja na rak gušterače može proizaći iz povišenja "tumorskog biljega", krvnog testa koji može biti nenormalno visok u ljudi s rakom gušterače. Tumorski marker koji se najčešće povezuje s rakom gušterače naziva se CA19-9. Često ga stanice raka gušterače otpuštaju u krvotok i može biti povišen u pacijenata kod kojih je otkriveno da imaju rak gušterače. Nažalost, iako je test CA19-9 povezan s rakom, nije specifičan za rak gušterače. Drugi karcinomi, kao i neka benigna stanja mogu uzrokovati povišenje CA 19-9. Ponekad (oko 20% vremena) CA19-9 će biti na normalnim razinama u krvi unatoč potvrđenoj dijagnozi raka gušterače, tako da tumorski marker nije savršen. Međutim, može biti korisno pratiti tijekom bolesti jer njezin porast i pad mogu korelirati s rastom raka i pomoći u usmjeravanju odgovarajuće terapije.
Jednom kada se dijagnosticira rak gušterače, on se "inscenira". Rak gušterače podijeljen je u četiri stadija, pri čemu je 1. stadij najraniji (stadij 0 se ne računa) i stadij IV najnapredniji (metastatska bolest). Sljedeće su faze raka gušterače prema Nacionalnom institutu za rak:
Faza 0 :Rak se nalazi samo u sluznici kanala gušterače. Stadij 0 također se naziva karcinom in situ.
I. faza :Rak je nastao i nalazi se samo u gušterači.
II. faza :Rak se možda proširio ili uznapredovao u obližnje tkivo i organe i limfne čvorove u blizini gušterače.
III. faza :Rak se proširio ili napredovao na glavne krvne žile u blizini gušterače i možda se proširio na obližnje limfne čvorove.
Stapa IV :Rak može biti bilo koje veličine i proširio se na udaljene organe, kao što su jetra, pluća i peritonealna šupljina. Također se može proširiti na organe i tkiva u blizini gušterače ili na limfne čvorove. Ovaj stadij se također naziva krajnjim stadijem karcinoma gušterače.
Međutim, za razliku od mnogih karcinoma, pacijenti s karcinomom gušterače obično se grupiraju u tri kategorije, oni s lokalnom bolešću, oni s lokalno uznapredovalom bolešću koja se ne može resektabilnom bolešću i oni s metastatskom bolešću. Početna terapija se često razlikuje za pacijente u ove tri skupine.
Smatra se da pacijenti sa stadijem I i II stadijem raka imaju lokalni ili "resektabilni" rak (rak koji se može potpuno ukloniti operacijom). Bolesnici sa stadijem raka III imaju "lokalno uznapredovalu, neresektabilnu" bolest. U ovoj situaciji, prilika za izlječenje je izgubljena, ali lokalni tretmani kao što je terapija zračenjem ostaju opcije. U bolesnika s karcinomom gušterače IV stadija, kemoterapija se najčešće preporučuje kao sredstvo za kontrolu simptoma povezanih s rakom i produljenje života. U nastavku ćemo pregledati uobičajene tretmane za tri skupine karcinoma gušterače (resektabilni, lokalno uznapredovali neresektabilni i metastatski karcinom gušterače).
Ako se rak gušterače pronađe u ranoj fazi (stadij I i stadij II) i lokaliziran je unutar ili oko gušterače, može se preporučiti kirurški zahvat (resektabilni karcinom gušterače). Kirurgija je jedini potencijalno izlječivi tretman za rak gušterače. The surgical procedure most commonly performed to remove a pancreatic cancer is a Whipple procedure (pancreatoduodenectomy or pancreaticoduodenectomy). It often comprises removal of a portion of the stomach, the duodenum (the first part of the small intestine), pancreas, a portion of the main bile duct, lymph nodes, and gallbladder. It is important to be evaluated at a hospital with lots of experience performing pancreatic cancer surgery because the operation is a big one, and evidence shows that experienced surgeons better select people who can get through the surgery safely and also better judge who will most likely benefit from the operation. In experienced hands, the mortality from the surgery itself is less than 4%.
After the Whipple surgery, patients typically spend about one week in the hospital recovering from the operation. Complications from the surgery can include blood loss (anemia), leakage from the reconnected intestines or ducts, or slow return of bowel function. Recovery to presurgical health often can take several months.
After patients recover from a Whipple procedure for pancreatic cancer, treatment to reduce the risk of the cancer returning is a standard recommendation. This treatment, referred to as "adjuvant therapy (chemotherapy)," has proven to lower the risk of recurrent cancer. Typically, physicians recommend six months of adjuvant chemotherapy, sometimes with radiation incorporated into the treatment plan.
Some patients with pancreatic cancer experience blockage of bile and/or pancreas ducts and thus may need a surgeon to place a stent to allow drainage through the stent.
Unfortunately, only about 20 people out of 100 diagnosed with pancreatic cancer are found to have a tumor that is amenable to surgical resection or is borderline resectable. The rest have pancreatic tumors that are too locally advanced to completely remove or have metastatic spread at the time of diagnosis. Even among patients whose cancers are amenable to surgery, statistical data suggest that only 20% live 5 years. Most pancreatic cancer patients do not qualify for a pancreas transplant because of their advanced disease; most pancreas transplants are done in patients with diabetes that results from the removal of the endocrine portion of the pancreas and not for pancreatic cancer. Consequently, remission rates are fair to poor.
If a pancreatic cancer is found when it has grown into important local structures but not yet spread to distant sites, this is described as locally advanced, unresectable (inoperable) pancreatic cancer (stage III). The standard of care in the United States for the treatment of locally advanced cancer is a combination of low-dose chemotherapy given simultaneously with radiation treatments to the pancreas and surrounding tissues. Radiation treatments are designed to lower the risk of local growth of the cancer, thereby minimizing the symptoms that local progression causes (back or belly pain, nausea, loss of appetite, intestinal blockage, jaundice). Radiation treatments are typically given Monday through Friday for about five weeks. Chemotherapy given concurrently (at the same time; FOLFOX combination therapy) may improve the effectiveness of the radiation and may lower the risk for cancer spread outside the area where the radiation is delivered. When the radiation is completed and the patient has recovered, more chemotherapy often is recommended. Recently, newer forms of radiation delivery (proton therapy, stereotactic radiosurgery, gamma knife radiation, Nanoknife, CyberKnife radiation) have been utilized in locally advanced pancreatic cancer with varying degrees of success, but these treatments can be more toxic and are, for now, largely experimental; individuals should discuss with their doctors what treatment(s) are best for their condition.
Once a pancreatic cancer has spread beyond the vicinity of the pancreas and involves other organs, it has become a problem through the system. As a result, a systemic treatment is most appropriate and chemotherapy (for example, nab-paclitaxel [Abraxane] in combination with gemcitabine [Gemzar]) is recommended. Chemotherapy travels through the bloodstream and goes anywhere the blood flows and, as such, treats most of the body. It can attack a cancer that has spread through the body wherever it is found. In metastatic pancreatic cancer, chemotherapy is recommended for individuals healthy enough to receive it. It has been proven to both extend the lives of patients with pancreatic cancer and to improve their quality of life. These benefits are documented, but unfortunately the overall benefit from chemotherapy in pancreatic cancer treatment is modest and chemotherapy prolongs life for the average patient by only a few months. Chemotherapy options for patients with pancreatic cancer vary from treatment with a single chemotherapy agent like Tarceva or Onivyde to treatment with as many as two or three chemotherapy agents or immunotherapy agents given together (for example, capecitabine plus ruxolitinib). The aggressiveness of the treatment is determined by the cancer doctor (medical oncologist) and by the overall health and strength of the individual patient.
Side effects of treatment for pancreatic cancer vary depending on the type of treatment. For example, radiation treatment (which is a local treatment) side effects tend to accumulate throughout the course of radiation therapy and include fatigue, nausea, and diarrhea. Chemotherapy side effects depend on the type of chemotherapy given (less aggressive chemotherapy treatments typically cause fewer side effects whereas more aggressive combination regimens are more toxic) and can include fatigue, loss of appetite, change in taste, hair loss (although not usually), and lowering of the immune system with risk for infections (immunosuppression). While these lists of side effects may seem worrisome, radiation doctors (radiation oncologists) and medical oncologists have much better supportive medications than they did in years past to control any nausea, pain, diarrhea, or immunosuppression related to treatment. The risks associated with pancreatic cancer treatment must be weighed against the inevitable and devastating risks associated with uncontrolled pancreatic cancer and, if the treatments control progression of the cancer, most patients feel better on treatment than they otherwise would.
Pancreatic cancer is a difficult disease. Even for surgically resectable (and therefore potentially curable) pancreatic tumors, the risk of cancer recurrence and subsequent death remains high. Consequently, the prognosis of pancreatic cancer usually ranges from fair to poor. Only about 20% of patients undergoing a Whipple procedure for potentially curable pancreatic cancer live five years, with the rest surviving on average less than two years. For patients with incurable (locally advanced unresectable or metastatic) pancreatic cancer, survival is even shorter; typically, it is measured in months. With metastatic disease (stage IV), the average survival is just over six months. The American Cancer Society statistics suggest that for all stages of pancreatic cancer combined, the one-year survival rate is 20% and the mortality rate is 80%, while the five-year survival rate is 6% with a mortality rate of 94%. These rates are mainly based on patients diagnosed between 1985 and 2004 and are representative of those patients according to the American Cancer Society (ACS). These data-based survival rates are what are available currently, but they are only estimates and are not predictive about what may happen to each individual. Currently, the ACS advises patients to discuss their individual situation and prognosis with their treatment team of physicians. Doctors around the world continue to study pancreatic cancer and strive to improve treatments, but progress has been difficult to achieve.
Doctors and researchers all over the world are hard at work developing better treatments for pancreatic cancer. Cooperative cancer research led by centers of excellence in this country and many others continue daily to test new surgical techniques, radiation strategies, chemotherapy agents, and alternative therapies in an effort to improve care. Given the slow progress experienced over the last quarter century, many doctors feel that every eligible patient with pancreatic cancer should be offered enrollment in a research trial. New cytotoxic combinations of drugs are being tried in clinical trials. For example, Folfirinox, a new combination regimen consisting of four different chemicals has shown increased survival times for patients in clinical trials. In addition, patients who received one of two vaccines, GVAX and CRS-207, showed about a doubling of survival time compared to patients that did not receive the vaccine; this vaccine protocol is still undergoing clinical trials. For a complete list of clinical trials in pancreatic cancer treatment, please check online at http://www.cancer.gov.
Complimentary or alternative medicine is of unclear benefit in pancreatic cancer treatment. No specific complimentary or alternative therapy has been proven beneficial, but many adjunctive treatments have been tried. Compounds such as curcumin, the principle ingredient in turmeric, have shown efficacy in nonhuman research and are being tested in clinical trials in pancreatic cancer. Given the modest benefit derived from chemotherapy and radiation in this disease, alternative approaches in the treatment of pancreatic cancer in conjunction with (rather than instead of) standard treatment is warranted.
At this time, there is no known surveillance strategy to reduce the risk of pancreatic cancer for the general population. With only 48,900 new diagnoses a year, screening blood tests or X-rays have never been proven to be cost effective or beneficial. Additionally, doctors do not routinely screen individuals with family members diagnosed with pancreatic cancer aside from the rare instance where a known genetic risk factor is present. Some researchers suggest vitamin D blood levels above 40 ng/ml may reduce the risk of pancreatic cancer.
There are many fine organizations helping to provide support for individuals and families battling pancreatic cancer. Many hospitals provide support networks utilizing the expertise of trained social workers with experience in caring for people with cancer. Additionally, the Pancreatic Cancer Action Network (PANCAN) and the American Cancer Society both provide information and support for people living with pancreatic cancer. Visit their web sites at http://www.pancan.org and http://www.cancer.org. Diet recommendations can be found at ACS Guidelines on Nutrition and Physical Activity for Cancer Prevention.
Again, both PANCAN and the American Cancer Society are excellent resources for additional information regarding pancreatic cancer. The American Society of Clinical Oncology web site (http://www.cancer.net) also boasts a wealth of information for patients, family members, and professionals interesting in learning more about this disease. November is Pancreatic Awareness Month with the goal to make pancreas care an everyday event (http://daysofyear.com/pancreatic-cancer-awareness-month/).
 Mjesec svijesti o IBS-u
Mjesec svijesti o IBS-u
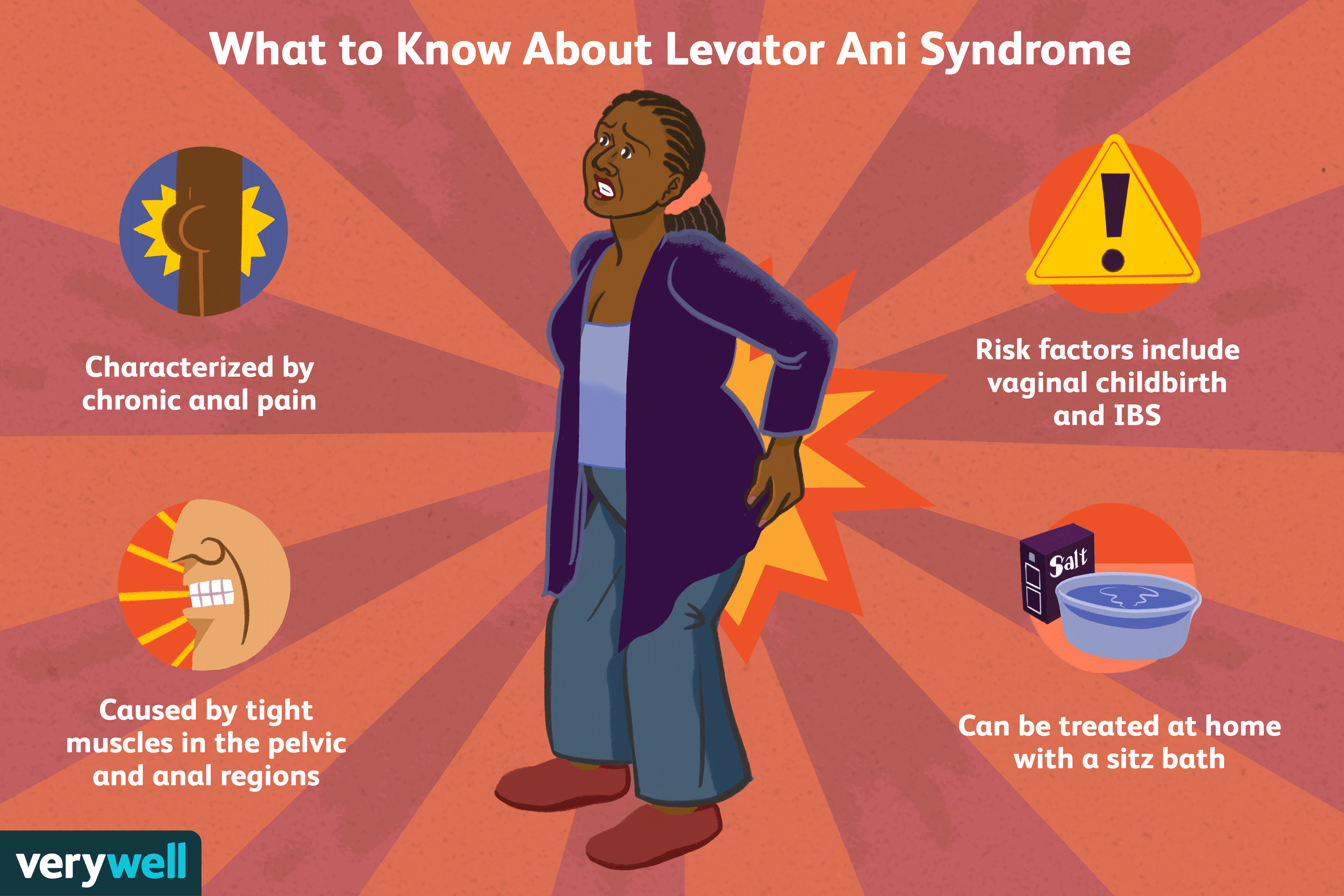 Pregled Levator Ani sindroma
Pregled Levator Ani sindroma
 Jeste li dio epidemije probavnih bolesti? (i što učiniti u vezi s tim)
Jeste li dio epidemije probavnih bolesti? (i što učiniti u vezi s tim)
 Pulule za kontrolu rađanja povučene zbog opasnosti od neželjene trudnoće
Pulule za kontrolu rađanja povučene zbog opasnosti od neželjene trudnoće
 Studija otkriva antivirusne učinke kurkumina
Studija otkriva antivirusne učinke kurkumina
 Rješavanje problema:razlika između bolesnog i ozdravljenja
Rješavanje problema:razlika između bolesnog i ozdravljenja
 Uloga upale u sindromu iritabilnog crijeva
Konvencionalna mudrost oduvijek je smatrala da se upala ne vidi kod pacijenata sa sindromom iritabilnog crijeva (IBS). Pa, vremena se možda mijenjaju. Najmodernija istraživanja počela su pronalaziti d
Uloga upale u sindromu iritabilnog crijeva
Konvencionalna mudrost oduvijek je smatrala da se upala ne vidi kod pacijenata sa sindromom iritabilnog crijeva (IBS). Pa, vremena se možda mijenjaju. Najmodernija istraživanja počela su pronalaziti d
 Koji su simptomi celijakije u odraslih?
Što je celijakija u odraslih? Celijakija može dovesti do različitih simptoma zbog oštećenja crijeva. Zapravo, postoji više od 200 poznatih simptoma celijakije. Celijakija je imunološka reakcija
Koji su simptomi celijakije u odraslih?
Što je celijakija u odraslih? Celijakija može dovesti do različitih simptoma zbog oštećenja crijeva. Zapravo, postoji više od 200 poznatih simptoma celijakije. Celijakija je imunološka reakcija
 Ultimate SIBO božićni jelovnik
Ultimativni SIBO božićni jelovnik Budući da je Božić pred vratima, još uvijek se pitate što jesti za svoj svečani obrok? Nikad se ne plašite! Pokrili smo vas našim Ultimate SIBO božićnim jelovnikom.
Ultimate SIBO božićni jelovnik
Ultimativni SIBO božićni jelovnik Budući da je Božić pred vratima, još uvijek se pitate što jesti za svoj svečani obrok? Nikad se ne plašite! Pokrili smo vas našim Ultimate SIBO božićnim jelovnikom.