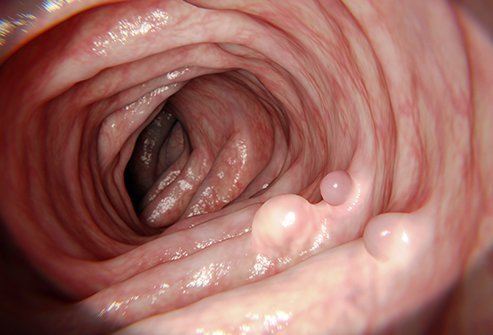
 Polypy hrubého čreva sa môžu zmeniť na rakovinu hrubého čreva.
Polypy hrubého čreva sa môžu zmeniť na rakovinu hrubého čreva.
Testujú sa štyri testy na okultné krvácanie (FOBT) vo výkaloch (stolici);
Polypy hrubého čreva sú výrastky, ktoré sa vyskytujú na vnútornej výstelke hrubého čreva (hrubého čreva) a zvyčajne vyčnievajú do hrubého čreva. Polypy sa tvoria, keď sa genetický materiál v bunkách lemujúcich hrubé črevo zmení a stane sa abnormálnym (mutuje). Normálne sú nezrelé bunky lemujúce hrubé črevo naprogramované tak, aby sa delili (množili), dozrievali a potom umierali veľmi konzistentným a včasným spôsobom. Genetické zmeny, ktoré sa vyskytujú vo výstelkových bunkách, však bránia bunkám dozrieť a bunky neumierajú. To vedie k akumulácii nezrelých, geneticky abnormálnych buniek, čo nakoniec vedie k tvorbe polypov. Mutácie sa môžu vyskytnúť ako sporadická udalosť po narodení alebo môžu byť prítomné už pred narodením.
Deväťdesiatpäť percent polypov hrubého čreva nespôsobuje symptómy ani znaky a sú objavené počas skríningu alebo kolonoskopie.
Keď sa objavia príznaky alebo príznaky, môžu zahŕňať:
Polypy hrubého čreva sú veľmi časté. Ich prevalencia sa zvyšuje, keď ľudia starnú; vo veku 60 rokov bude mať jedna tretina alebo viac ľudí aspoň jeden polyp. Ak má osoba polyp hrubého čreva, je pravdepodobnejšie, že bude mať ďalšie polypy inde v hrubom čreve a je pravdepodobnejšie, že neskôr vytvorí nové polypy. U malej podskupiny pacientov s polypmi hrubého čreva existuje familiárna genetická abnormalita, ktorá spôsobuje, že sa u pacientov a ďalších členov ich rodín vyvinie väčší počet polypov, vyvinú sa v ranom veku a častejšie sa z nich stanú rakovinové.
Polypy hrubého čreva sú dôležité, pretože môžu spôsobiť rakovinu hrubého čreva (kolorektálny karcinóm). Typ polypu predpovedá, u koho je väčšia pravdepodobnosť vzniku ďalších polypov a rakoviny hrubého čreva. Polypy spôsobujú ďalšie problémy (o ktorých sa bude diskutovať), ale najviac znepokojuje smrteľná povaha rakoviny hrubého čreva.
Z benígnych polypov sa stávajú malígne polypy (rakovina) s ďalšími mutáciami a zmenami v genetickom materiáli buniek (génoch). Bunky sa začnú nekontrolovateľne deliť a rozmnožovať, niekedy vzniká väčší polyp. Na začiatku sú čoraz viac geneticky abnormálne bunky obmedzené na vrstvu buniek, ktorá lemuje vnútro hrubého čreva. Bunky si potom vyvinú schopnosť preniknúť hlbšie do steny hrubého čreva. Jednotlivé bunky si tiež rozvíjajú schopnosť oddeliť sa od polypu a šíriť sa do lymfatických kanálov cez stenu hrubého čreva do miestnych lymfatických uzlín a potom do celého tela, čo je proces nazývaný metastáza, aj keď je to nezvyčajné, pokiaľ rakovina neprenikne do stena hrubého čreva.
Prechod z benígneho na malígny polyp možno vidieť pod mikroskopom. V skoršej fáze prechodu, nazývanej dysplázia nízkeho stupňa (dysplázia =abnormálna tvorba), sa bunky a ich vzájomné vzťahy stanú abnormálnymi. Keď sa bunky a ich vzťahy stanú ešte abnormálnejšími, nazýva sa to dysplázia vysokého stupňa. Dysplázia vysokého stupňa vyvoláva väčšie obavy, pretože bunky sú jasne rakovinové, hoci sú obmedzené na najvnútornejšiu výstelku hrubého čreva; až na zriedkavé výnimky ešte nemajú vyvinuté schopnosti invázie a metastázovania (šírenia sa do iných častí tela). Ak sa neodstránia, môže dôjsť k invázii a metastáze.
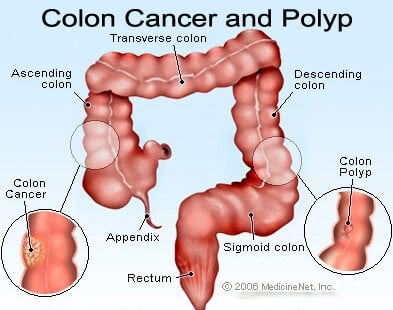 Obrázok polypov hrubého čreva a rakoviny hrubého čreva (kolorektálna).
Obrázok polypov hrubého čreva a rakoviny hrubého čreva (kolorektálna).
Nie všetky polypy hrubého čreva sú rovnaké. Existujú rôzne histologické typy, to znamená, že bunky, ktoré tvoria polyp, majú pri pohľade pod mikroskopom rôzne vlastnosti. Líšia sa tiež veľkosťou, počtom a umiestnením. Najdôležitejšie je, že majú rôznu tendenciu stať sa rakovinovými (malígnymi).
Najbežnejším typom polypu je adenóm alebo adenomatózny polyp. Je to dôležitý typ polypu nielen preto, že je najbežnejší, ale aj preto, že je najčastejšou príčinou rakoviny hrubého čreva. Pravdepodobnosť, že sa z adenómu vyvinie (alebo sa už rozvinul) do rakoviny, čiastočne závisí od jeho veľkosti; čím je polyp väčší, tým je pravdepodobnejšie, že polyp je alebo sa stane malígnym (obavy z malígneho potenciálu sa zvyšujú s polypom väčším ako jeden centimeter). Je tiež dôležité, či existuje jeden polyp alebo viac polypov. U pacientov s viacerými polypmi - aj keď nie sú malígne pri vyšetrení pod mikroskopom - je pravdepodobnejšie, že sa v budúcnosti vyvinú ďalšie polypy, ktoré sa môžu stať malígnymi. Obavy z tohto rastúceho malígneho potenciálu začínajú, keď sú tri alebo viac polypov. Nakoniec, malígny potenciál adenomatózneho polypu súvisí so spôsobom, akým sa bunky polypu organizujú, ako je vidieť pod mikroskopom. Bunky, ktoré sa organizujú do tubulárnych štruktúr (tubulárne adenómy), majú menšiu pravdepodobnosť, že sa stanú rakovinovými ako bunky, ktoré sa organizujú do štruktúr podobných prstom (klkovité adenómy).
Väčšina adenomatóznych polypov sa považuje za sporadickú, to znamená, že nepochádzajú z uznanej genetickej mutácie, ktorá je prítomná pri narodení (nie sú familiárne). Napriek tomu je riziko vzniku polypov hrubého čreva väčších ako jeden centimeter alebo vzniku rakoviny hrubého čreva dvojnásobne vyššie, ak má príbuzný prvého stupňa polypy hrubého čreva väčšie ako jeden centimeter. Preto je pravdepodobné, že genetický faktor funguje aj pri sporadických adenomatóznych polypoch.
Existuje niekoľko familiárnych, genetických stavov, pri ktorých sú mutácie alebo vývoj mutácií naprogramované do génov jedinca ešte pred narodením a odovzdávajú sa z rodiča na dieťa. Pri najbežnejšom z týchto stavov vznikajú stovky až tisíce adenomatóznych polypov (familiárna adenomatózna polypóza alebo FAP) v dôsledku mutácie v géne APC. Je dôležité rozpoznať tieto polypózne syndrómy a presnú genetickú abnormalitu, ktorá ich spôsobuje, ak je to možné, pretože malígny potenciál týchto polypov je oveľa väčší ako u jedincov bez genetickej abnormality. (U osemdesiatich percent alebo viac z týchto pacientov sa rozvinie rakovina hrubého čreva.) Aj keď sú tieto syndrómy zodpovedné len za niekoľko percent všetkých rakovín hrubého čreva, rozpoznanie syndrómu polypózy identifikuje pacientov, u ktorých je potrebné častejšie vykonávať skríning na ďalšie polypy. nové polypy a rakoviny môžu byť objavené a liečené včas. Môže sa dokonca odporučiť odstránenie celého hrubého čreva, aby sa predišlo rakovine. Okrem toho je možné vykonať genetické testovanie príbuzných pacienta, aby sa zistilo, či príbuzný má rovnakú mutáciu ako pacient, a preto je veľmi pravdepodobné, že sa u neho vyvinú polypy a rakovina. Príbuzní s rovnakou mutáciou sa potom môžu skrínovať na prítomnosť polypov a rakoviny, prednostne začať skríning kolorektálneho karcinómu v skoršom veku, než by sa normálne robilo, pretože rakoviny pri týchto syndrómoch sa vyvinú v skoršom veku ako rakoviny nesúvisiace so syndrómom. Kvôli autozomálne dominantnému spôsobu prenosu génu a jeho účinkom len jeden rodič potrebuje mať gén FAP, aby ho odovzdal svojim deťom, a preto existuje šanca 50/50, že každé z jeho detí bude mať FAP.
Existuje neobvyklá forma FAP, v ktorej je počet polypov menší ako klasický FAP - menej ako 100 - nazývaný oslabený FAP. Mutácia v géne APC v oslabenom FAP je iná ako mutácia v klasickom FAP. Pacienti s mnohými polypmi, ale nie s počtom pozorovaným pri FAP, by mali byť identifikovaní a testovaní na mutáciu. Na rozdiel od FAP, čo je autozomálne dominantný syndróm, oslabený FAP je recesívna mutácia, takže jedinec musí zdediť jeden mutovaný gén od každého rodiča, aby sa u neho vyvinuli polypy a rakovina hrubého čreva, a kvôli vzácnosti mutácie sa to vyskytuje zriedkavo.
Ďalším syndrómom polypov a rakoviny hrubého čreva je syndróm polypózy MYH. U jedincov s polypózou MYH sa v mladom veku vyvinie menej ako 100 polypov a sú vystavení vysokému riziku vzniku rakoviny hrubého čreva. Je to spôsobené mutáciami v inom géne ako je FAP, gén MYH; mutácia sa však vyskytuje sporadicky v dôsledku spontánnych mutácií, a preto dedičný vzor nie je zrejmý u rodičov, hoci ho možno pozorovať u súrodencov. Pretože ide o autozomálne recesívny gén, ktorý vyžaduje zmutovaný gén od každého rodiča, syndróm polypózy MYH je zriedkavý.
Druhým najbežnejším typom polypu hrubého čreva je hyperplastický polyp. Je dôležité rozpoznať tieto polypy a odlíšiť ich od adenomatóznych polypov, pretože majú malý alebo žiadny potenciál stať sa rakovinovými, pokiaľ nie sú lokalizované v proximálnom (vzostupnom hrubom čreve) alebo ak nevykazujú konkrétny histologický obraz pod mikroskopom (zúbkovaný vzhľad). . Napriek tomu existujú zriedkavé genetické syndrómy, pri ktorých sa u pacientov vytvára veľa hyperplastických polypov. Títo pacienti môžu byť vystavení podobnému riziku vzniku rakoviny hrubého čreva ako pacienti s viacerými adenomatóznymi polypmi, najmä ak sú polypy veľké, zúbkované, nachádzajú sa vo vzostupnom hrubom čreve a v rodinnej anamnéze sa vyskytuje rakovina hrubého čreva. Hyperplastické polypy môžu koexistovať s adenomatóznymi polypmi.
Existujú oveľa menej bežné typy polypov hrubého čreva a ich potenciál stať sa rakovinovým sa značne líši, napríklad hamartomatózne, juvenilné a zápalové polypy.
Nie, hoci väčšina rakoviny hrubého čreva vzniká z polypov, niektoré nie. Niektoré vznikajú v stene hrubého čreva. Tieto rakoviny môžu byť ploché alebo dokonca depresívne (vykopané). Je ťažšie ich identifikovať a liečiť a je pravdepodobnejšie, že sa rozšíria do steny hrubého čreva a blízkych lymfatických uzlín ako rakoviny pochádzajúce z polypov. To platí najmä pre zúbkované adenomatózne polypy, ktoré majú zvyčajne plochý a nie polypózny vzhľad.
Existuje tiež familiárny genetický syndróm nazývaný dedičný nepolypózny kolorektálny karcinóm (HNPCC, Lynchov syndróm), pri ktorom sa rakovina hrubého čreva vyskytuje s veľmi vysokou incidenciou (80 % alebo viac pacientov). U týchto pacientov je málo alebo žiadne polypy na identifikáciu. Okrem toho sa rakoviny vyskytujú v mladšom veku, často pred začiatkom skríningu rakoviny hrubého čreva a syndróm sa nerozpozná, kým sa u člena rodiny nevyvinie rakovina zvyčajne v mladom veku. HNPCC je podozrivý, pretože iní členovia rodiny majú tiež rakovinu hrubého čreva a sú splnené určité kritériá (kritériá Amsterdam alebo Bethesda), alebo rakovina vykazuje pod mikroskopom konkrétny vzor so špeciálnymi škvrnami. Ak je podozrenie na HNPCC, môže sa vykonať genetické testovanie rakoviny na identifikáciu dedičnej mutácie a ostatní členovia rodiny môžu byť testovaní na rovnakú mutáciu. Ak sú prítomní, členovia rodiny môžu podstúpiť skríningovú kolonoskopiu a následné kolonoskopie. HNPCC môže súvisieť aj s rakovinou v tkanivách mimo hrubého čreva. Našťastie je HNPCC zodpovedný len za niekoľko percent všetkých druhov rakoviny hrubého čreva.
Polypy hrubého čreva môžu mať rôznu veľkosť od niekoľkých milimetrov do niekoľkých centimetrov. Čím väčší je polyp, tým je pravdepodobnejšie, že v polype bude rakovina alebo že sa polyp neskôr stane rakovinovým.
Existuje niekoľko spôsobov, ako diagnostikovať polypy hrubého čreva.
Endoskopická kolonoskopia zahŕňa použitie kolonoskopu, ohybnej trubice s dĺžkou približne päť stôp so svetlom a kamerou na konci a dutým kanálom, cez ktorý môžu prechádzať nástroje. Kolonoskop prechádza cez konečník do hrubého čreva a potom cez hrubé črevo, kým sa nedosiahne proximálny koniec hrubého čreva - slepé črevo. Po vytiahnutí kolonoskopu sa pozoruje výstelka hrubého čreva na polypy a iné abnormality. Tieto môžu byť biopsiou alebo odstránené pomocou elektrokauterizácie a potom vyšetrené pod mikroskopom. Kolonoskopia identifikuje 95 % polypov, malých aj veľkých, aj keď niekedy polypy vynechajú, ak sú malé, skryté záhybmi vo výstelke hrubého čreva, ploché alebo je kolonoskopia uponáhľaná.
Virtuálna kolonoskopia zahŕňa použitie buď počítačovej tomografie (CT) alebo zobrazovania magnetickou rezonanciou (MRI). Hrubé črevo sa naplní buď tekutou kontrastnou látkou alebo vzduchom a vykoná sa CT alebo MRI. Počítačová rekonštrukcia snímok CT alebo MRI poskytuje virtuálny obraz, ktorý napodobňuje pohľad získaný kolonoskopom. Virtuálna kolonoskopia je veľmi dobrá pri hľadaní polypov, ale nie taká dobrá ako kolonoskopia; môže vynechať polypy menšie ako jeden centimeter, hoci o potrebe identifikácie týchto menších polypov sa diskutuje, pretože len zriedka sú malígne. MRI má oproti CT výhodu, pretože pacienta nevystavuje žiareniu. Je to však drahšie a s MRI je menej skúseností ako s CT. Problém virtuálnej kolonoskopie CT aj MRI spočíva v tom, že ak sa nájde polyp, ktorý by sa mal odstrániť, kolonoskopia sa musí urobiť neskôr, aby sa odstránil.
Báriový klystír je staršou metódou diagnostiky polypov hrubého čreva. Počas báryovej klyzmy sa hrubé črevo naplní báryom a pri zmene polohy pacienta sa zhotovia viaceré röntgenové snímky hrubého čreva. Báriový klystír je dobrý spôsob diagnostiky polypov a je relatívne lacný; môže však ľahko minúť malé polypy a vystavuje pacientov žiareniu. Navyše, zručnosti a skúsenosti potrebné na správne vykonanie báryovej klystíry medzi rádiológmi klesli, pretože báryové klystíry sa teraz, keď je k dispozícii kolonoskopia a virtuálna kolonoskopia, objednávajú menej často. Nakoniec, podobne ako pri virtuálnej kolonoskopii, ak sa nájdu polypy, musí sa urobiť kolonoskopia na odstránenie polypu.
Flexibilná sigmoidoskopia používa skrátenú verziu kolonoskopu s dĺžkou približne tri stopy. Dokáže vyšetriť iba distálnu tretinu až polovicu hrubého čreva. Rovnako ako kolonoskop sa môže použiť na identifikáciu, biopsiu a odstránenie polypov bez vystavenia žiareniu. Na účely skríningu, keďže sigmoidoskop nedokáže vyšetriť celé hrubé črevo, sa zvyčajne kombinuje s menej častou kolonoskopiou alebo častými testami na okultnú krv v stolici na identifikáciu polypov mimo jeho dosahu.
Niekoľko expertných skupín vydalo odporúčania na sledovanie u jedincov, u ktorých sa zistilo, že majú polypy pri ich počiatočnom vyšetrení, ktorým je zvyčajne endoskopická kolonoskopia, ale občas virtuálna kolonoskopia alebo flexibilná sigmoidoskopia. Odporúčania sa mierne líšia od skupiny ku skupine, ale nie v dôležitých smeroch. Všetci vydávajú odporúčania na základe faktorov, ako je rodinná anamnéza polypov a rakoviny hrubého čreva, počet nájdených polypov, veľkosť polypov a histológia polypov. Použitím týchto faktorov môže byť interval medzi monitorovacími postupmi prispôsobený riziku vzniku ďalších polypov a malignity v budúcnosti – čím vyššie je riziko, tým kratší je interval medzi monitorovacími postupmi. Nasledujúce odporúčania sú upravené z usmernení navrhnutých americkou Multi-Society Task Force on Colorectal Cancer publikovaných v roku 2012.
Adenómy možno klasifikovať ako nízke riziko (LRA) a vysoké riziko (HRA) rakoviny.
LRA je definovaná ako jeden až dva tubulárne adenómy menšie ako jeden centimeter.
HRA je definovaná ako tri alebo viac adenómov, s jedným tubulárnym adenómom väčším ako jeden centimeter, alebo adenóm s histológiou klkov alebo dyspláziou vysokého stupňa.
Odporúčania týkajúce sa toho, kedy absolvovať tretie a ďalšie vyšetrenie, závisia od prítomnosti LRA alebo HRA pri prvom a druhom vyšetrení a môžu sa líšiť od troch do 10 rokov.
Väčšinu polypov je možné odstrániť endoskopom. Potom sa skúmajú pod mikroskopom. Je dôležité určiť, či obsahujú alebo neobsahujú rakovinu, či sú typu, ktorý má malígny potenciál, a či majú vlastnosti, ktoré zvyšujú pravdepodobnosť ich spojenia s rakovinou, buď v inom polype v rovnakom čase, alebo v polypoch. ktoré sa môžu v budúcnosti vytvoriť (napríklad sú vilózne alebo zúbkované).
Výsledky kolonoskopie a histologického vyšetrenia sú dôležité, pretože určujú potrebu zvýšenej frekvencie skríningovej kolonoskopie v budúcnosti (napríklad adenomatózne polypy). Ak je už v polype prítomná rakovina, je dôležité určiť, ako hlboko do steny hrubého čreva sa rakovina rozšírila. Ak sa rozšíri hlboko, je pravdepodobnejšie, že sa rakovina rozšírila do vzdialenejších lymfatických uzlín. Ak dôjde k hlbokému rozšíreniu rakoviny, môže byť potrebné vykonať dodatočnú endoskopickú resekciu oblasti hrubého čreva, kde bol polyp, alebo chirurgicky odstrániť časť hrubého čreva, aby ste si boli istí, že celá rakovina bola odstránená. Neďaleké lymfatické uzliny môžu byť tiež odstránené a vyšetrené, aby sa identifikovalo akékoľvek rozšírenie rakoviny mimo hrubého čreva.
Ak je podozrenie na genetickú mutáciu, hľadá sa genetickým testovaním časti biopsie a ak je prítomná, príbuzní by mali byť vyšetrení na rovnakú mutáciu. Ak sú prítomní, príbuzní by mali podstúpiť skríningovú kolonoskopiu a častejšiu dohľadovú kolonoskopiu.
Odporúča sa, aby pacienti s FAP a inými polypovými syndrómami zvážili profylaktické odstránenie hrubého čreva, aby sa zabránilo vzniku rakoviny.
Genetika a genetické testovanie sa stali dôležitým aspektom pri hodnotení polypov hrubého čreva a rakoviny hrubého čreva.
Každý pacient s polypom hrubého čreva by mal mať starostlivú rodinnú anamnézu. Ak je to potrebné, jednotlivci alebo rodiny môžu byť odkázaní na lekárov, ktorí sa špecializujú na genetiku chorôb, ktorí môžu pomôcť pri rozhodovaní o genetickom testovaní a skríningu. Toto je obzvlášť dôležité u pacientov s mnohopočetnými polypmi, niekoľkých členov rodiny s polypmi alebo rakovinou hrubého čreva alebo člena rodiny so skorým nástupom rakoviny hrubého čreva (vo veku pred 50 rokmi).
Rodinná anamnéza polypov hrubého čreva a rakoviny hrubého čreva je dôležitým kľúčom k možnej prítomnosti familiárneho genetického syndrómu. Ak existuje podozrenie na syndróm, jednotlivci môžu byť testovaní na známe mutácie a môžu začať s kolonoskopiou s pozorovaním v skoršom veku; stále však existujú syndrómy, pre ktoré nie sú mutácie známe a na ktoré nie je možné testovať. Napriek tomu aj v týchto rodinách existuje výhoda; rodinní príslušníci sú upozornení na možnosť neidentifikovateľného syndrómu a môžu začať s kolonoskopiou včas. Pacienti s FAP majú často iné polypy s malígnym potenciálom v gastrointestinálnom trakte a vyvíjajú sa u nich polypy a/alebo rakoviny v iných gastrointestinálnych a negastrointestinálnych tkanivách. Vyžadujú si ďalší skríning, aby sa zistilo, či polypy bez hrubého čreva majú malígny potenciál a či sa rakovina vyvinula mimo gastrointestinálneho traktu.
Genetika sa dá využiť aj inak. V rodinách s FAP alebo HNPCC, ak sa genetická abnormalita identifikuje u pôvodného člena rodiny s polypmi alebo rakovinou, môžu byť s rovnakou abnormalitou identifikovaní aj ďalší členovia rodiny, ktorí potom môžu začať včasné vyšetrenie rakoviny hrubého čreva.
Kvôli obavám týkajúcim sa prechodu polypov na rakovinu sa uskutočnili pokusy určiť, či liečba s teoretickým potenciálom skutočne zabraňuje vzniku polypov. Problém väčšiny štúdií je, že ide o retrospektívne, pozorovacie štúdie, ktoré ako dôkaz nestačia. Dlhé časové obdobie (mnoho rokov), ktoré je potrebné na vytvorenie polypov, si vyžaduje dlhodobé štúdie, ale takéto štúdie bolo ťažké vykonať, s výnimkou prípadov familiárnych, genetických polypóznych syndrómov a kvôli rozdielom v ich príčin, nie je jasné, či to, čo sa na ne vzťahuje, platí aj pre bežnejšie sporadické adenómy.
Pre antioxidanty vrátane selénu, beta karoténu a vitamínov A, C a E sa skúmalo niekoľko súvislostí. Väčšina vykonaných štúdií nepodporuje úlohu týchto látok pri prevencii polypov alebo pri prevencii rakoviny hrubého čreva. Pre použitie selénu na prevenciu polypov je k dispozícii obmedzené množstvo podpory, ale selén sa neodporúča používať mimo experimentálnych skúšok.
V jednej štúdii sa preukázalo, že doplnkový vápnik z potravy zabraňuje tvorbe polypov. Prínos bol pozorovaný pri suplementácii 1200 mg vápnika denne. Existujú určité obavy z používania vápnika, pretože vyššie hladiny v potrave a doplnkov sú spojené s nárastom vaskulárnych ochorení. Príjem vápnika, ktorý sa skúmal, bol vyšší ako odporúčaný príjem vápnika, 800 mg denne.
Najlepšou podporou liečby na prevenciu polypov sú nesteroidné protizápalové lieky (NSAID), trieda liekov, ktorá zahŕňa aspirín, ibuprofén (Motrin, Advil), celekoxib (Celebrex) a mnoho ďalších. V niekoľkých štúdiách sa preukázalo, že aspirín znižuje tvorbu polypov o 30 % až 50 %. Účinok sa pravdepodobne dostaví pri vyšších dávkach aspirínu (viac ako 81 – 325 mg, ktoré sa odporúčajú na prevenciu kardiovaskulárnych chorôb) a existuje obava z vedľajšieho účinku aspirínu, ktorým je gastrointestinálne krvácanie pri týchto dávkach.
Ukázalo sa, že celekoxib (Celebrex), „COX-2 selektívny NSAID“ alebo inhibítor Cox-2, znižuje aj polypy hrubého čreva o 30 % až 50 %, ale pretrvávajú obavy z možných kardiovaskulárnych vedľajších účinkov, ktoré možno pozorovať pri väčšina NSAID (hoci údaje podporujúce tento vedľajší účinok sú protichodné). Môže sa použiť u pacientov so syndrómom genetickej polypózy, ktorí sa rozhodnú nenechať si odstrániť hrubé črevo. U pacientov s nízkym rizikom kardiovaskulárneho ochorenia, u ktorých sa často vyvíjajú adenomatózne polypy, možno zvážiť celecoxib.
Ukázalo sa, že Sulindac (Clinoril), "neselektívne NSAID", zabraňuje vzniku polypov u pacientov so sporadickým adenómom, ako aj genetickým syndrómom. Rovnako ako v prípade celekoxibu existujú obavy z kardiovaskulárnych vedľajších účinkov a gastrointestinálnej ulcerácie a krvácania.
Vzhľadom na dostupné informácie sa neodporúča, aby sa pacienti s priemerným rizikom tvorby ďalších polypov liečili na prevenciu, pretože sa obáva, že riziká liečby, predovšetkým črevné krvácanie a kardiovaskulárne ochorenie, môžu prevážiť prínos prevencie polypov. Môže byť rozumné liečiť pacientov, ktorí majú vyššie ako priemerné riziko polypov, u ktorých môže prínos prevážiť riziká. Medzi takýchto pacientov môžu patriť pacienti s častou tvorbou polypov, najmä tí, ktorí preukázali rakovinové zmeny v polypoch, alebo pacienti, ktorí už mali rakovinu hrubého čreva. Štúdie na týchto typoch pacientov sú netrpezlivo očakávané.
 Angioplastika môže byť riziková pre tých, ktorí majú slabú cirkuláciu nôh
Angioplastika môže byť riziková pre tých, ktorí majú slabú cirkuláciu nôh
 Nová štúdia by mohla pomôcť predchádzať smrteľným infekciám u detí
Nová štúdia by mohla pomôcť predchádzať smrteľným infekciám u detí
 Používanie CT vyšetrenia u detí za posledné desaťročie kleslo
Používanie CT vyšetrenia u detí za posledné desaťročie kleslo
 Ľudia preberajú infekciu zo šteniatok v obchode so zvieratami:CDC
Ľudia preberajú infekciu zo šteniatok v obchode so zvieratami:CDC
 Ako správne pripraviť fazuľu (aby bola zdravá pre črevá)
Ako správne pripraviť fazuľu (aby bola zdravá pre črevá)
 Stres a trávenie – 3 tipy na zvládanie stresu na zlepšenie trávenia
Stres a trávenie – 3 tipy na zvládanie stresu na zlepšenie trávenia
 Veda o ohnivom jablčnom mušte a oxymeloch na zlepšenie zdravia
„Fire Cider je ako Veľký medveď v chladnej zimnej noci – Veľký medveď, ktorý žmolí, čo ťa trápi!“ – Byliny mesta Shire Bolo tesne po Vianociach... a ja som sa začal cítiť mimo. Viete, ako to začína
Veda o ohnivom jablčnom mušte a oxymeloch na zlepšenie zdravia
„Fire Cider je ako Veľký medveď v chladnej zimnej noci – Veľký medveď, ktorý žmolí, čo ťa trápi!“ – Byliny mesta Shire Bolo tesne po Vianociach... a ja som sa začal cítiť mimo. Viete, ako to začína
 Recept na jednoduchú domácu horkú čokoládu
Zdravá liečba je vážna vec. Hovorím o niečom, čo si môžete užiť, čo vás na vašej ceste uzdravenia nestiahne o 3 dni (alebo viac). Mohlo byť rozdiel medzi zostať na správnej ceste alebo úplne spadnúť
Recept na jednoduchú domácu horkú čokoládu
Zdravá liečba je vážna vec. Hovorím o niečom, čo si môžete užiť, čo vás na vašej ceste uzdravenia nestiahne o 3 dni (alebo viac). Mohlo byť rozdiel medzi zostať na správnej ceste alebo úplne spadnúť
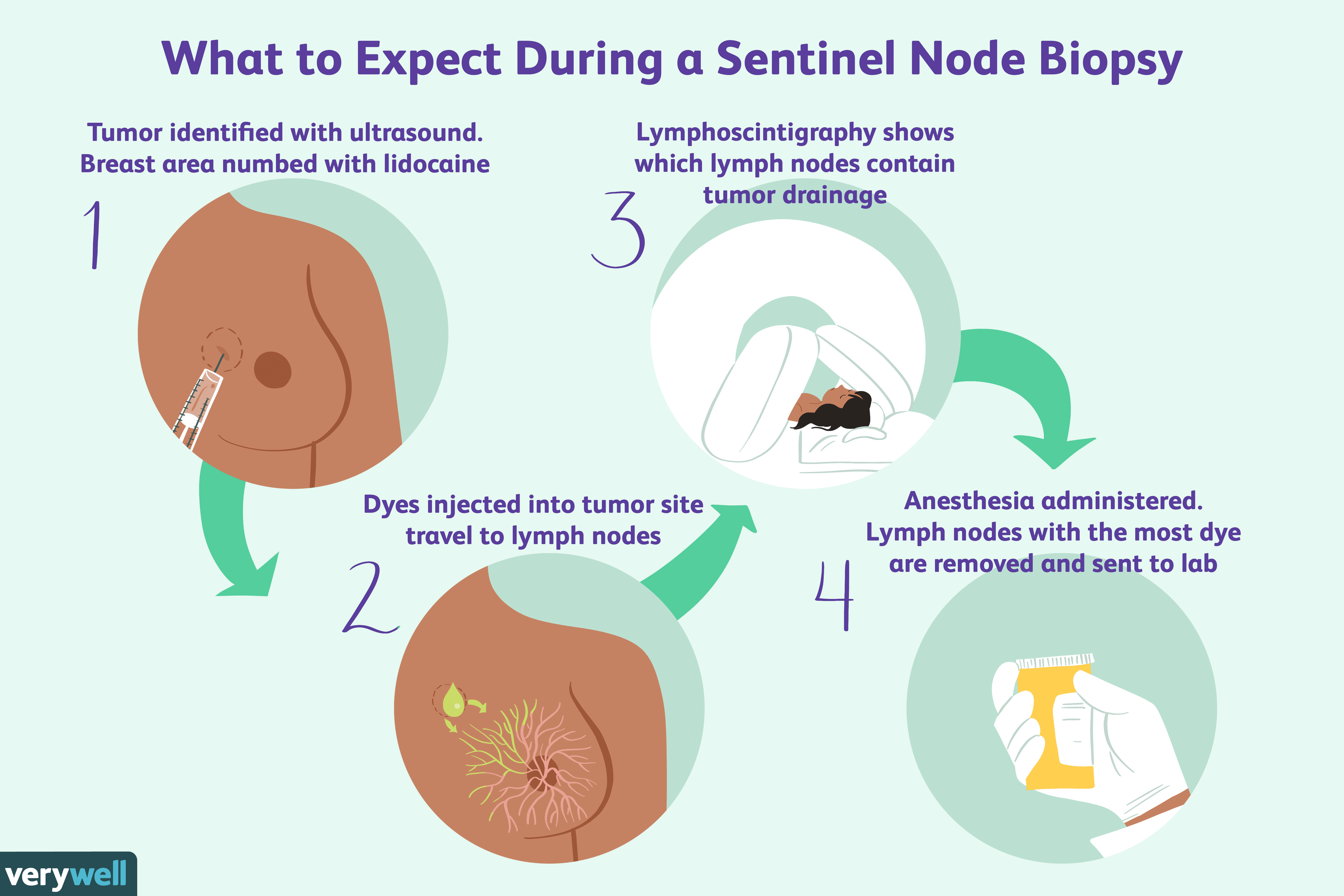 Prehľad rakoviny prsníka s pozitívnymi lymfatickými uzlinami
Testovanie lymfatických uzlín je jedným z predpovedí prognózy rakoviny prsníka. Pozitívna rakovina prsníka na lymfatické uzliny je typ rakoviny, ktorá sa rozšírila z pôvodného nádoru do najbližších ly
Prehľad rakoviny prsníka s pozitívnymi lymfatickými uzlinami
Testovanie lymfatických uzlín je jedným z predpovedí prognózy rakoviny prsníka. Pozitívna rakovina prsníka na lymfatické uzliny je typ rakoviny, ktorá sa rozšírila z pôvodného nádoru do najbližších ly