Les compléments alimentaires, également appelés compléments alimentaires, comprennent les produits à base de plantes, les vitamines, les minéraux et tout produit qui n'est pas commercialisé comme aliment ou médicament (médicament). Les gens prennent des compléments alimentaires dans l'idée de maintenir ou d'améliorer leur santé. Récemment, cependant, mes collègues et moi avons rapporté dans un journal médical une série de sept patients qui nous ont été référés avec une atteinte hépatique grave. Ils ont développé des dommages au foie après avoir pris un supplément de santé appelé Lipokinetix® pour perdre du poids. Ce supplément est un mélange de produits chimiques qui comprend un extrait d'un thé particulier. On dit qu'il réduit le poids en travaillant pour imiter l'exercice et augmenter le métabolisme.
Comment et pourquoi les compléments alimentaires peuvent-ils endommager le foie ? Dans les trois mois suivant le début de Lipokinetix, ces sept patients ont développé des symptômes d'hépatite aiguë, notamment de la fatigue, une perte d'appétit et des douleurs abdominales. Ils ont consulté un médecin et leurs tests sanguins ont révélé de graves dommages au foie. L'une des patientes a en fait développé une insuffisance hépatique aiguë (rapide) et a presque eu besoin d'une greffe de foie pour lui sauver la vie. Après avoir été dans le coma pendant trois jours, elle a miraculeusement récupéré et a pu quitter l'hôpital. En effet, chez les sept patients, les symptômes ont disparu et les tests hépatiques sont revenus à la normale quelques mois après l'arrêt de Lipokinetix. Cela dit, j'ai depuis été informé d'une autre personne qui a pris ce même supplément, a développé une insuffisance hépatique aiguë et a eu besoin d'une greffe de foie. Elle va bien maintenant. Cependant, afin que son corps puisse continuer à accepter le nouveau foie (étranger), elle prendra de puissants médicaments anti-rejet pour le reste de sa vie.
Mais ce n'est pas tout! De nombreux cas ont été rapportés dans la littérature médicale de compléments alimentaires, en particulier de produits à base de plantes, causant des dommages au foie. Ces suppléments comprennent le kava (qui a reçu une couverture récente dans la presse), le Jin Bu Huan, la germandrée, le chaparral, le cartilage de requin et le gui, pour n'en nommer que quelques-uns. Les compléments alimentaires peuvent causer des lésions hépatiques de différentes manières. Dans certains cas, par exemple avec le kava, les lésions hépatiques sont liées à la dose. Autrement dit, plus la dose est élevée, plus les lésions hépatiques sont fréquentes. Dans de nombreux cas, cependant, les lésions hépatiques sont une particularité imprévisible chez un individu (une réaction idiosyncrasique).
Il est bien connu que les gens prennent souvent des combinaisons de suppléments à base de plantes et/ou d'autres aliments. Dans cette circonstance, si une personne développe une atteinte hépatique grave, il est très difficile d'identifier quel supplément est le coupable spécifique. avant été jugé. Un exemple typique est le Lipokinetix mentionné ci-dessus, qui contient parmi ses ingrédients un stimulant de type anéphédrine, un type d'hormone thyroïdienne et l'extrait de thé.
Le principal problème est que la Food and Drug Administration (FDA) ne réglemente pas le processus de fabrication des compléments alimentaires, comme elle le fait pour les médicaments conventionnels. Vous voyez, la FDA ne peut pas considérer un complément alimentaire comme un aliment ou un médicament. Ainsi, la pureté des compléments alimentaires est déterminée et communiquée au public uniquement par le fabricant. De plus, le dosage de ces suppléments est déterminé par le fabricant et est souvent sans support scientifique ni données publiées dans des revues scientifiques à comité de lecture. De plus, la FDA n'exige aucun test animal ou clinique de pré-commercialisation des compléments alimentaires, comme c'est le cas pour les médicaments conventionnels. De plus, les médecins ne signalent les événements indésirables que volontairement lorsqu'ils les rencontrent.
Par conséquent, tant que le fabricant ne fait pas d'affirmation scandaleuse sur son produit et ne le commercialise pas comme un aliment ou un médicament, ces suppléments se retrouvent sur les étagères des magasins sans trop, voire aucun, examen par la FDA. Il s'avère que la désignation d'un produit de santé comme complément alimentaire est une échappatoire créée par la loi de 1994 sur les compléments alimentaires, la santé et l'éducation. (Le terme "complément alimentaire" implique un ajout au régime de quelque chose qui est déjà présent dans les aliments que nous mangeons.) Cette échappatoire permet aux producteurs de compléments alimentaires d'éviter la réglementation de la FDA sur la fabrication de ces produits. Eh bien, cette situation concernant la réglementation plutôt lâche des compléments alimentaires me rend nerveux. Je suis inquiet, surtout si l'on considère que les médicaments conventionnels (médicaments) sont soumis à un processus d'examen assez rigoureux.
Quel est le processus d'examen des médicaments conventionnels? Pour qu'un médicament soit mis sur le marché aux États-Unis, il doit passer par de nombreuses étapes, y compris des tests approfondis sur des animaux et trois phases de tests cliniques sur des humains. Dans la première phase, le médicament est administré à des sujets sains pour déterminer les effets indésirables potentiels (toxicité). Ce faisant, différentes doses du médicament sont testées pour s'assurer que même une dose plusieurs fois supérieure à la dose prévue est sans danger pour l'homme.
Dans la deuxième phase, le médicament est administré aux patients qui ont réellement la condition que le médicament est destiné à traiter. Cette phase implique généralement jusqu'à cinquante à cent patients. Encore une fois, plusieurs doses différentes sont essayées pour déterminer l'efficacité et la toxicité des différentes doses. L'objectif est de trouver la dose qui atteint une efficacité maximale avec des effets secondaires minimes (tolérables) (toxicité).
La troisième phase implique généralement un essai contrôlé randomisé (ECR). Dans un ECR, chacun des deux groupes de plusieurs centaines de patients atteints de la condition spécifique est assigné au hasard pour recevoir l'un des deux traitements. L'un des traitements est le médicament qui est évalué et l'autre (le traitement de contrôle) est soit un placebo (une pilule de sucre inactive), soit le traitement standard (efficace) pour la condition spécifique. Les ECR sont généralement réalisés en double aveugle (masqué). Cela signifie que ni les patients ni les médecins qui les soignent et les évaluent ne savent quels traitements les patients individuels reçoivent jusqu'à ce que l'étude soit terminée. Un comité de surveillance de l'innocuité des médicaments composé d'experts indépendants qui ne sont pas liés au fabricant et aux chercheurs est généralement nommé pour superviser l'étude.
La FDA examine également les données recueillies à chaque phase pour assurer la sécurité avant d'approuver la prochaine phase de test. Puis, à la fin de la phase trois, toutes les données cliniques sur le médicament sont soumises à la FDA pour examen. De plus, avant que le médicament ne puisse être approuvé, la FDA fait appel à un groupe indépendant d'experts pour examiner toutes les données et tous les documents. Enfin, une fois que le médicament a reçu l'approbation de la FDA et qu'il peut être prescrit, les médecins sont tenus de signaler tout cas d'effets indésirables possibles au programme MedWatch parrainé par la FDA. Ce dernier type de surveillance est appelé surveillance post-marketing.
Ironiquement, les consommateurs, les médecins et l'industrie pharmaceutique ont parfois critiqué ce processus d'évaluation rigoureux des médicaments. Ces critiques affirment que le processus entraîne des retards inutiles dans la publication de remèdes potentiellement vitaux. J'estime cependant que ces procédures sont nécessaires pour protéger la santé du public. En effet, malgré ce processus exigeant, nous entendons encore parfois parler de terribles réactions indésirables à des médicaments qui ont déjà été approuvés par la FDA. Le médicament contre le diabète, la troglitazone (Rezulin), vient à l'esprit.
La troglitazone était considérée comme un nouveau médicament pour le traitement du diabète de l'adulte. Ce n'est qu'après que le médicament a reçu l'approbation de la FDA et qu'il a été largement utilisé qu'il est devenu évident que la troglitazone pouvait causer des lésions hépatiques graves et la mort. (Cette histoire tragique a en fait été révélée grâce à la persistance d'un journaliste d'investigation du LA Times.) Le médicament a depuis été retiré du marché, mais cela nous rappelle que nous devons être vigilants lorsque nous prenons des médicaments ou des suppléments.
Retour sur les compléments alimentaires diététiques. D'autres recherches, y compris des études cliniques, sont nécessaires sur l'efficacité et la sécurité des compléments alimentaires. En fait, je ne suis pas au courant de données publiées dans des revues médicales évaluées par des pairs d'études de phase 1 ou de phase 2 sur ces suppléments. Je ne connais pas non plus d'essais contrôlés randomisés qui ont été menés sur des compléments alimentaires pour montrer leur innocuité, sans parler de leur efficacité.
D'un autre côté, il est important de reconnaître que peu de fabricants de suppléments de santé ont les ressources (l'argent) pour mener des ECR valides car ces essais sont extrêmement coûteux à réaliser. De plus, à l'heure actuelle, aucun financement fédéral n'est disponible pour la FDA pour étudier et surveiller activement les événements indésirables associés à ces suppléments. Néanmoins, une plus grande réglementation des compléments alimentaires est nécessaire et devrait être instituée. À cet égard, une commission de la Maison Blanche sur la médecine complémentaire et alternative (CAM) a récemment publié son rapport quelque peu controversé après deux ans d'étude. La bonne nouvelle est que le rapport a appelé à davantage de financement pour des recherches scientifiques valables sur les avantages et les dangers des MCA, y compris les compléments alimentaires.
Enfin, je voudrais mettre en garde nos lecteurs. Un médicament est un médicament, qu'il s'agisse d'un médicament ou d'un complément alimentaire. De plus, tout médicament peut interagir avec un autre médicament et entraîner un événement indésirable grave. Par exemple, le ginkgo biloba, qui est un produit à base de plantes censé améliorer la mémoire, peut réagir avec l'ibuprofène (Motrin) pour provoquer une grave hémorragie interne. Ne vous fiez pas à ce qui est dit dans une publicité sur un médicament ou un complément alimentaire. Au lieu de cela, regardez d'un œil critique les données sur le produit. Lorsque vous consultez votre médecin, informez-le de tous les médicaments que vous prenez, y compris les suppléments. Dans votre intérêt, ils devraient le savoir. En fait, j'ai appris à demander, pas seulement une fois, mais plusieurs fois, si mes patients prenaient des compléments alimentaires, en particulier des produits à base de plantes. Si vous ne vous sentez pas bien, arrêtez immédiatement le supplément et consultez un médecin. Ne cachez pas d'informations à votre médecin concernant vos suppléments.
 Plus d'actualités sur la santé »
Plus d'actualités sur la santé » Comment traiter le prolapsus rectal chez les enfants ?
Comment traiter le prolapsus rectal chez les enfants ?
 Une étude met en lumière les causes des douleurs intestinales débilitantes
Une étude met en lumière les causes des douleurs intestinales débilitantes
 l'australie tombe amoureuse des recettes sibo-friendly !
l'australie tombe amoureuse des recettes sibo-friendly !
 Les oxyures (Enterobiasis) chez les enfants et les adultes
Les oxyures (Enterobiasis) chez les enfants et les adultes
 Qu'y a-t-il dans le suc gastrique de votre estomac ?
Qu'y a-t-il dans le suc gastrique de votre estomac ?
 La respiration d'hydrogène ne vient pas de l'atoll de Bikini
La respiration d'hydrogène ne vient pas de l'atoll de Bikini
 Quels sont les signes avant-coureurs de la maladie de Crohn ?
La maladie de Crohn peut provoquer ces signes et symptômes ; cependant, seul un médecin peut vous diagnostiquer correctement. La maladie de Crohn est une maladie inflammatoire de lintestin (MICI) q
Quels sont les signes avant-coureurs de la maladie de Crohn ?
La maladie de Crohn peut provoquer ces signes et symptômes ; cependant, seul un médecin peut vous diagnostiquer correctement. La maladie de Crohn est une maladie inflammatoire de lintestin (MICI) q
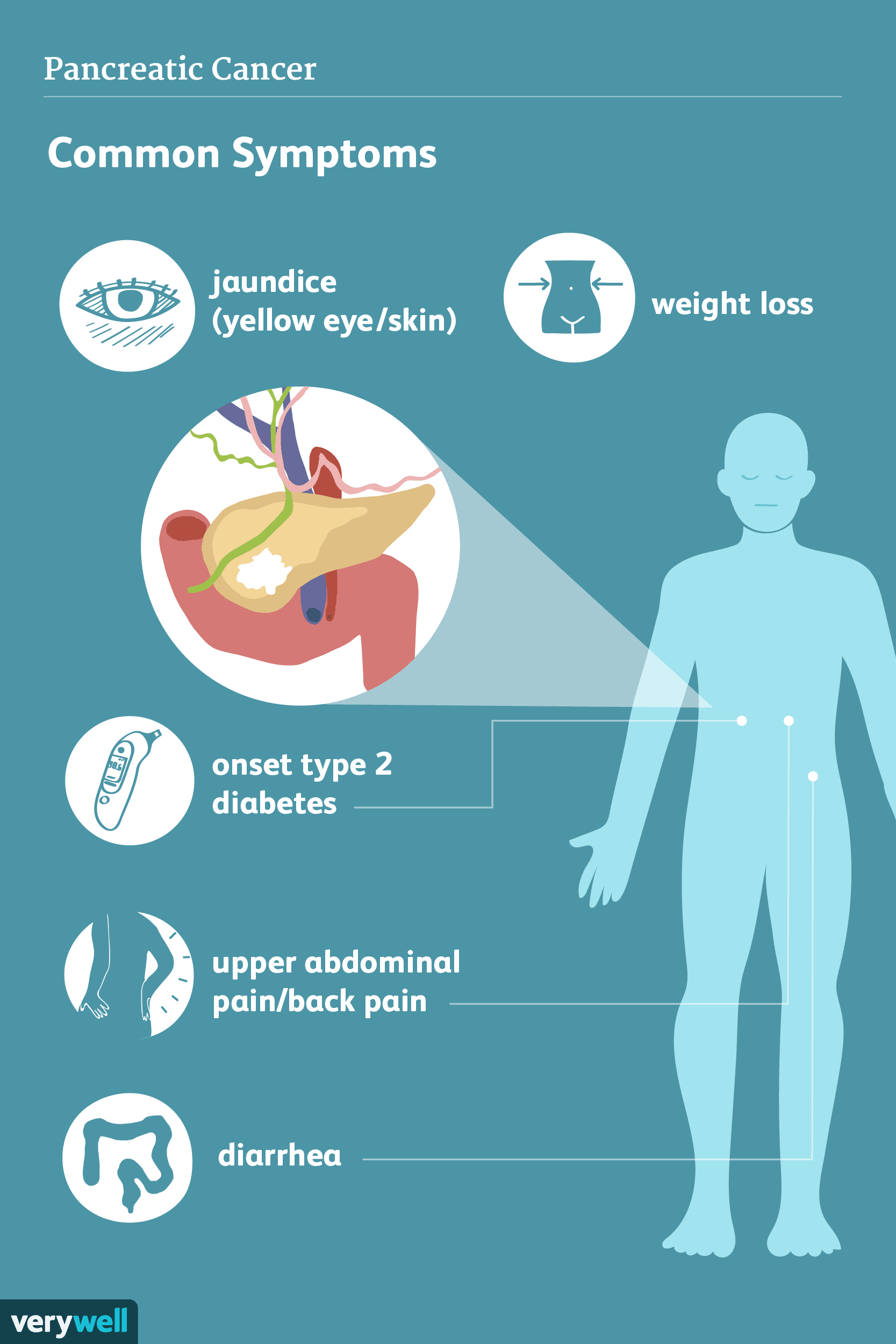 Symptômes du cancer du pancréas
Les symptômes du cancer du pancréas peuvent inclure la jaunisse, des douleurs dans la partie supérieure de labdomen qui irradient dans le dos, lapparition inattendue de diabète, une masse dure dans la
Symptômes du cancer du pancréas
Les symptômes du cancer du pancréas peuvent inclure la jaunisse, des douleurs dans la partie supérieure de labdomen qui irradient dans le dos, lapparition inattendue de diabète, une masse dure dans la
 Comment garder votre intestin en bonne santé pendant les fêtes
Cette semaine, sur #AskADietitian Facebook Live, nous arrivons à parler de la façon de garder votre intestin en bonne santé et heureux pendant les vacances ! Je passe en revue mes 5 conseils pour rédu
Comment garder votre intestin en bonne santé pendant les fêtes
Cette semaine, sur #AskADietitian Facebook Live, nous arrivons à parler de la façon de garder votre intestin en bonne santé et heureux pendant les vacances ! Je passe en revue mes 5 conseils pour rédu