ПЯТНИЦА, 3 августа (HealthDay News). Залтрап (зив-афилберцепт) был одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США в сочетании со схемой химиотерапии FOLFIRI для взрослых с распространенным метастатическим (распространяющимся) колоректальным раком, сообщило агентство в пятницу.
FOLFIRI означает схему, включающую фолиновую кислоту, фторурацил и иринотекан. Zaltrap, относящийся к классу препаратов, называемых ингибиторами ангиогенеза, ограничивает рост опухолей, препятствуя их кровоснабжению. Препарат был одобрен для людей, у которых опухоли устойчивы к химиотерапии на основе оксалиплатина или прогрессировали после химиотерапии на основе оксалиплатина, говорится в пресс-релизе FDA.
Агентство сообщило, что колоректальный рак, 4-я по значимости причина рака и смертности от рака в Соединенных Штатах, будет диагностирован примерно у 143 460 американцев в этом году, и около 51 690 человек умрут от него.
По данным FDA, в клинических испытаниях люди, получавшие комбинацию Zaltrap-FOLFIRI, жили в среднем 13,5 месяцев по сравнению с 12 месяцами при комбинации FOLFIRI и плацебо.
Наиболее распространенные побочные эффекты комбинации Zaltrap-FOLFIRI включали снижение лейкоцитов, диарею, язвы во рту, утомляемость, высокое кровяное давление, потерю веса, потерю аппетита, боль в животе и головную боль.
Zaltrap производится компанией Sanofi-Aventis, базирующейся в Бриджуотере, штат Нью-Джерси.
-- Скотт Робертс
 Авторские права © HealthDay, 2012. Все права защищены.
Авторские права © HealthDay, 2012. Все права защищены.
 Безглютеновая мода на здоровье стоимостью 12 миллиардов долларов
Когда в 2007 году мне поставили диагноз целиакия, я понятия не имел, что такое безглютеновая пища. Я никогда не слышал о нем раньше и совершенно не знал, где его купить. Но в то время продажи продукт
Безглютеновая мода на здоровье стоимостью 12 миллиардов долларов
Когда в 2007 году мне поставили диагноз целиакия, я понятия не имел, что такое безглютеновая пища. Я никогда не слышал о нем раньше и совершенно не знал, где его купить. Но в то время продажи продукт
 Эти хронические тенденции в области здоровья поразят вас (но есть надежда)
По оценкам Центра по контролю за заболеваниями США, к 2020 году 157 МИЛЛИОНОВ американцев будут страдать хроническими заболеваниями. Насколько я могу судить по данным, в это число не входят даже те и
Эти хронические тенденции в области здоровья поразят вас (но есть надежда)
По оценкам Центра по контролю за заболеваниями США, к 2020 году 157 МИЛЛИОНОВ американцев будут страдать хроническими заболеваниями. Насколько я могу судить по данным, в это число не входят даже те и
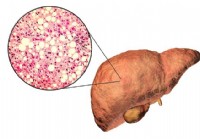 Как долго вы живете с НАЖБП? Показатели выживаемости
Большинство людей живут долго с неалкогольной жировой болезнью печени (НАЖБП). Однако НАЖБП может сократить ожидаемую продолжительность жизни примерно на 4,2–4,4 года. Большинство людей живут долго с
Как долго вы живете с НАЖБП? Показатели выживаемости
Большинство людей живут долго с неалкогольной жировой болезнью печени (НАЖБП). Однако НАЖБП может сократить ожидаемую продолжительность жизни примерно на 4,2–4,4 года. Большинство людей живут долго с