LUNES, 26 de enero de 2015 (HealthDay News) -- La Administración de Alimentos y Medicamentos (FDA) de EE. UU. aprobó la primera versión genérica del medicamento para la acidez estomacal Nexium (esomeprazol).
El medicamento ayuda a tratar la ERGE, que significa enfermedad por reflujo gastroesofágico. La ERGE ocurre cuando el ácido del estómago regresa al esófago y se conoce comúnmente como acidez estomacal crónica o reflujo ácido.
La licencia para producir esomeprazol genérico en cápsulas de 20 miligramos y 40 miligramos se otorgó a Ivax Pharmaceuticals, una subsidiaria de la firma israelí Teva Pharmaceuticals, dijo la FDA en un comunicado de prensa.
El esomeprazol también está aprobado para reducir la probabilidad de úlceras gástricas asociadas con una clase de analgésicos conocidos como medicamentos antiinflamatorios no esteroideos (AINE), dijo la agencia. Y está aprobado para tratar una infección estomacal con H. pylori, que se ha relacionado con las úlceras.
Una guía de medicamentos distribuida con el fármaco advierte sobre posibles problemas que incluyen diarrea severa y, con el uso prolongado, un mayor potencial de fracturas óseas, dijo la FDA.
Los efectos secundarios más comunes de esomeprazol incluyen dolor de cabeza, diarrea, náuseas, flatulencia, dolor abdominal, fatiga, estreñimiento y boca seca.
La FDA enfatizó que los medicamentos genéricos aprobados tienen la misma potencia y calidad que sus equivalentes de marca.
-- Scott Roberts

Copyright © 2015 HealthDay. Todos los derechos reservados.
 ¿Es hora de incluir microorganismos vivos y seguros como componentes de una dieta equilibrada?
¿Es hora de incluir microorganismos vivos y seguros como componentes de una dieta equilibrada?
 Cómo encontrar un profesional de medicina funcional de confianza
Cómo encontrar un profesional de medicina funcional de confianza
 Lomotil para la diarrea del SII
Lomotil para la diarrea del SII
 Salud digestiva:¿Por qué estoy hinchado?
Salud digestiva:¿Por qué estoy hinchado?
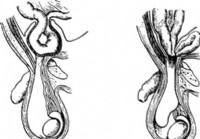 Las hernias inguinales restringidas - Diagnóstico del abdomen agudo
Las hernias inguinales restringidas - Diagnóstico del abdomen agudo
 ¿Por qué me duele el estómago después de cada comida?
¿Por qué me duele el estómago después de cada comida?
 Cáncer de esófago:¿qué es?
El cáncer de esófago (también llamado cáncer de esófago) es un tumor maligno que crece en el revestimiento del esófago. El esófago (la garganta) es el conducto que transporta los alimentos desde la b
Cáncer de esófago:¿qué es?
El cáncer de esófago (también llamado cáncer de esófago) es un tumor maligno que crece en el revestimiento del esófago. El esófago (la garganta) es el conducto que transporta los alimentos desde la b
 Frijoles, súper alimento para la salud intestinal y cerebral
Tal vez te lo hayas perdido en las noticias últimamente, pero se ha informado que los frijoles saludables son súper alimentos, no solo para el intestino sino también para la salud física y mental en g
Frijoles, súper alimento para la salud intestinal y cerebral
Tal vez te lo hayas perdido en las noticias últimamente, pero se ha informado que los frijoles saludables son súper alimentos, no solo para el intestino sino también para la salud física y mental en g
 La dieta para la enfermedad celíaca:por qué no funciona la dieta sin gluten (y qué hacer en su lugar)
Estaba listo para perder la esperanza… Años de diarrea… Fatiga Crónica… Depresión… Ansiedad… Acné… Estaba muriendo lentamente… Y las cosas siguieron empeorando. Los médicos no sabían qué me pa
La dieta para la enfermedad celíaca:por qué no funciona la dieta sin gluten (y qué hacer en su lugar)
Estaba listo para perder la esperanza… Años de diarrea… Fatiga Crónica… Depresión… Ansiedad… Acné… Estaba muriendo lentamente… Y las cosas siguieron empeorando. Los médicos no sabían qué me pa