LUNES, 19 de diciembre de 2016 (HealthDay News) -- El medicamento contra el cáncer Rubraca (rucaparib) recibió la aprobación acelerada de la Administración de Alimentos y Medicamentos (FDA) de EE. UU. para tratar el cáncer de ovario avanzado.
La aprobación se limita a los casos en los que el cáncer es causado por mutaciones genéticas específicas conocidas como "BRCA nocivo".
Los genes BRCA normalmente reparan el ADN dañado y están diseñados para prevenir el crecimiento de tumores, dijo la agencia el lunes en un comunicado de prensa. Pero las mutaciones en estos genes podrían provocar cáncer.
Rubraca está diseñado para inhibir cierta enzima producida por un gen BRCA dañado.
Se proyecta que más de 22 000 mujeres serán diagnosticadas con cáncer de ovario este año, y más de 14 000 morirán a causa de la enfermedad, según estimaciones del Instituto Nacional del Cáncer de EE. UU. citadas por la FDA.
La FDA aprobó simultáneamente el examen de diagnóstico FoundationFocus CDxBRCA. Esta prueba detecta la presencia de mutaciones nocivas de BRCA en los tumores de mujeres con cáncer de ovario, dijo la FDA.
Rubraca se evaluó en estudios clínicos en los que participaron 106 mujeres con cáncer de ovario avanzado con mutación BRCA. Cincuenta y cuatro por ciento de los participantes que recibieron Rubraca tuvieron una reducción total o parcial de los tumores, con una duración promedio de 9.2 meses, dijo la agencia.
Los efectos secundarios más comunes del medicamento incluyeron náuseas, fatiga, vómitos, anemia, dolor abdominal, sensación de sabor inusual y pérdida de apetito. El medicamento también se asoció con problemas de la médula ósea, leucemia mieloide aguda y daño al feto en desarrollo, advirtió la FDA.
Rubraca es comercializado por Clovis Oncology, con sede en Boulder, Colorado.
-- Scott Roberts

Copyright © 2016 HealthDay. Todos los derechos reservados.
 Cálculos biliares (colelitiasis)
Cálculos biliares (colelitiasis)
 ¿Cómo puedo recuperar la salud de mi hígado?
¿Cómo puedo recuperar la salud de mi hígado?
 Cuide su salud intestinal en esta temporada de regreso a clases
Cuide su salud intestinal en esta temporada de regreso a clases
 Para mujeres (ayuda con sus hormonas)
Para mujeres (ayuda con sus hormonas)
 ¿Cuáles son los síntomas de un intestino no saludable?
¿Cuáles son los síntomas de un intestino no saludable?
 La genética puede influir en la composición del microbioma más que los factores ambientales
La genética puede influir en la composición del microbioma más que los factores ambientales
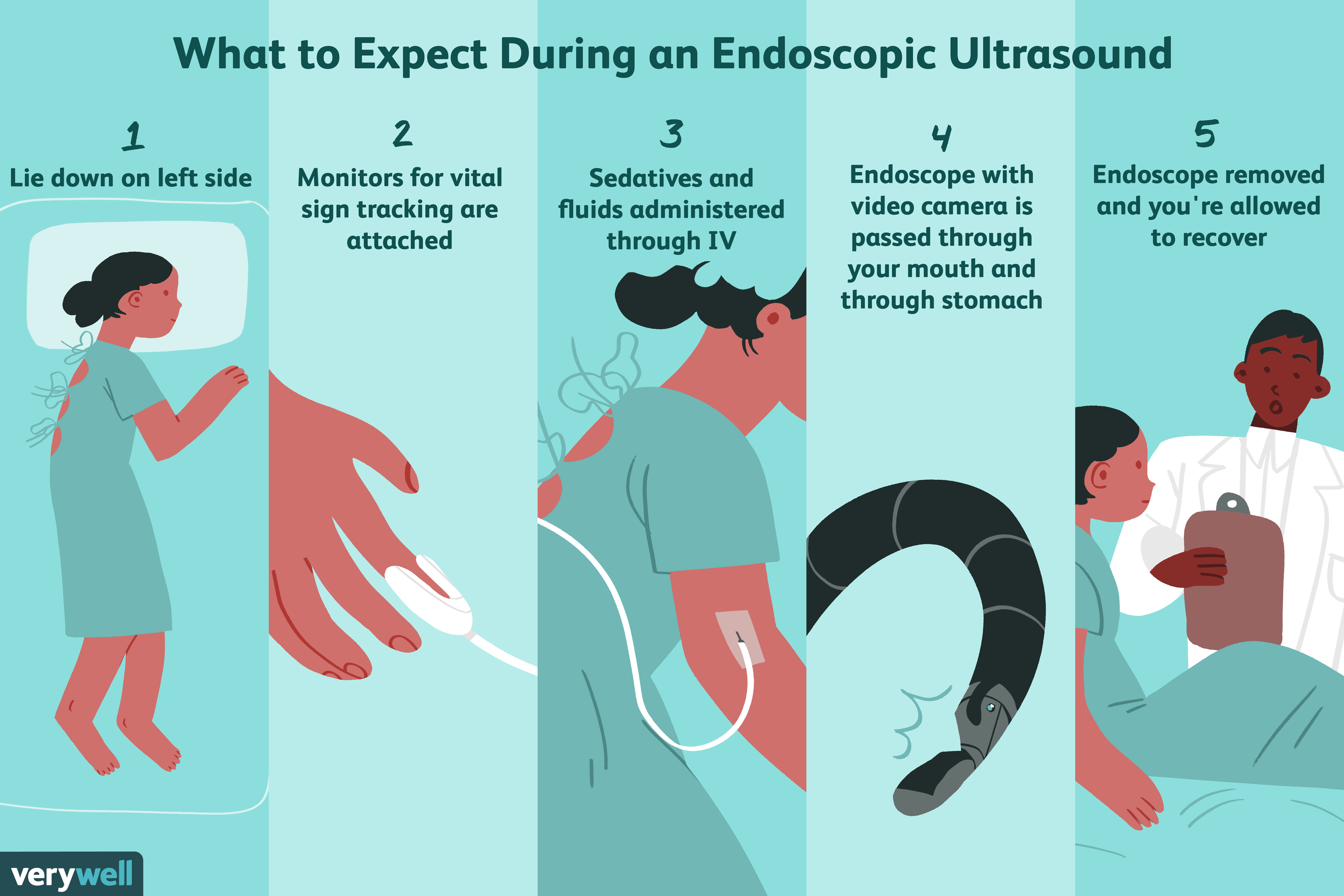 ¿Qué es la ecografía endoscópica?
Un ultrasonido endoscópico es una prueba que ayuda a visualizar partes del tracto digestivo, como el estómago, el páncreas y la vesícula biliar, y los órganos y tejidos cercanos, como el sistema linfá
¿Qué es la ecografía endoscópica?
Un ultrasonido endoscópico es una prueba que ayuda a visualizar partes del tracto digestivo, como el estómago, el páncreas y la vesícula biliar, y los órganos y tejidos cercanos, como el sistema linfá
 La criptosporidiosis empeora con los probióticos de uso común
Los investigadores han descubierto que la infección por el parásito intestinal Cryptosporidium parvum empeora en ratones a los que se les ha administrado un probiótico. Haber de imagen:A
La criptosporidiosis empeora con los probióticos de uso común
Los investigadores han descubierto que la infección por el parásito intestinal Cryptosporidium parvum empeora en ratones a los que se les ha administrado un probiótico. Haber de imagen:A
 ¿Cómo puedo deshacerme de la diverticulitis rápidamente?
Deshacerse de la diverticulitis puede requerir una dieta para la diverticulitis recomendada por el médico, junto con ciertas modificaciones en el estilo de vida como parte de tu tratamiento La enfe
¿Cómo puedo deshacerme de la diverticulitis rápidamente?
Deshacerse de la diverticulitis puede requerir una dieta para la diverticulitis recomendada por el médico, junto con ciertas modificaciones en el estilo de vida como parte de tu tratamiento La enfe