MARDI 31 mai 2016 (HealthDay News) -- Ocaliva (acide obéticholique) a été approuvé par la Food and Drug Administration des États-Unis pour traiter une maladie hépatique chronique rare appelée cholangite biliaire primitive (CBP).
La maladie provoque l'inflammation des petits canaux biliaires du foie, détruisant finalement les canaux et conduisant à la cirrhose, qui est une cicatrisation du foie. Au fil du temps, cela conduit à une perte potentiellement mortelle de la fonction hépatique, a déclaré l'agence mardi dans un communiqué de presse.
Ocaliva est conçu pour augmenter le flux de bile du foie. Le médicament a été évalué dans des études cliniques portant sur 216 personnes, et les effets secondaires les plus fréquemment enregistrés comprenaient des démangeaisons cutanées, de la fatigue, des douleurs abdominales, des maux de gorge, des étourdissements et de la constipation.
Ocaliva ne doit pas être administré aux personnes dont les voies biliaires sont complètement obstruées, a averti la FDA.
Les études cliniques n'ont pas établi d'amélioration de la survie, de progression vers la cicatrisation du foie ou de suppression des symptômes liés à la maladie, a indiqué l'agence, notant que des essais cliniques évaluant ces facteurs sont en cours.
Ocaliva est produit par Intercept Pharmaceuticals, basé à New York.
-- Scott Roberts

Copyright © 2016 HealthDay. Tous droits réservés.
 Pourquoi les vomissements se produisent-ils ? Conseils et remèdes pour l'arrêter
Pourquoi les vomissements se produisent-ils ? Conseils et remèdes pour l'arrêter
 Une étude suggère un lien entre l'utilisation de probiotiques et le « brouillard cérébral »
Une étude suggère un lien entre l'utilisation de probiotiques et le « brouillard cérébral »
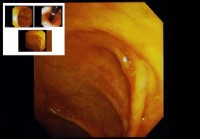 Qu'est-ce qu'une chromoendoscopie ?
Qu'est-ce qu'une chromoendoscopie ?
 Des scientifiques extraient le génome humain complet d'un « chewing-gum » vieux de plusieurs milliers d'années
Des scientifiques extraient le génome humain complet d'un « chewing-gum » vieux de plusieurs milliers d'années
 Les fuites intestinales et la dysbiose microbienne pourraient contribuer à la tempête de cytokines dans les cas de COVID-19 gravement malades
Les fuites intestinales et la dysbiose microbienne pourraient contribuer à la tempête de cytokines dans les cas de COVID-19 gravement malades
 Les patients sous immunothérapie devraient consommer plus de fibres,
Les patients sous immunothérapie devraient consommer plus de fibres,
 Symptômes d'une perforation de l'ulcère - Diagnostic de l'abdomen aigu
Lors dune perforation de lulcère dans un état libre cavité abdominale tous les symptômes de perforation peuvent être divisés en deux groupes : 1) principaux symptômes (leaders) et 2) symptômes auxilia
Symptômes d'une perforation de l'ulcère - Diagnostic de l'abdomen aigu
Lors dune perforation de lulcère dans un état libre cavité abdominale tous les symptômes de perforation peuvent être divisés en deux groupes : 1) principaux symptômes (leaders) et 2) symptômes auxilia
 Indigestion (dyspepsie, maux d'estomac)
Définition de lindigestion (dyspepsie, maux destomac) et faits Lindigestion peut avoir de nombreuses causes différentes. Lindigestion (dyspepsie) est une maladie fonctionnelle dans laquelle les organ
Indigestion (dyspepsie, maux d'estomac)
Définition de lindigestion (dyspepsie, maux destomac) et faits Lindigestion peut avoir de nombreuses causes différentes. Lindigestion (dyspepsie) est une maladie fonctionnelle dans laquelle les organ
 Journal de guérison diététique SCD de Steve :Semaine 24 – L'échec de la puce au chou frisé !
Le co-fondateur de SCD Lifestyle, Steve Wright, sest finalement effondré et a commencé son chemin vers la guérison intestinale. Après de nombreuses années de guerre digestive non diagnostiquée dans so
Journal de guérison diététique SCD de Steve :Semaine 24 – L'échec de la puce au chou frisé !
Le co-fondateur de SCD Lifestyle, Steve Wright, sest finalement effondré et a commencé son chemin vers la guérison intestinale. Après de nombreuses années de guerre digestive non diagnostiquée dans so