Kokolorektalt karcinom som härrör från kolon eller rektal slemhinna (topincidens 60-70 år). De ses vanligtvis hos äldre patienter eller unga patienter som vanligtvis har ulcerös kolit, kroniska eller genetiska predispositionsfenotyper som familjär polypossyndrom (FAP) och Lynch syndrom (HNPCC).
Orsaker och riskfaktorer för kolorektal cancer: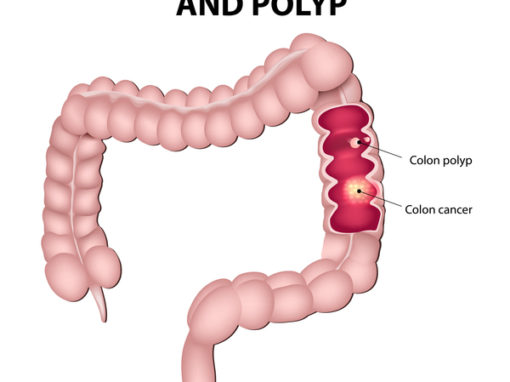
Innehållsförteckning
- 1 Orsaker och riskfaktorer för kolorektal cancer:
- 2 symtom och klinisk presentation
- 3 Morfologi av kolonkarcinom
- 4 Diagnos av kolorektal cancer
- 5 Diagnostik av tjocktarmscancer
- 6 labb efter behandling
- 7 Behandling av tjocktarmscancer
Den vanligaste orsaken till kolorektal cancer beror på adenom-karcinomsekvensen (APC, KRAS, P53-mutation) hos 90 %. Den näst viktigaste molekylära vägen för att orsaka kolorektal cancer är MSI-mutation (10 %) som kan involvera polyper eller inte.
Riskfaktorer för att utveckla kolorektal cancer inkluderar:inflammatorisk tarmsjukdom (IBD), rökning, kost med låg fiberhalt och hög animalisk fetthalt, fetma och stillasittande livsstil.
Annat samband:Endokardit med (Streptococcus bovis och Clostridium speticum) – därför behöver alla patienter med endokardit av dessa organismer koloskopi för att utesluta intestinal malignitet.
Symtom och klinisk presentation
Kokolorektal cancer är vanligtvis asymtomatisk tills tumören växer sig större och orsakar symtom. Eftersom de flesta lesioner börjar med polyper är det viktigt att screena för polyper och ta bort dem om de upptäcks.
Högersidig lesion med trötthet, svaghet och Fe-brist på grund av blodförlust (melena) från tumörsår som är skrymmande och lätt blöder. Fe
2+
Bristanemi hos äldre är GI-malignitet om inte annat bevisas.
Vänstersidig lesion med förändrade tarmvanor (obstruktion) och klarröda blödningar (hematochezi) som ibland har pennavföring.
- Adenom-karcinomsekvens
- Uppstår från APC/β-catenin: KRAS, P53/DCC-mutationssekvens
- Platsen är vänstersidig (rektalsigmoid eller distal kolon), vänster nedre quad (LLQ) smärta
- Tumör närvarande som servettring-konstriktionspolyptyp.(bildar vanligtvis adenoma polyper först)
- Orsaka obstruktion av tarmen (främst), kan också orsaka ljusa blödningar.
- Genetisk predisposition:Germline APC-mutation (leder till FAPs/Gardner/Turcot syndrom)
- MSI (mikrosatellitinstabilitet) Mismatch Repair Genmutationsväg.
- Uppstår från DNA-felmatchningsreparationsgenmutationer (MSH2, MSH6, MSL1, PMS etc)
- Platsen är högersidig (stigande/proximal kolon), höger nedre quad vag smärta
- Tumör närvarande som exofytisk massa polyptyp (kan eller kanske inte bildar adenomatösa polyper.)
- Orsak blödning, därav Fe
2+
bristanemi
- Genetisk predisposition:Germline MSH2, MSL1 könslinjemutation (HNPCC=Lynch syndrom)
- Öka risken för andra cancerformer:kolorektal cancer, äggstockscancer, endometriecancer, mage, gallvägar, även tunntarmen, bukspottkörteln
- Karcinom uppstår denovo, inte från adenomatös polyp vid mycket ung ålder.
Morfologi av kolonkarcinom
- Vanligtvis ensam om inte genetiskt predisponerade säger FAPs
- Flera cancerformer (ulcerös kolit, polypossyndrom, HNPCC)
- Neoplastiska körtlar som invaderar submucosa och vidare à regional LN (lymfkörtel), lever, lunga, ben
- 10-15 % kan producera omfattande mucin
Diagnos av kolorektal cancer
- Riktlinjer för skärmning:
- Utan genetisk risk Patient ≥ 50 år.
- Kolonoskopi vart tionde år* bästa metoden.
- Fekalt ockult blodprov årligen och om det är positivt kommer du att behöva en koloskopi (Falskt negativt om C-vitamin konsumeras, Falskt positivt om NSAID används.)
- Flexibel Sigmoidoskopi eller dubbel kontrast Barium vart 5:e år
- Om dysplastiska polyper hittats tidigare
- behöver colonoscoy-screening vart 3-5 år
- Om jag själv hade tjocktarmscancer
- 1 år efter resektion, sedan vid 3 år, följt av vart femte år
- Om enstaka FHx av cancer/polyper
- 10 år innan familjen har tjocktarmscancer /polyp ELLER 40 år gammal skärm (beroende på vilket som kommer först)
- Behöver upprepa koloskopi vart 3-5 år
- HNPCC (Lynchsyndrom) – MSI-mutation (syndrom definierat av 3 familjemedlemmar i minst 2 generationer har tjocktarmscancer
- Börja vid 25 års ålder (koloskopi vart 1-2 år)
- Hög förekomst av äggstockscancer och endometriecancer
- FAPS (Familiar Adenomatous Polyposis Syndrome)
- Börja vid 12 års ålder (Flexi sigmoidoskopi vart 1-2 år)
- Polyper så tidigt som 25 år gamla och 100 % penetrans – tjocktarmscancer vid 50 år.
- Om polyper positiva (total kolektomi) måste göras och anslut terminal ileum för att bilda ett nytt rektum.
- FAP-varianter (ingen screeningsrekommendation ännu)
- Gardners syndrom:Tjocktarmscancer associerad med mjukdelstumörer (lipom, osteom, fibromsarkom) – osteom speciellt vid underkäken – gör koloskopi om du ser någon av de associerade mjukdelstumörerna. Vissa rekommenderar skärm som FAP.
- Turcot syndrom:Koloncancer associerad med CNS-malignitet (GBM, Medulloblastom)
- Harmatomatös polypossyndrom (ingen rekommendation ännu)
- Juvenilt polypossyndrom (10 % risk för tjocktarmscancer till skillnad från FAPS) – bara några dussin till skillnad från FAP-tusentals. Icke-adenom (Harmatom) lågriskcancer
- Cowdens syndrom – rektal blödning som barn (även harmatom) endast liten risk än släktpopulationen
- Dannayan-Ruvacalba-Rileys syndrom
- Peutz-Jeghers polypssyndrom
- För patient med IBD
- Särskilt ulcerös kolit Med diagnosen 8-10 år måste du undersöka koloskopi vart 1-2 år för kolorektal cancer.
Diagnos av tjocktarmscancer
- Kolonoskopi (endast 60 % av tjocktarmscancer fångas med sigmoidoskopi)
Labb efter behandling
- CEA användbart för att följa terapeutiskt svar och upptäcka återfall, inte bra för screening.
- Också gjort före behandling för att jämföra
Behandling av tjocktarmscancer
- Beroende på scenen och spridningens omfattning.
- Metastaserande leversjukdom (en lesion) kan avlägsnas kirurgiskt om> 1 lesion =kemoterapi.
- Lokaliserad (mucosa, submucosa, muscularis mucosae) – kan resekeras för att botas
- Penetrerade serosa eller omgivande vävnad och LN – Kemoterapi
- 5FU + Leukovirin
- Xeloda =Capecitabin =5FU prodrug; Leukovirin =folinsyra
- Nya läkemedel – Avastin (Bevacizumab) som är en VEGF-hämmare som blockerar kärltillväxt för att försörja den växande tumören.

 Tiopuriner kan hjälpa till att stoppa viral replikation hos mänskliga coronavirus
Tiopuriner kan hjälpa till att stoppa viral replikation hos mänskliga coronavirus
 Så här påverkar din tarm och matsmältning din sömn
Så här påverkar din tarm och matsmältning din sömn
 Hjälp en hemorrojder tillbaka?
Hjälp en hemorrojder tillbaka?
 Råfoder för sällskapsdjur är en risk för människor och djur
Råfoder för sällskapsdjur är en risk för människor och djur
 Ska du prova Iberogast för din IBS?
Ska du prova Iberogast för din IBS?
 Kära mamma, 7 steg för att minska risken för bröstcancer
Kära mamma, 7 steg för att minska risken för bröstcancer
 Vilka är de typiska SIBO-symtomen?
Det enda som är förenligt med SIBO är att ingen är den andra lik när det kommer till deras symtom. Vissa människor känner knappt någonting medan andra är sängliggande och oförmögna att arbeta. Det fin
Vilka är de typiska SIBO-symtomen?
Det enda som är förenligt med SIBO är att ingen är den andra lik när det kommer till deras symtom. Vissa människor känner knappt någonting medan andra är sängliggande och oförmögna att arbeta. Det fin
 Icke-alkoholisk fettleversjukdom:Vad du bör veta
Senast uppdaterad:12 april 2021 Termen leversjukdom omfattar många olika tillstånd inklusive hepatit, levercancer, fettleversjukdom och genetiska tillstånd som hemokromatos. Hoppas du fortfarande är
Icke-alkoholisk fettleversjukdom:Vad du bör veta
Senast uppdaterad:12 april 2021 Termen leversjukdom omfattar många olika tillstånd inklusive hepatit, levercancer, fettleversjukdom och genetiska tillstånd som hemokromatos. Hoppas du fortfarande är
 Studie med tvillingar visar att covid-19-symtom har ett genetiskt bidrag
En ny studie publicerad på förtrycksservern medRxiv från Kings College, London, föreslår att en individs genetiska sammansättning kan bidra till hur mycket en person sannolikt kommer att påverkas av
Studie med tvillingar visar att covid-19-symtom har ett genetiskt bidrag
En ny studie publicerad på förtrycksservern medRxiv från Kings College, London, föreslår att en individs genetiska sammansättning kan bidra till hur mycket en person sannolikt kommer att påverkas av