Их исследование под названием «Тиопурины активируют противовирусный ответ развернутого белка, который блокирует накопление вирусных гликопротеинов в модели инфекции клеточной культуры, »Был опубликован в виде предпечатной версии на сайте bioRxiv * .
Исследователи объяснили, что вирусы, которые обволакивают, такие как коронавирус, имеют генетический материал, который может кодировать мембранные белки, которые могут быть синтезированы и модифицированы в эндоплазматическом ретикулуме (ЭР), прежде чем они могут быть доставлены в области сборки частей вириона.
Если способность к укладке белка ER подавляется слишком большим количеством частиц вириона, в ЭПР наблюдается перегрузка развернутыми белками. Это вызывает развернутый белковый ответ (UPR). Это активирует фактор транскрипции-6 (ATF6), инозит, требующий фермента-1 (IRE1) и PKR-подобную киназу эндоплазматического ретикулума (PERK). Они могут почувствовать, что ER находится в состоянии стресса, и, таким образом, происходит синтез основных факторов транскрипции лейциновой молнии (bZIP).
Когда UPR активируется, способность ER к укладке белков увеличивается. Это также запускает деградацию, связанную с ER (ERAD). Все белки, которые не свернуты должным образом, выводятся из ER и разрушаются через протеасому 26S.
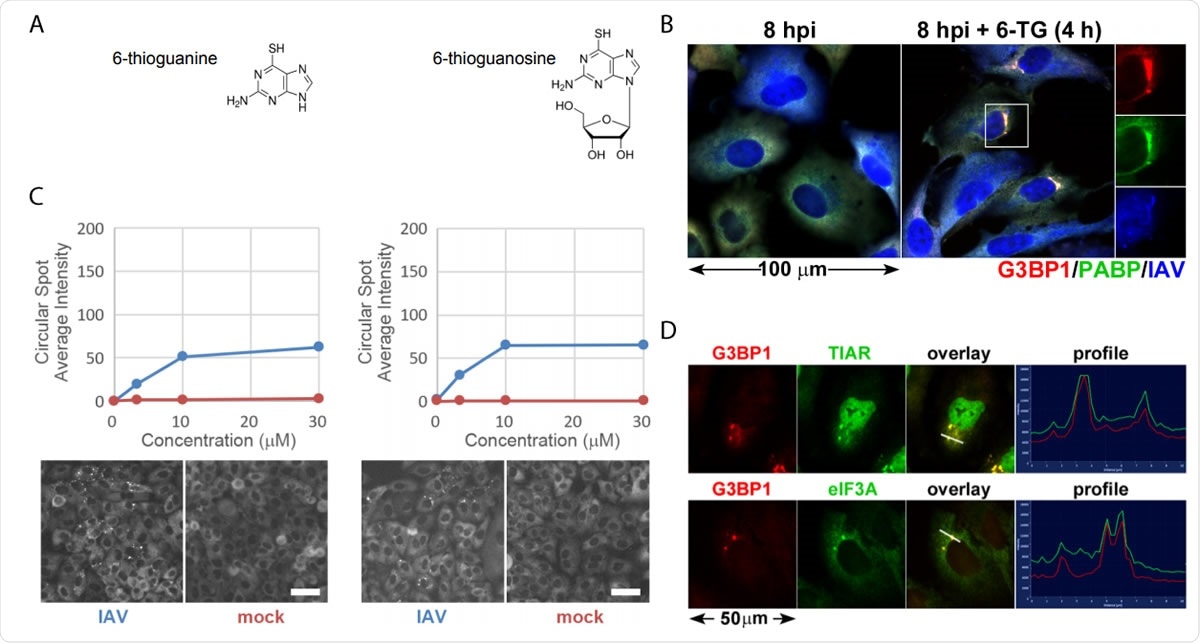 Аналоги тиопурина 6-TG и 6-TGo избирательно индуцируют стрессовые гранулы в инфицированных IAV клетках. (A) Структурные диаграммы небольших молекул, идентифицированных на экране. (B) Количественная оценка образования очагов EGFP-G3BP в инфицированных IAV-Udorn (синий) или ложных (красный) инфицированных клетках, обработанных возрастающими дозами 6-TG и 6-TGo (вверху), и репрезентативные изображения Cellomics канала EGFP обработанных клеток с 30 мкМ 6-TG и 6-TGo (внизу). При 4 hpi, клетки обрабатывали 0, 1, Дозы 10 и 30 мкМ аналогов тиопурина 6-тиогуанин (6-TG) или 6-тиогуанозин (6-TGo). При 8 hpi, клетки фиксировали и окрашивали Hoeschst 33342. Автоматизированный захват изображений выполняли с использованием ридера Cellomics Arrayscan VTI HCS. Для каждой лунки было снято 15 изображений и рассчитана средняя интенсивность точечного EGFP-G3BP1. (C) Клетки A549 были инфицированы IAV-CA / 07 при MOI, равном 1. При 4 hpi, клетки обрабатывали 6-TG или имитировали. При 8 hpi, клетки фиксировали и иммуноокрашивали антителами, направленными на белки-маркеры стрессовых гранул G3BP1 (красный), PABP (зеленый) и поликлональное антитело против IAV (синий), которое выявляет антигены из NP, M1, и HA, с последующим окрашиванием вторичными антителами, конъюгированными с Alexa. (D) Клетки A549 были инфицированы IAV-CA / 07 при MOI, равном 1. При 4 hpi, клетки обрабатывали 6-ТГ (10 мкМ). При 8 hpi, клетки фиксировали и иммуноокрашивали антителами, направленными на белки-маркеры стрессовых гранул G3BP1 (красный), TIAR (зеленый) и eIF3A (зеленый), с последующим окрашиванием вторичными антителами, конъюгированными с Alexa. Изображения получены на флуоресцентном микроскопе Zeiss Axioimager Z2. Показаны репрезентативные изображения. Масштабные полосы представляют собой 20 мкм.
Аналоги тиопурина 6-TG и 6-TGo избирательно индуцируют стрессовые гранулы в инфицированных IAV клетках. (A) Структурные диаграммы небольших молекул, идентифицированных на экране. (B) Количественная оценка образования очагов EGFP-G3BP в инфицированных IAV-Udorn (синий) или ложных (красный) инфицированных клетках, обработанных возрастающими дозами 6-TG и 6-TGo (вверху), и репрезентативные изображения Cellomics канала EGFP обработанных клеток с 30 мкМ 6-TG и 6-TGo (внизу). При 4 hpi, клетки обрабатывали 0, 1, Дозы 10 и 30 мкМ аналогов тиопурина 6-тиогуанин (6-TG) или 6-тиогуанозин (6-TGo). При 8 hpi, клетки фиксировали и окрашивали Hoeschst 33342. Автоматизированный захват изображений выполняли с использованием ридера Cellomics Arrayscan VTI HCS. Для каждой лунки было снято 15 изображений и рассчитана средняя интенсивность точечного EGFP-G3BP1. (C) Клетки A549 были инфицированы IAV-CA / 07 при MOI, равном 1. При 4 hpi, клетки обрабатывали 6-TG или имитировали. При 8 hpi, клетки фиксировали и иммуноокрашивали антителами, направленными на белки-маркеры стрессовых гранул G3BP1 (красный), PABP (зеленый) и поликлональное антитело против IAV (синий), которое выявляет антигены из NP, M1, и HA, с последующим окрашиванием вторичными антителами, конъюгированными с Alexa. (D) Клетки A549 были инфицированы IAV-CA / 07 при MOI, равном 1. При 4 hpi, клетки обрабатывали 6-ТГ (10 мкМ). При 8 hpi, клетки фиксировали и иммуноокрашивали антителами, направленными на белки-маркеры стрессовых гранул G3BP1 (красный), TIAR (зеленый) и eIF3A (зеленый), с последующим окрашиванием вторичными антителами, конъюгированными с Alexa. Изображения получены на флуоресцентном микроскопе Zeiss Axioimager Z2. Показаны репрезентативные изображения. Масштабные полосы представляют собой 20 мкм. Когда вирусная частица проникает в клетку, он пытается быстро воспроизвести, и это обременяет ER. Вирус выделяет выбросы гликопротеинов, которые подавляют ER. Вирус, тем не мение, способен обходить UPR и способствует эффективной репликации.
IAV может кодировать три интегральных мембранных белка:гемагглютинин (HA), нейраминидаза (NA), и матричный белок 2 (M2). В то время как репликация IAV вызывает избирательную активацию UPR, определенные механизмы могут активировать UPR, но затем обходить его, способствуя эффективной репликации вируса. Команда объясняет, что влияние белков NA и M2 на UPR неясно, но HA может продвигать UPR.
Несколько коронавирусов (CoV) могут активировать UPR. Это включает «вирус инфекционного бронхита (IBV), вирус гепатита мышей (MHV), вирус трансмиссивного гастроэнтерита (TGEV), коронавирус человека (HCoV) -OC43, и SARS-CoV-1 ». Вся генетическая последовательность, тем не мение, не реагирует аналогично на репликацию CoV.
Команда определила два одобренных FDA аналога тиопурина, названных «6-тиогуанин (6-TG) и 6-тиогуанозин (6-TGo)». Было обнаружено, что они блокируют репликацию IAV и HCoV-OC43 при постепенном увеличении их дозы.
Патамин А и Сильвестрол были протестированы ранее. Эти два тиопурина, тем не мение, Было обнаружено, что они нарушают процесс накопления вирусных гликопротеинов, которые могут активировать UPR. В клетках, обработанных 6-ТГ, синтез вирусного гликопротеина может быть частично восстановлен за счет химического ингибирования UPR.
Белки CoV Spike (S), которые экспрессируются на поверхности вируса, показали активацию UPR. Белок S из нового коронавируса или SARS-CoV-2 S также вызывал активацию UPR. 6-ТГ ингибировал накопление полноразмерных слитых белков S0 или расщепленных фурином S2, они отметили. Это не повлияло на эктодомен S1. 6-TG может индуцировать UPR, который ускоряет ERAD-опосредованный обмен гликопротеинов S0 и S2, заякоренных в мембране, команда нашла.
Исследователи провели эксперименты и обнаружили, что химически подобное соединение тиопурин 6-меркаптопурин (6-MP) мало влияет на UPR и не влияет на репликацию IAV HCoV-OC43.
Размышляя о механизме индукции UPR тиопуриновыми соединениями 6-TG и 6-TGo, команда писала, что эти эффекты вряд ли будут опосредованы включением 6-TG в ДНК или РНК по нескольким причинам. Первая причина заключается в том, что стресс, связанный с репликацией вируса, не вызывает специфического UPR. Вторая причина заключается в том, что среди вирусных белков накопление гликопротеинов и их переработка избирательно нарушалась. Третья причина заключалась в том, что уровни информационной РНК HA и NA в IAV не подвергались значительному влиянию. 6-МП, с другой стороны, может быть преобразован в 6-тиогуанозинтрифосфат, но не вызывает UPR и не влияет на гликопротеины IAV или репликацию OC43.
Команда написала, что их данные показывают, что «молекулы, вызывающие UPR, могут быть эффективными противовирусными препаратами, нацеленными на хозяина, против вирусов, которые зависят от процессов ER для поддержки эффективной репликации». Таким образом, индукция UPR с помощью 6-TG и 6-TGo может быть новым методом, с помощью которого противовирусный механизм может запускаться самой клеткой-хозяином. Это был ранее неизвестный уникальный механизм действия, команда написала.
<цитата>В заключение они написали:«... эти данные показывают, что 6-TG и 6-TGo являются эффективными противовирусными препаратами, нацеленными на хозяина, которые запускают UPR и нарушают накопление вирусных гликопротеинов».
medRxiv публикует предварительные научные отчеты, которые не рецензируются, и следовательно, не следует рассматривать как окончательный, руководить клинической практикой / поведением, связанным со здоровьем, или рассматриваться как установленная информация.
 Клещи теперь переносят множество болезней,
Клещи теперь переносят множество болезней,
 Домашние собаки вряд ли будут передавать SARS-CoV-2,
Домашние собаки вряд ли будут передавать SARS-CoV-2,
 Анализ крови на микробную ДНК может предупредить о раке
Анализ крови на микробную ДНК может предупредить о раке
 Нил Белл назначен директором по развитию Avacta Life Sciences
Нил Белл назначен директором по развитию Avacta Life Sciences
 Если вам больше 50,
Если вам больше 50,
 Распространение супербактерии E. coli из-за плохой гигиены туалета,
Распространение супербактерии E. coli из-за плохой гигиены туалета,
 Микробы легких могут помочь предсказать исходы у тяжелобольных
Новое исследование, опубликованное в Американский журнал респираторной медицины и реанимации показывает, что регистрация того, как организмы, живущие в легких, меняются по типу и количеству, может о
Микробы легких могут помочь предсказать исходы у тяжелобольных
Новое исследование, опубликованное в Американский журнал респираторной медицины и реанимации показывает, что регистрация того, как организмы, живущие в легких, меняются по типу и количеству, может о
 Что такое ERCP?
Если мы подозреваем потенциальную проблему с желчным пузырем, желчная система, поджелудочная железа или печень, мы можем заказать эндоскопическую ретроградную холангиопанкреатографию (ЭРХПГ). ERCP исс
Что такое ERCP?
Если мы подозреваем потенциальную проблему с желчным пузырем, желчная система, поджелудочная железа или печень, мы можем заказать эндоскопическую ретроградную холангиопанкреатографию (ЭРХПГ). ERCP исс
 Генетика может влиять на состав микробиома больше, чем факторы окружающей среды.
Исследователи, изучающие мышей в Израильском технологическом институте Техниона, обнаружили, что на микробиом гораздо больше влияет генетика, чем среда материнского рождения. Катерина Кон |
Генетика может влиять на состав микробиома больше, чем факторы окружающей среды.
Исследователи, изучающие мышей в Израильском технологическом институте Техниона, обнаружили, что на микробиом гораздо больше влияет генетика, чем среда материнского рождения. Катерина Кон |