SRIJEDA, 1. veljače (HealthDay News) -- Odobrenje američke Uprave za hranu i lijekove za Novartisov lijek Gleevec prošireno je tako da uključuje odrasle osobe koje su imale kirurško uklanjanje CD117-pozitivnih gastrointestinalnih stromalnih tumora (GIST), objavila je agencija u vijestima oslobodi.
GIST je rijedak rak koji se formira u stanicama koje oblažu zidove GI trakta, uključujući želudac. Takve stanice igraju ulogu u probavi hrane i drugim tjelesnim procesima, kaže FDA.
Gleevec, koji je prvi put odobren 2001. za liječenje genetske bolesti nazvane kronična mijeloična leukemija pozitivne na kromosom Philadelphia, naknadno je kažnjen zbog brojnih oblika GIST-a.
Gleevecova oznaka bit će ažurirana kako bi uključila rezultate kliničkih studija o CD117-pozitivnom GIST-u. Lijek je značajno povećao preživljavanje pacijenata kada se uzimao 36 mjeseci, u usporedbi sa standardnih 12 mjeseci, rekla je FDA.
Uobičajene kliničke nuspojave Gleeveca uključivale su oticanje, mučninu i povraćanje, grčeve u mišićima, bolove u kostima ili mišićima, proljev, osip, umor i bolove u trbuhu.
Novartis ima sjedište u East Hannoveru, N.J.
-- Scott Roberts
 Autorska prava © 2012 HealthDay. Sva prava pridržana.
Autorska prava © 2012 HealthDay. Sva prava pridržana.
 Istraživanja pokazuju da probiotici mogu pomoći u borbi protiv anksioznosti i depresije
Istraživanja pokazuju da probiotici mogu pomoći u borbi protiv anksioznosti i depresije
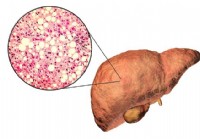 Koliko dugo živite s NAFLD-om? Stope preživljavanja
Koliko dugo živite s NAFLD-om? Stope preživljavanja
 Steveov dnevnik iscjeljenja SCD-a:26. tjedan – Kokosova voda je Gatorade majke prirode!
Steveov dnevnik iscjeljenja SCD-a:26. tjedan – Kokosova voda je Gatorade majke prirode!
 Može li se izliječiti alkoholni hepatitis?
Može li se izliječiti alkoholni hepatitis?
 Vjerojatnije komplikacije kod hitne operacije žučnog mjehura:studija
Vjerojatnije komplikacije kod hitne operacije žučnog mjehura:studija
 Specifična dijeta s ugljikohidratima Prijatelji u središtu pažnje:Kat s Kat's Food Bloga
Specifična dijeta s ugljikohidratima Prijatelji u središtu pažnje:Kat s Kat's Food Bloga
 Može li infekcija bubrega uzrokovati bol u leđima?
Što je infekcija bubrega bol u leđima? Ako osjećate bol u donjem dijelu leđa uz često mokrenje, krv u mokraći, groznicu ili zimicu, može imati infekciju bubrega bol u leđima. Bol u donjem dijelu l
Može li infekcija bubrega uzrokovati bol u leđima?
Što je infekcija bubrega bol u leđima? Ako osjećate bol u donjem dijelu leđa uz često mokrenje, krv u mokraći, groznicu ili zimicu, može imati infekciju bubrega bol u leđima. Bol u donjem dijelu l
 U centru pažnje:Erin iz NoMoreCrohns
Prioritet nam je istaknuti SCD ličnosti s cijelog interneta. Volimo slušati priče o uspjehu i želimo širiti znanje onih koji su dovoljno hrabri da podijele svoje specifične priče o dijeti s ugljikohid
U centru pažnje:Erin iz NoMoreCrohns
Prioritet nam je istaknuti SCD ličnosti s cijelog interneta. Volimo slušati priče o uspjehu i želimo širiti znanje onih koji su dovoljno hrabri da podijele svoje specifične priče o dijeti s ugljikohid
 Kako se narodi razvijaju, tako mogu i bolesti crijeva
Posljednje vijesti o probavi Kada transplantacija bubrega ne uspije pokušati je ponovno Ne dopustite da vam žgaravica pokvari blagdansku gozbu Potražnja za transplantacijom jetre naglo raste Niske do
Kako se narodi razvijaju, tako mogu i bolesti crijeva
Posljednje vijesti o probavi Kada transplantacija bubrega ne uspije pokušati je ponovno Ne dopustite da vam žgaravica pokvari blagdansku gozbu Potražnja za transplantacijom jetre naglo raste Niske do