Makrofagai yra imuninės gynybos ląstelės, yra įgimtos imuninės sistemos, kuri stebi infekcijas, dalis. Tačiau, jų reakcija į bet kokius patogenus taip pat gali sukelti lėtinį ar per didelį uždegimą. Tokia nenormali makrofagų aktyvacija pastebima sergant reumatoidiniu artritu (RA) ir kitomis autoimuninėmis ligomis. Vienas RA gydymo tikslas yra modifikuoti makrofagų aktyvacijos būsenas ir sumažinti makrofagų įsiskverbimą į uždegimo audinį.
Plaučiuose, taip pat, infekcija gali sukelti makrofagų sukeltą uždegimą, dėl kurio sunaikinamas plaučių audinys. Jis taip pat gali sukelti citokinų audrą, pastebėtas esant ūminiam kvėpavimo distreso sindromui (ARDS). Makrofagų aktyvavimas priklauso nuo receptorių, kurie savo ruožtu reaguoja į įvairius išorinius signalus. Daugumą jų sukelia citokinai ir mikrobuose esantys antigenai.
Viena žinomiausių ir svarbiausių makrofagų aktyvatoriaus molekulių yra interferonas-γ (IFN-γ). Makrofagai, paruošti naudojant IFN-γ ekspoziciją, stipriau reaguoja į vėlesnę stimuliaciją. Kitoje panašioje aktyvatorių klasėje yra į rinkliavą panašių receptorių (TLR) agonistų, kurie išskiria makrofagus taip, kad išskiria molekules, kurios sudaro uždegiminį kūną, vadinamą uždegimu. Uždegiminių komponentų aktyvavimas sukelia ląstelės mirtį dėl piroptozės ir kartu išsiskiriančio interleukino -1β (IL -1β).
Mokslininkų žodžiais, “ Svarbus makrofagų atsako į pirminį signalą komponentas yra antrinio superaktyvatoriaus receptoriaus reguliavimas, kuris vėliau gali paversti šiuos pradėtus makrofagus į sprogmenį, galimai patogeniška uždegiminė būsena . “
Mokslininkai ištyrė keletą uždegiminių sąlygų, tokių kaip RA, Krono liga ir sunkus COVID-19, rasti naują antrinį superaktyvinantį makrofagų receptorių, vadinamą SLAMF7. Ši, jie sako, yra raktas į šių sąlygų patogenezę.
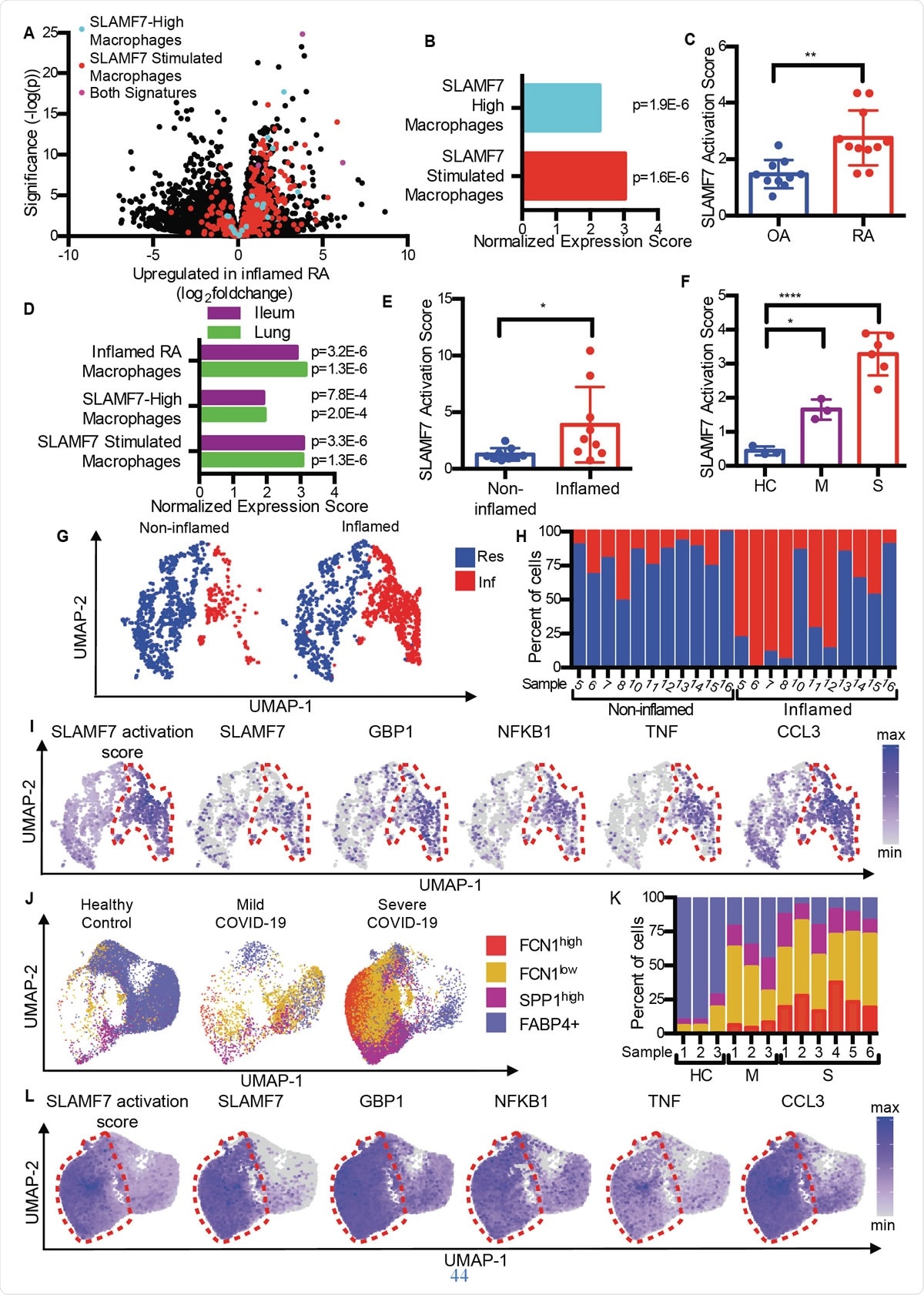 SLAMF7 super aktyvuoti makrofagai skatina uždegimą sergant autoimuninėmis ir infekcinėmis ligomis. A) 1A pav. Ugnikalnio brėžinys, išryškinantis genus iš „SLAMF7-High Macrophage Signature, “„ Makrofagų SLAMF7 stimuliavimo parašas, “Ir į abu parašus įtrauktus genus. B) Genų rinkinio praturtinimo analizė, lyginanti skirtingą genų ekspresiją RA ir OA su „SLAMF7-High Macrophage Signature“ ir „Macrophage SLAMF7 Stimulation Signature“. C) SLAMF7 aktyvinimo balas masiniams RNR seq duomenims apie sinovinius makrofagus iš pacientų, sergančių OA (n =10) arba RA (n =11). Duomenys reiškia vidurkį ± SD. D) Genų rinkinio praturtinimo analizė, kurioje lyginama genų ekspresija iš makrofagų iš uždegtų ilealinių audinių pacientams, sergantiems Krono liga, arba pacientų, sergančių COVID-19, plaučiais su „uždegimo RA makrofagų parašu“, „SLAMF7-High Macrophage Signature“ ir „Macrophage SLAMF7 Stimulation Signature“. E) SLAMF7 aktyvinimo balas makrofagams iš neuždegtų (n =9) ir uždegusių ilealinių audinių (n =9). F) SLAMF7 aktyvinimo balas bronchoalveolinio plovimo makrofagams iš sveikų kontrolinių grupių (n =3), arba asmenys, sergantys lengvu (n =3) ar sunkiu COVID-19 (n =6). E-F duomenys rodo vidurkį ± SD. G) Makrofagų grupių iš dalyvaujančių ir neįtrauktų ilealinių audinių UMAP grafikas. H) Makrofagų procentas iš kiekvieno donoro, priskirto kiekvienai grupei. I) UMAP brėžiniai, rodantys ilealinių makrofagų populiacijų genų ekspresiją. J) Bronchoalveolinio plovimo makrofagų populiacijų UMAP grafikas. K) Makrofagų procentas iš kiekvieno donoro, priskirto kiekvienai populiacijai. L) UMAP brėžiniai, rodantys bronchoalveolinio plovimo makrofagų populiacijų genų ekspresiją. Suporuotas t-testas buvo naudojamas abipusiam statistiniam palyginimui, ir vienpusis ANOVA su Dunnett daugybinio palyginimo testu buvo naudojamas palyginti lengvą ir sunkų COVID-19 su sveikomis kontrolėmis.*, p ≤ 0,05; **, p ≤ 0,01; ****, p <0,0001; Res, Gyventojų makrofagų klasteris; Inf, Uždegiminis makrofagų klasteris; HC, sveika kontrolė; M, lengvas COVID-19; S, sunkus COVID-19.
SLAMF7 super aktyvuoti makrofagai skatina uždegimą sergant autoimuninėmis ir infekcinėmis ligomis. A) 1A pav. Ugnikalnio brėžinys, išryškinantis genus iš „SLAMF7-High Macrophage Signature, “„ Makrofagų SLAMF7 stimuliavimo parašas, “Ir į abu parašus įtrauktus genus. B) Genų rinkinio praturtinimo analizė, lyginanti skirtingą genų ekspresiją RA ir OA su „SLAMF7-High Macrophage Signature“ ir „Macrophage SLAMF7 Stimulation Signature“. C) SLAMF7 aktyvinimo balas masiniams RNR seq duomenims apie sinovinius makrofagus iš pacientų, sergančių OA (n =10) arba RA (n =11). Duomenys reiškia vidurkį ± SD. D) Genų rinkinio praturtinimo analizė, kurioje lyginama genų ekspresija iš makrofagų iš uždegtų ilealinių audinių pacientams, sergantiems Krono liga, arba pacientų, sergančių COVID-19, plaučiais su „uždegimo RA makrofagų parašu“, „SLAMF7-High Macrophage Signature“ ir „Macrophage SLAMF7 Stimulation Signature“. E) SLAMF7 aktyvinimo balas makrofagams iš neuždegtų (n =9) ir uždegusių ilealinių audinių (n =9). F) SLAMF7 aktyvinimo balas bronchoalveolinio plovimo makrofagams iš sveikų kontrolinių grupių (n =3), arba asmenys, sergantys lengvu (n =3) ar sunkiu COVID-19 (n =6). E-F duomenys rodo vidurkį ± SD. G) Makrofagų grupių iš dalyvaujančių ir neįtrauktų ilealinių audinių UMAP grafikas. H) Makrofagų procentas iš kiekvieno donoro, priskirto kiekvienai grupei. I) UMAP brėžiniai, rodantys ilealinių makrofagų populiacijų genų ekspresiją. J) Bronchoalveolinio plovimo makrofagų populiacijų UMAP grafikas. K) Makrofagų procentas iš kiekvieno donoro, priskirto kiekvienai populiacijai. L) UMAP brėžiniai, rodantys bronchoalveolinio plovimo makrofagų populiacijų genų ekspresiją. Suporuotas t-testas buvo naudojamas abipusiam statistiniam palyginimui, ir vienpusis ANOVA su Dunnett daugybinio palyginimo testu buvo naudojamas palyginti lengvą ir sunkų COVID-19 su sveikomis kontrolėmis.*, p ≤ 0,05; **, p ≤ 0,01; ****, p <0,0001; Res, Gyventojų makrofagų klasteris; Inf, Uždegiminis makrofagų klasteris; HC, sveika kontrolė; M, lengvas COVID-19; S, sunkus COVID-19. Palyginti osteoartritą (OA) su reumatoidiniu artritu, tyrėjai nustatė, kad RA audinyje yra makrofagų su uždegimo parašu, įskaitant genų, kuriuos sukelia interferonas, ir genų, koduojančių uždegimines chemines medžiagas organizme, reguliavimą. Labiausiai išraiškos padidėjęs genas buvo SLAMF7.
Tai nustatyta mažu sąnarių sinovialinio audinio kiekiu iš sąnarių, kuriuos uždegė OA, tačiau aukštas lygis pacientams, sergantiems RA. Pastarojoje jo buvo 55% makrofagų, bet <6% pacientų, sergančių OA. Jis buvo dvigubai didesnis RA grupės sinovialinio skysčio makrofagų lygyje, palyginti su OA grupe, ir apie pusę ir ketvirtadalį kiekvienos grupės makrofagų, atitinkamai. Tačiau, tai nebuvo tiesa apie kitą SLAM receptorių, nurodydamas SLAMF7 kaip būdingą RA uždegiminiams makrofagams.
Nustatyta, kad IFN-γ yra pagrindinis šio receptoriaus induktorius makrofaguose, kartu su IFN-β, IL-1β ir TNF-α žemesniuose lygiuose. Tačiau, priešuždegiminis citokinas IL-6 nesukėlė SLAMF7 ekspresijos. Vėlgi, buvę citokinai sumažino kito SLAM receptoriaus kiekį, CD84, iki pusės.
Tyrėjai taip pat patvirtino, kad JAK kelias vaidino svarbų vaidmenį aktyvinant SLAMF7 tarpininkaujantį makrofagą. JAK inhibitorius ruxolitinibas jį veiksmingai slopino. Iš tiesų, šis vaistas vartojamas mielofibrozei gydyti, kur, vėl, randami aktyvuoti SLAMF7 ekspresuojantys makrofagai. Taip pat padvigubina CD84 lygį, tai gali reikšti, kad IFN-γ turi priešingą ir abipusį poveikį šiems dviem SLAM receptoriams.
Kitame žingsnyje SLAMF7 ekspresija buvo sukelta aukštu lygiu makrofaguose, pagal IFN-γ. Vėliau, buvo prijungtas aktyvinantis monokloninis antikūnas arba rekombinantinis SLAMF7 baltymas, kad prisijungtų prie receptorių. Mokslininkai nustatė, kad šis privalomas įvykis sukėlė dramatiškus genų ekspresijos pokyčius.
Buvo sureguliuota beveik 600 genų - makrofagų SLAMF7 stimuliacijos parašas - kartu padidėjo keletas uždegiminių citokinų ir chemokinų, netgi viršijus vien IFN-γ sukeltą pakilimą. Pavyzdžiui, Šiuo metu TNF-α ir IL-6 lygis padidėja nuo pikomolinio iki nanomolinio. Be to, SLAMF7 išraiška dar labiau padidėjo, rodo teigiamą grįžtamojo ryšio ciklą.
Makrofagų susiejimas su SLAMF7 taip pat sukelia mieloidinį uždegiminį ciklą, be uždegimo paruošimo, kad jis stipriai reaguotų į mikrobinius TLR surišančius antigenus, arba į citokinus, su didžiuliu IL-1β išsiskyrimu. Iš kitos pusės, kai makrofagams suaktyvinti buvo naudojamas IFN-γ + LPS (stipri bakterijų molekulė) derinys, nebuvo pastebėtas SLAMF7 surišimui būdingas citokinų profilis. Tačiau, buvo dalinis panašumas tarp citokinų atsako ir genų ekspresijos profilio, kuris atsirado pirmą kartą naudojant IFN-γ, po to LPS ekspozicija.
Tyrėjai sakė, “ Ši SLAMF7 aktyvinimo programa remiasi ir yra atskiras žingsnis po pirminės makrofagų stimuliacijos IFN-γ ar kitais M1 diferenciacijos ir aktyvinimo veiksniais . “ Būdinga šios aktyvinimo programos sąlyga-superaktyvinta makrofagų uždegiminė būsena, kurią sukelia SLAMF7 įsitraukimas (SAM7)-yra pradinis makrofagų sustiprinimas IFN-γ, kai SLAMF7 yra labai sureguliuotas. Susiejimo įvykiai šiame receptoriuje dabar užbaigia pradėtų makrofagų aktyvavimą, kad susidarytų hiperuždegiminė makrofagų aktyvacijos būsena.
Atrodo, kad šį kelią palaiko ir dar labiau sustiprina autokrininio grįžtamojo ryšio kilpa, apimantis TNF-α, kuris greitai sukeltas (per dvi valandas) po SLAMF7 įsitraukimo ir laikui bėgant toliau kaupiasi. Įrodymai rodo, kad anti-TNF antikūnas perpus sumažina TNF-α ekspresiją, arba nutildant TNF receptorius siRNR.
Jie nustatė, kad vidutinis SLAMF7 aktyvinimo balas RA buvo beveik dvigubai didesnis nei asmenų, sergančių OA, tai rodo, kad šis receptorius yra glaudžiai susijęs su RA sergančių pacientų uždegimu.
Panašiai, sutapę makrofagų aktyvinimo genų profiliai buvo sukurti tiek sergant uždegimine žarnyno liga (IBD), tiek sergant COVID-19, palyginti su RA. Iš tiesų, Bronchosalveolinio plovimo skysčio ląstelės ir ląstelės iš uždegto žarnyno audinio COVID-19 ir IBD parodė tuos pačius makrofagų aktyvacijos parašus. Jie taip pat pažymėjo dvigubą SLAMF7 aktyvinimo balą uždegimo žarnyne, palyginti su normaliu žarnyno audiniu. Ir esant sunkiam COVID-19, rezultatas buvo šešis kartus didesnis palyginti su lengvu COVID-19. Visa tai rodo makrofagų aktyvinimo SAM7 programos dominavimą uždegiminėmis sąlygomis, ypač todėl, kad SLAMF7 receptorių nėra normaliuose audiniuose esančiuose makrofaguose.
Tyrinėti skirtingus makrofagų pogrupius, jie nustatė, kad uždegiminiai makrofagai turėjo labai aukštus aktyvinimo balus, palyginti su makrofagų rezidentais. Vėlgi, trys skirtingi makrofagų pogrupiai COVID-19 pacientams buvo pastebimai padidėję, dvi iš šių grupių parodė, kad išsivysto sunki liga. Įdomu tai, jie turėjo aukščiausius aktyvinimo balus, ir sunkiai sergančių COVID-19 pacientų makrofagai turėjo labai aukštą SLAMF7 ekspresijos lygį, kartu su labai dideliu daugelio kitų uždegiminių ir interferono sukeliamų žymenų ir receptorių kiekiu.
Trumpai tariant, SAM7 būsena gali būti pagrindinis hiperuždegiminio atsako, pastebėto sergant COVID-19 pneumonija, komponentas, taip pat RA, ir IBD. Tačiau, nuoseklus būdas, kuriuo toks aktyvinimas pasiekiamas, taip pat leidžia naudoti daugybę skirtingų terapinių priemonių. Tai apima JAK inhibitorius, tokius kaip ruksolitinibas, TNF-α inhibitoriai, arba SLAMF7 blokada, kurią atliko Elotuzumabas. Paskutinė kategorija yra ypač naudinga tuo, kad ji gali leisti selektyviai slopinti SAM7 programą, tuo pačiu leidžiant makrofagams atlikti įprastas esmines imunines funkcijas.
bioRxiv skelbia preliminarias mokslines ataskaitas, kurios nėra recenzuojamos ir todėl, neturėtų būti laikomas galutiniu, vadovauti klinikinei praktikai/su sveikata susijusiam elgesiui, arba traktuojama kaip nustatyta informacija.
 Jaunas kraujas senyvo amžiaus žmonėms atkuria gyvybingumą
Jaunas kraujas senyvo amžiaus žmonėms atkuria gyvybingumą
 Tyrimas fermentuotų daržovių vartojimą sieja su mažu mirtingumu nuo COVID-19
Tyrimas fermentuotų daržovių vartojimą sieja su mažu mirtingumu nuo COVID-19
 Kaimo ir miesto mikrobiota skiriasi nuo jauno amžiaus,
Kaimo ir miesto mikrobiota skiriasi nuo jauno amžiaus,
 „Wegovy“ svorio netekimo vaistas, patvirtintas FDA
„Wegovy“ svorio netekimo vaistas, patvirtintas FDA
 Miego kokybė gali būti vėlesnio Alzheimerio ligos tyrimo rodiklis
Miego kokybė gali būti vėlesnio Alzheimerio ligos tyrimo rodiklis
 Žarnyno bakterijos, susijusios su medžiagų apykaitos pokyčiais ir autizmu naujame tyrime
Žarnyno bakterijos, susijusios su medžiagų apykaitos pokyčiais ir autizmu naujame tyrime
 Nesandarus žarnynas ir skrydis į kosmosą - atskleistas mechanizmas
Naujas imituojamo mikrogravitacijos poveikio tyrimas, sąlyga, su kuria astronautai susiduria kosmose, trukdo žarnyno epitelio barjerui, o poveikis išlieka net ir po to, kai astronautas grįžta į įprast
Nesandarus žarnynas ir skrydis į kosmosą - atskleistas mechanizmas
Naujas imituojamo mikrogravitacijos poveikio tyrimas, sąlyga, su kuria astronautai susiduria kosmose, trukdo žarnyno epitelio barjerui, o poveikis išlieka net ir po to, kai astronautas grįžta į įprast
 Žarnyno mikrobiomas ir IBD - ryšys gali būti mityboje, sako tyrimas
Naujas tyrimas parodė įtikinamus įrodymus, kad uždegiminė žarnyno liga ar IBD yra glaudžiai susiję su žarnyno mikrobų aplinka, kurią galima pakeisti laikantis receptinės dietos. Žmogaus žarnyno mikrob
Žarnyno mikrobiomas ir IBD - ryšys gali būti mityboje, sako tyrimas
Naujas tyrimas parodė įtikinamus įrodymus, kad uždegiminė žarnyno liga ar IBD yra glaudžiai susiję su žarnyno mikrobų aplinka, kurią galima pakeisti laikantis receptinės dietos. Žmogaus žarnyno mikrob
 IBD yra daug dažnesnis nei tikėtasi,
ir ateityje tik didės Yra tris kartus daugiau žmonių, sergančių lėtiniu ir sekinančiu žarnyno sutrikimu, vadinamu uždegimine žarnyno liga (IBD), nei kada nors maniau, pagal naują tyrimą, pristatytą ši
IBD yra daug dažnesnis nei tikėtasi,
ir ateityje tik didės Yra tris kartus daugiau žmonių, sergančių lėtiniu ir sekinančiu žarnyno sutrikimu, vadinamu uždegimine žarnyno liga (IBD), nei kada nors maniau, pagal naują tyrimą, pristatytą ši