
MARTEDÌ, 11 giugno 2019 (HealthDay News) -- L'IB-Stim ha ricevuto l'approvazione alla commercializzazione dalla Food and Drug Administration statunitense come primo dispositivo medico utilizzato per alleviare il dolore addominale funzionale in pazienti di età compresa tra 11 e 18 anni con sindrome dell'intestino irritabile (IBS), l'agenzia ha annunciato venerdì.
Il dispositivo di sola prescrizione è composto da un piccolo stimolatore nervoso elettrico monouso posizionato dietro l'orecchio del paziente. Un chip alimentato a batteria nello stimolatore emette impulsi elettrici a bassa frequenza per stimolare continuamente alcuni rami dei nervi cranici. Lo stimolatore viene sostituito dopo cinque giorni e i pazienti possono utilizzare il dispositivo per un massimo di tre settimane consecutive in combinazione con altre terapie IBS.
L'approvazione all'immissione in commercio si è basata sui dati di uno studio clinico pubblicato su 50 pazienti di età compresa tra 11 e 18 anni con IBS. Ventisette pazienti sono stati trattati con il dispositivo e i restanti 23 pazienti hanno ricevuto un dispositivo placebo. I pazienti di entrambi i gruppi hanno riportato il dolore peggiore simile al basale e tutti i pazienti hanno continuato a somministrare dosi stabili di farmaci per trattare il dolore addominale cronico. Il 52% dei pazienti nel gruppo di trattamento ha sperimentato una riduzione di almeno il 30% del dolore abituale a tre settimane rispetto al 30% dei pazienti che hanno ricevuto il dispositivo placebo. Il 59% dei pazienti trattati ha riportato una riduzione di almeno il 30% del dolore peggiore rispetto al 26% dei pazienti che hanno ricevuto il placebo. I pazienti nel gruppo di trattamento hanno anche avuto un cambiamento maggiore nei punteggi compositi della frequenza del dolore Severità Durata dal basale alla settimana 3.
È stato segnalato un lieve fastidio all'orecchio in sei pazienti trattati e tre pazienti hanno riportato un'allergia all'adesivo nel sito di applicazione. La FDA rileva che l'IB-Stim è controindicato per i pazienti con emofilia, quelli con pacemaker cardiaci e quelli con diagnosi di psoriasi volgare.
L'approvazione dell'IB-Stim è stata concessa a Innovative Health Solutions.
Ulteriori informazioni

Copyright © 2019 HealthDay. Tutti i diritti riservati.
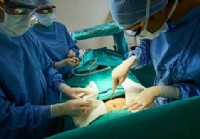 Che cos'è un'epaticodigiunostomia?
Cosè lepaticodigiunostomia? Unepaticodigiunostomia, o procedura Roux-en-Y, bypassa il dotto biliare per consentire ai succhi digestivi di drenare dal fegato direttamente nellintestino tenue. Il do
Che cos'è un'epaticodigiunostomia?
Cosè lepaticodigiunostomia? Unepaticodigiunostomia, o procedura Roux-en-Y, bypassa il dotto biliare per consentire ai succhi digestivi di drenare dal fegato direttamente nellintestino tenue. Il do
 Studio sullo svuotamento gastrico
Cosè uno studio di svuotamento gastrico? Il dolore addominale può essere un sintomo di un lento svuotamento gastrico. Il tipo più comune di studio di svuotamento gastrico è una procedura eseguita d
Studio sullo svuotamento gastrico
Cosè uno studio di svuotamento gastrico? Il dolore addominale può essere un sintomo di un lento svuotamento gastrico. Il tipo più comune di studio di svuotamento gastrico è una procedura eseguita d
 Carafate (sucralfato)
Presentazione di bruciori di stomaco:cibi da mangiare, cibi da evitare Miti sulle malattie digestive Rispondi al quiz GERD Cosè il Carafate (sucralfato)? Il carafato (sucralfato) è disponibile come
Carafate (sucralfato)
Presentazione di bruciori di stomaco:cibi da mangiare, cibi da evitare Miti sulle malattie digestive Rispondi al quiz GERD Cosè il Carafate (sucralfato)? Il carafato (sucralfato) è disponibile come