HÉTFŐ, 2015. augusztus 24. (HealthDay News) – Az Egyesült Államok Élelmiszer- és Gyógyszerügyi Hatósága a Promacta (eltrombopag) gyógyszerre vonatkozó jóváhagyását kiterjesztette a krónikus immunthrombocytopeniás purpurának (ITP) nevezett ritka vérbetegségben szenvedő egyéves és idősebb gyermekekre is.
Az ITP-t alacsony vérlemezkeszám jellemzi. Az ügynökség közleménye szerint a Promacta már engedélyezett a betegség kezelésére olyan gyermekek körében, akiknek nem volt kielégítő eredménye más gyógyszerekkel vagy lép eltávolítására irányuló műtéttel.
A vérlemezkék elősegítik a vérrögképződést, és az ITP-ben szenvedőknél vérzés alakulhat ki a bőr alatt vagy a nyálkahártyákon, például a szájban. Az FDA szerint a napi egyszeri Promacta célja a vérlemezke-termelés növelése.
A tabletta vagy por formájában kapható gyógyszert egy 159 ember bevonásával végzett vizsgálatban értékelték klinikailag. A Promacta-t szedők 62 százalékánál javult a vérlemezkeszám, szemben a placebót szedők 32 százalékával.
A Promacta leggyakoribb mellékhatásai a felső légúti fertőzés, a hasmenés, a hasi fájdalom, a bőrkiütés és a májenzimek szintjének emelkedése volt.
Az FDA szerint a gyógyszert nem értékelték egy évnél fiatalabb gyermekek körében.
A Promacta gyártója a Novartis, székhelye East Hannover, N.J.
-- Scott Roberts

Szerzői jog © 2015 HealthDay. Minden jog fenntartva.
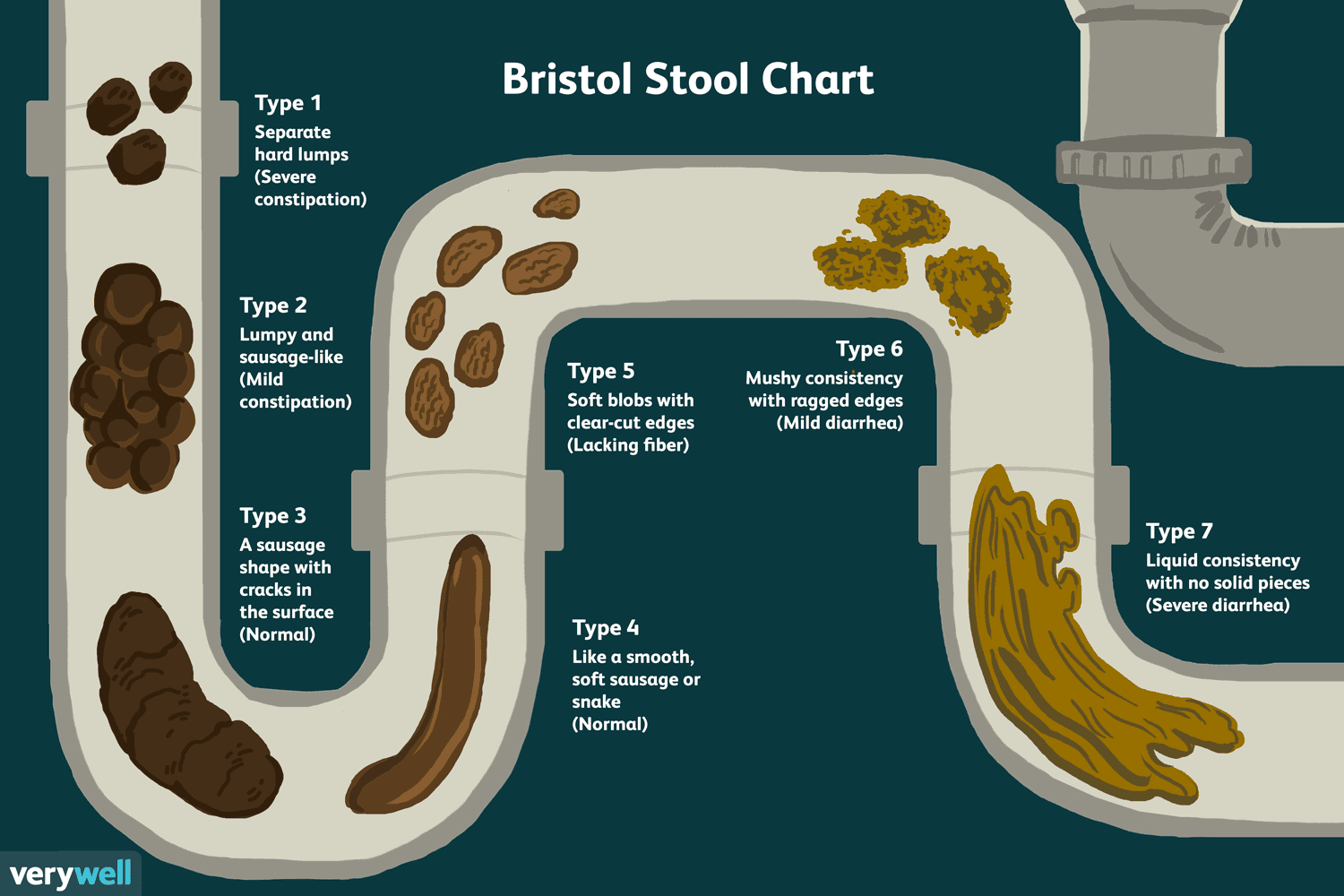 A bristoli székletdiagram áttekintése
A Bristoli székletdiagram egy olyan eszköz, amely az emberi széklet (kaka) meghatározására szolgál annak alakja és annak formája vagy lazasága alapján. Az eszközt a következőként is hallhatja: Bristo
A bristoli székletdiagram áttekintése
A Bristoli székletdiagram egy olyan eszköz, amely az emberi széklet (kaka) meghatározására szolgál annak alakja és annak formája vagy lazasága alapján. Az eszközt a következőként is hallhatja: Bristo
 Az immunsejtek helyreállítják a sérült bélrendszert IBD -s gyermekeknél
A folyóiratban megjelent új tanulmány szerint Gasztroenterológia , bizonyos típusú immunsejtek, amelyek szabályozzák a gyulladásos folyamatokat, sőt segítenek a bél normális működésének helyreállítá
Az immunsejtek helyreállítják a sérült bélrendszert IBD -s gyermekeknél
A folyóiratban megjelent új tanulmány szerint Gasztroenterológia , bizonyos típusú immunsejtek, amelyek szabályozzák a gyulladásos folyamatokat, sőt segítenek a bél normális működésének helyreállítá
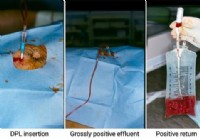 Hogyan történik a peritoneális mosás?
Mi az a peritoneális mosás? A diagnosztikai peritoneális mosást olyan instabil betegeknél alkalmazzák, akik súlyos fizikai traumát szenvedtek el. A peritoneális mosás egy ágy melletti eljárás a
Hogyan történik a peritoneális mosás?
Mi az a peritoneális mosás? A diagnosztikai peritoneális mosást olyan instabil betegeknél alkalmazzák, akik súlyos fizikai traumát szenvedtek el. A peritoneális mosás egy ágy melletti eljárás a