Et nyt papir i journalen Liv præsenterer en tidlig gennemgang af de virale faktorer, der er involveret i initiering og virkning af apoptose i inficerede celler.
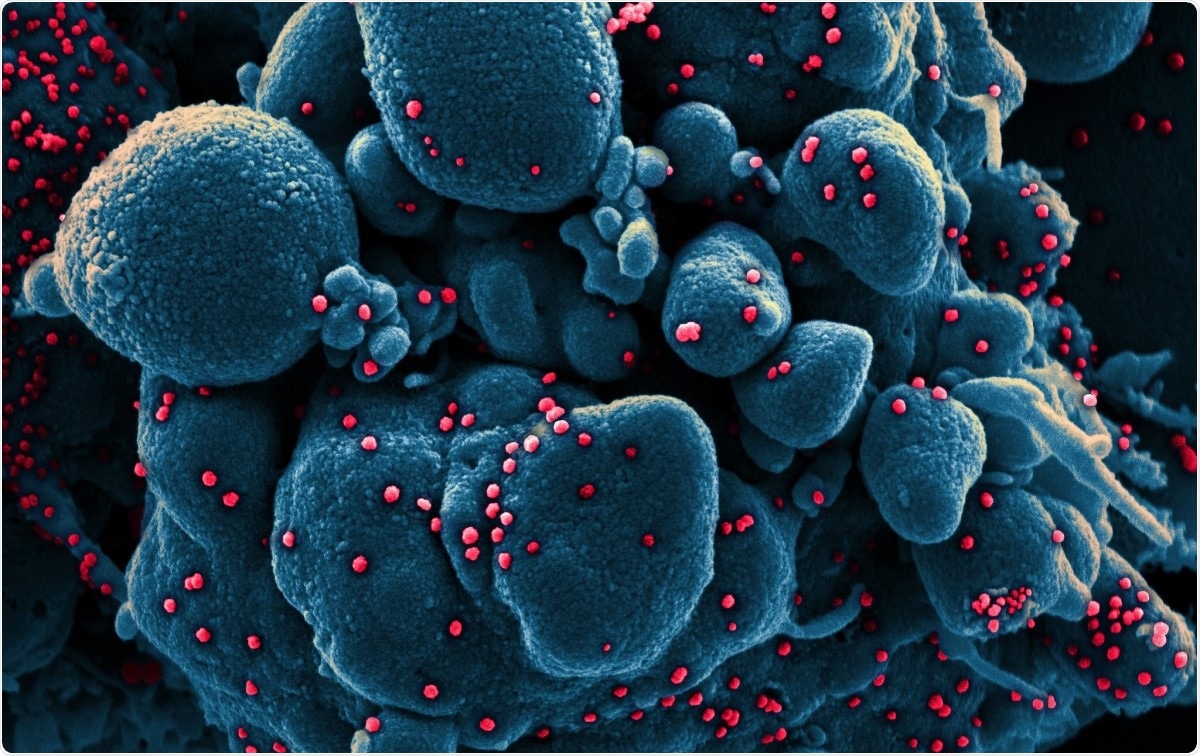 Farvet scanningselektronmikrograf af en apoptotisk celle (blå) inficeret med SARS-COV-2 viruspartikler (rød), isoleret fra en patientprøve. Billede taget på NIAID Integrated Research Facility (IRF) i Fort Detrick, Maryland. Billedkredit:NIAID / Flickr
Farvet scanningselektronmikrograf af en apoptotisk celle (blå) inficeret med SARS-COV-2 viruspartikler (rød), isoleret fra en patientprøve. Billede taget på NIAID Integrated Research Facility (IRF) i Fort Detrick, Maryland. Billedkredit:NIAID / Flickr Coronaviruses er blandt de største ribonukleinsyre (RNA) vira, der er identificeret hidtil. Deres genom er omkring 30 kb i længden, med fire strukturelle proteiner, og flere ikke-strukturelle og tilbehørsproteiner. De er klassificeret i alfa, beta, gamma- og delta -coronavirus.
Flere dyre- og menneskekoronavirus er hidtil blevet isoleret og forårsager for det meste luftvejs- eller gastrointestinale infektioner. Ligesom andre vira, de kaprer værtscellemaskineriet på alle stadier af deres replikation. Dette indebærer at ændre ekspressionen af forskellige værtsgener, herunder dem, der koder for værtsforsvar for at lette viral replikation.
For nylig, undersøgelser har vist, at tidligt i infektionen, coronavirus ændrer cellemetabolisme og øger celledødsfrekvensen. Dette sker, før adaptiv immunitet udløses, og dette kan indikere dets rolle i produktiv virusinfektion.
To af de vigtigste processer involveret i denne modulering er apoptose og cellecyklusmodifikation. Apoptose udløses af en række signalveje. Apoptose kan reducere virusudbredelse, men den modsatte virkning kan også forekomme - frigivelse af de infektiøse nyproducerede viruspartikler under lytisk infektion.
Celleveje, der aktiverer apoptose, kan udløses direkte af selve virusinfektionen eller indirekte via andre signalkaskader. Sidstnævnte modvirkes af tilstedeværelsen af virussen og rekruttere immunceller til infektionsstedet. Sluthændelsen er apoptose, forårsager betydelig skade på vævene ved lytisk infektion.
De virale komponenter i cellen kaldes patogenassocierede molekylære mønstre (PAMP'er) og genkendes af mønstergenkendelsesreceptorer (PRR'er). Disse reagerer ved at aktivere cytokiner og andre signalmolekyler, der opregulerer ekspression af interferon -gen.
En anden forsvarsmekanisme involverer genkendelse af viral nukleinsyre af værtsproteiner, der forbinder, ligesom PRR'erne, med adapterproteiner til aktivering af to centrale transkriptionsfaktorer, nemlig, NFĸB og IFN regulatorisk faktor 3 (IRF3). Disse translokeres til kernen og øger ekspressionen af type I -interferoner (IFN'er).
Disse binder til IFN-α/β-receptor (IFNAR), på tur, afværge et system af signaler, der involverer Janus kinase/signaltransducere og aktivatorer af transskription (JAK/STAT) pathway. Resultatet er opregulering af flere IFN-stimulerede gener (ISG'er).
Disse gener inaktiverer processen involveret i syntesen af celleproteiner og inducerer dermed celledød. En anden ISG, der er en spiller i denne proces med at lukke oversættelse, er kombinationen af 2 ′, 5′-oligoadenylatsyntetase (OAS) og RNase L.
Apoptose reguleres af flere pro- og anti-apoptotiske proteiner i værtscellen. En sådan proteinfamilie er familien Bcl-2 (B-cellelymfom-2), herunder faktorer, der forårsager porering af mitokondriemembranen og eventuel aktivering af caspaseenzymer, igangsætning af apoptose. Andre beskytter mod apoptose.
En anden familie er de mitogenaktiverede proteinkinaser (MAPK'er), som inkluderer ekstracellulær reguleret kinase 1/2 (ERK1/2), ERK5, p38, og c-Jun N-terminale kinaser (JNK). Den første opreguleres af vækstfaktorer og mitogener, de to sidste ved cellestress. JNK-vejen kan føre til aktivering af pro-apoptotiske gener eller kan interagere med Bcl-2-gener for at gøre det, eller kan aktivere andre transkriptionsfaktorer som 53 og p73.
To veje til apoptose er blevet identificeret, det ydre og det iboende. Førstnævnte formidles ved aktivering af dødsligander (FasL, TNF) om deres interaktion med deres respektive dødsreceptorer (DR'er). Caspase-8 er en vigtig inducer af apoptose i animalsk coronavirus, der virker via DR'er. Dette enzym, når den er aktiveret, kløver bud, et Bcl2 -protein, fører til frigivelse af mitokondrielt cytokrom c. Sidstnævnte er nøglen til dannelsen af apoptosomet med spaltning og aktivering af caspase 9.
Den iboende vej er baseret på permeabilisering af mitokondrielle ydre membraner og ses hovedsageligt med dyrevirus. Bcl2-proteiner som Bax og Bak favoriserer apoptose og er forpligtet til at udløse denne proces via den iboende eller mitokondriemedierede vej, sammen med caspase-9.
Mange dyrevirus forårsager aktivering af både ekstrinsiske og iboende veje, viser det indviklede netværk af signalveje involveret i apoptose.
Virale genomer koder ofte for gener, der er homologe til at være vært for anti-apoptotiske proteiner. Dette giver dem mulighed for at forsinke apoptose i de tidlige infektionsstadier og dermed generere et tilstrækkeligt udbytte af nye virioner. Andre virale proteiner kan forhindre transkription af nogle apoptotiske gener eller forårsage ændring af deres proteinprodukter, at undertrykke deres aktivitet.
Induktion af apoptose med virale proteiner kan indebære afslutning af cap-afhængig translation i værtsceller, fremkalder apoptose, som set med poliovirus. I tilfælde af hepatitis C -virus, det virale NS3-protein interagerer med caspase-8, at udløse celledød.
Den nuværende anmeldelse er fokuseret på at identificere pro-apoptotiske mekanismer udløst af dyrekoronavirus. For eksempel, Porcine Epidemic Diarrhea Virus (PEDV) udløser ændringer i ekspressionen af 14 gener involveret i caspase-uafhængig apoptose for at fremme dets replikation, samt at producere de karakteristiske træk ved sygdom.
En anden måde, hvorpå apoptose er involveret i viral replikation, er ved at aktivere caspase, som er påkrævet til spaltning af det virale nucleocapsid (N) protein under denne proces. Dette er tilfældet med den overførbare gastroenteritisvirus (TGEV), som aktiverer MAPK -familien, samt FasL- og mitokondrier-induceret apoptose. Denne proces inkluderer også nedregulering af værtsmikroRNA'er, der undertrykker den mitokondrielle apoptotiske vej.
Betacoronavirus, såsom murin hepatitisvirus (MHV), fremkalder apoptose. Denne virus viser kuvertprotein (E) -induceret apoptose, igen via caspase -aktivering. I dette tilfælde, apoptose ser ud til at være beskyttende mod virionproduktion.
Med den porcine hæmagglutinerende encephalomyelitis virus (PHEV), celledød medieres af DR'er og de mitokondriemedierede veje, involverer caspase-8 og caspase-9, som initiativtagere, og caspase-3, som en effektor af apoptose.
Tilsvarende gamma- og delta-coronavirus viser kompleks induktion af cellulære signalveje i værtscellen, hvilket fører til modulering af apoptose. Dermed, mange virale proteiner modulerer værtscelleveje for at fremme viral replikation og sygdomsegenskaber.
Den kendsgerning, at apoptose opstår efter infektion af flere værter med en række coronavirus, fører til den konklusion, at det er et fælles træk ved infektion med mennesker og dyr coronavirus og har til formål at favorisere formering.
Med den tidligere alvorlige akutte respiratoriske syndrom coronavirus (SARS-CoV), 7a-proteinet danner et kompleks med Bcl-XL-protein eller andre pro-overlevelsesfaktorer, inaktivere dem og dermed tillade apoptose at fortsætte via caspase-3-aktivering. Den 3CL-lignende protease (3CLpro) aktiverer også både caspase-3 og caspase-9 for at inducere apoptose i cellekultur.
Både SARS-CoV og de i øjeblikket cirkulerende SARS-CoV-2-vira har ORF3a-proteinet, der udløser celledød via caspaseaktivering i den ekstrinsiske vej gennem DR'er.
En lignende rolle er endnu ikke blevet vist for virale proteiner ved infektioner med animalsk coronavirus. Imidlertid, med PEDV, S1 -underenheden af piggproteinet, og det ikke-strukturelle protein 1 (NSP1), er blevet foreslået at være initiator og effektor af celledød, henholdsvis, baseret på nylige forsøg.
Flere undersøgelser kan hjælpe med at forstå, hvordan disse veje fungerer i andre coronavirus. Den nuværende videnstilstand kan indikere nytten af at målrette denne vej til håndtering af coronavirus -infektioner.
 Gedemælkbaseret formel god til spædbørns tarmsundhed
Gedemælkbaseret formel god til spædbørns tarmsundhed
 Kvinder født med kejsersnit har større risiko for fedme og diabetes
Kvinder født med kejsersnit har større risiko for fedme og diabetes
 Edderkoppespift kan hjælpe med at stoppe smerter ved irritabel tarm
Edderkoppespift kan hjælpe med at stoppe smerter ved irritabel tarm
 Visse bakteriearter kan øge hiv -risikoen hos kvinder,
Visse bakteriearter kan øge hiv -risikoen hos kvinder,
 Genetisk tilpasning af tarmbakterier reducerer risikoen for tyktarmskræft hos mus finder undersøgelse
Genetisk tilpasning af tarmbakterier reducerer risikoen for tyktarmskræft hos mus finder undersøgelse
 Stærkt mikrobiom i det tidlige liv forbundet med færre luftvejsinfektioner
Stærkt mikrobiom i det tidlige liv forbundet med færre luftvejsinfektioner
 Proteinsendinger fra humant mikrobiom kaster lys over menneskers sundhed
Menneskekroppen er blevet undersøgt i århundreder, men der er stadig mysterier, der endnu ikke skal udspille sig. For eksempel, det blev opdaget, at der lever billioner af bakterier inde i kroppen, de
Proteinsendinger fra humant mikrobiom kaster lys over menneskers sundhed
Menneskekroppen er blevet undersøgt i århundreder, men der er stadig mysterier, der endnu ikke skal udspille sig. For eksempel, det blev opdaget, at der lever billioner af bakterier inde i kroppen, de
 Økologiske æbler har probiotiske egenskaber
Et æble om dagen ... siger det gamle ordsprog. Det ser ud til, at alle er enige, at dømme efter nummer 1 -positionen, som æbler holder blandt frugter verden over, med 83 millioner æbler hvert år. En
Økologiske æbler har probiotiske egenskaber
Et æble om dagen ... siger det gamle ordsprog. Det ser ud til, at alle er enige, at dømme efter nummer 1 -positionen, som æbler holder blandt frugter verden over, med 83 millioner æbler hvert år. En
 SARS-CoV-2-infektion forlænger viral shedding og lymfocyttab hos patienter med kræft
Patienter med kræft har en mere udfordrende tid med infektioner under behandling-hvilket placerer dem som en høj risiko for alvorlig COVID-19 sygdom og død. Imidlertid, hvordan det alvorlige akutte re
SARS-CoV-2-infektion forlænger viral shedding og lymfocyttab hos patienter med kræft
Patienter med kræft har en mere udfordrende tid med infektioner under behandling-hvilket placerer dem som en høj risiko for alvorlig COVID-19 sygdom og død. Imidlertid, hvordan det alvorlige akutte re