ВТОРНИК, 22 сентября 2015 г. (HealthDay News). Комбинированная таблетка Lonsurf (трифлуридин и типирацил) была одобрена Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США для лечения распространенного рака толстой кишки у людей, которые не реагируют на другие виды лечения, сообщает агентство. говорится во вторник в пресс-релизе.
Рак толстой кишки является третьей наиболее распространенной причиной рака кожи в Соединенных Штатах, сообщает FDA со ссылкой на Национальный институт рака США. Это по-прежнему вторая по распространенности причина смерти от рака после рака легких, хотя показатели снижаются, отчасти из-за более широкого скрининга на это заболевание.
Lonsurf был оценен в клинических испытаниях с участием около 800 человек с ранее леченным распространенным колоректальным раком. Те, кто принимал Лонсурф, жили в среднем более 7 месяцев по сравнению с 5,3 месяца для тех, кто принимал плацебо.
К наиболее распространенным побочным эффектам препарата относятся анемия, снижение количества лейкоцитов, борющихся с инфекциями, снижение количества тромбоцитов, слабость, утомляемость, тошнота, потеря аппетита, диарея, боль в животе и лихорадка.
FDA заявило, что из-за возможности серьезного снижения производства клеток крови и тромбоцитов врачам настоятельно рекомендуется проверять кровь пользователей перед началом каждого цикла лечения. Врачи также советуют предупреждать женщин детородного возраста о потенциальном вреде для развивающегося плода. Агентство предупредило, что женщины, использующие Lonsurf, не должны кормить грудью.
Lonsurf производится компанией Taiho Oncology, расположенной в Принстоне, штат Нью-Джерси.
-- Скотт Робертс

Авторское право © HealthDay, 2015. Все права защищены.
 Ученые обнаружили гены, ответственные за болезнь Крона и язвенный колит
Ученые обнаружили гены, ответственные за болезнь Крона и язвенный колит
 Синдром повышенной кишечной проницаемости не только страшен, но и чрезвычайно опасен для вашего здоровья
Синдром повышенной кишечной проницаемости не только страшен, но и чрезвычайно опасен для вашего здоровья
 Заразен ли гепатит? Симптомы, передача, лечение
Заразен ли гепатит? Симптомы, передача, лечение
 Электронная таблетка для обнаружения газов для диагностики желудочно-кишечных заболеваний
Электронная таблетка для обнаружения газов для диагностики желудочно-кишечных заболеваний
 вздутие живота и расстройства пищеварения
вздутие живота и расстройства пищеварения
 Что такое лапароскопическая правосторонняя колэктомия?
Что такое лапароскопическая правосторонняя колэктомия?
 Касл Коннолли назвал Р. Стивена Рашбаума лучшим документом 2016 года
Касл Коннолли назвал доктора Стивена Рашбаума лучшим врачом 2016 года Стивен Рашбаум , доктор медицины Выбранный Castle Connolly Top Doc в качестве лучшего врача, доктор Стивен Рашбаум попадает в кат
Касл Коннолли назвал Р. Стивена Рашбаума лучшим документом 2016 года
Касл Коннолли назвал доктора Стивена Рашбаума лучшим врачом 2016 года Стивен Рашбаум , доктор медицины Выбранный Castle Connolly Top Doc в качестве лучшего врача, доктор Стивен Рашбаум попадает в кат
 Невидимый лабораторный халат:5 мифов о маркетинге
Вы носите невидимый лабораторный халат? Если вы практикующий врач (или собираетесь им стать), найдите секунду и посмотрите на свой наряд прямо сейчас… что вы видите? Что ж, вы не увидите невидимого
Невидимый лабораторный халат:5 мифов о маркетинге
Вы носите невидимый лабораторный халат? Если вы практикующий врач (или собираетесь им стать), найдите секунду и посмотрите на свой наряд прямо сейчас… что вы видите? Что ж, вы не увидите невидимого
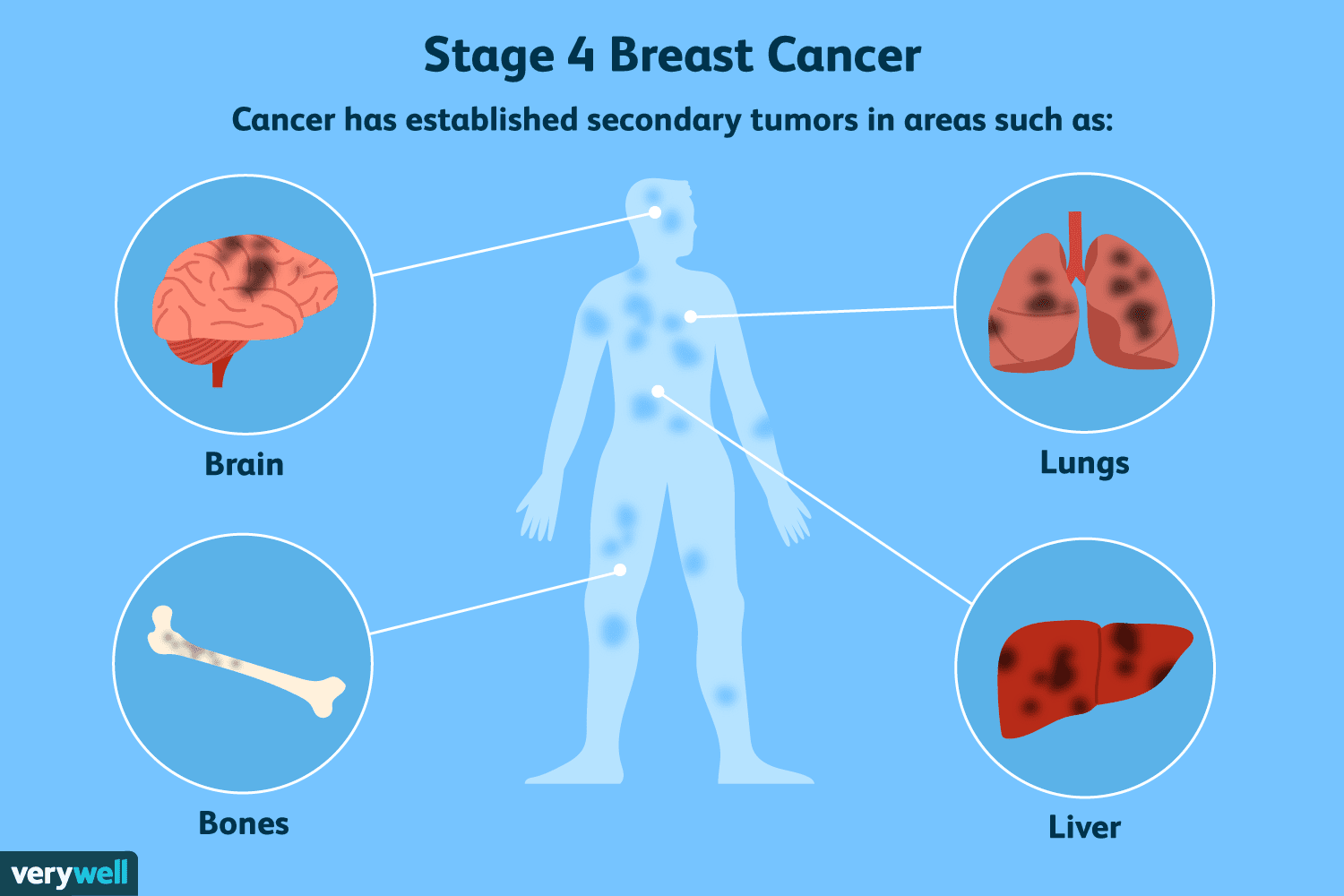 Обзор рака молочной железы 4 стадии
Стадия 4 — самая запущенная форма рака молочной железы. Его также называют метастатическим раком молочной железы, поскольку злокачественное новообразование распространяется (метастазирует) из молочной
Обзор рака молочной железы 4 стадии
Стадия 4 — самая запущенная форма рака молочной железы. Его также называют метастатическим раком молочной железы, поскольку злокачественное новообразование распространяется (метастазирует) из молочной