O desenvolvimento eficaz de medicamentos deve agilizar o número de medicamentos candidatos que entram no ciclo, para reduzir o custo e o tempo do processo. Estudos recentes recomendam a integração de uma variedade de técnicas para desenvolver canais de pesquisa e desenvolvimento (P&D), bem como o uso de dados genéticos para identificar as novas drogas de sucesso mais provável. Proteômica e transcriptômica estão entre os campos mais valiosos para esse fim.
Atualmente, existem mais de 150 ensaios clínicos testando drogas que são consideradas possivelmente eficazes para aumentar a sobrevida e melhorar a recuperação de pacientes com COVID-19. Estes incluem hidroxicloroquina, cloroquina, e baricitinibe.
Outra via de coleta de evidências sobre drogas potencialmente úteis contra COVID-19 é encontrar as proteínas do hospedeiro que facilitam a entrada viral e a infecção, e examinando a possibilidade de reaproveitar alvos de drogas anteriores no SARS-CoV para combater o vírus atual, síndrome respiratória aguda grave coronavírus 2 (SARS-CoV-2).
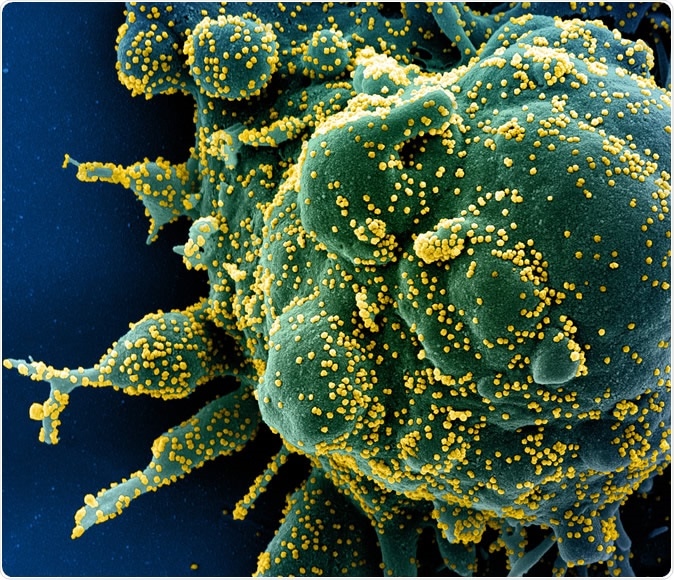 Novo Coronavírus SARS-CoV-2 Micrografia eletrônica de varredura colorida de uma célula apoptótica (verde) fortemente infectada com partículas do vírus SARS-COV-2 (amarelo), isolado de uma amostra de paciente. Imagem capturada no NIAID Integrated Research Facility (IRF) em Fort Detrick, Maryland. Crédito:NIAID
Novo Coronavírus SARS-CoV-2 Micrografia eletrônica de varredura colorida de uma célula apoptótica (verde) fortemente infectada com partículas do vírus SARS-COV-2 (amarelo), isolado de uma amostra de paciente. Imagem capturada no NIAID Integrated Research Facility (IRF) em Fort Detrick, Maryland. Crédito:NIAID Um estudo recente descobriu mais de 330 proteínas do hospedeiro humano que são necessárias para o vírus infectar humanos. Estes interagem com 26 proteínas virais. Isso poderia ajudar a promover a P&D ao longo da primeira rota.
O segundo método foi usado por alguns estudos, que produziram 59 genes de camundongo que estão ligados à infecção anterior por SARS-CoV. Entre estes, existem 44 que possuem equivalentes no genoma humano. Ao bloquear as interações de proteína humana-viral, pode ser possível direcionar os mecanismos de infecção viral de forma mais eficaz com uma menor chance de resistência aos medicamentos, em comparação com o direcionamento direto do vírus.
O principal problema dessa abordagem é o perigo de produzir inadvertidamente outros efeitos que podem piorar doenças complexas - ou até mesmo beneficiá-las. O estudo atual tem como objetivo avaliar como esses alvos de drogas podem afetar o funcionamento do corpo humano, com base na compreensão da genética subjacente.
Os pesquisadores usaram o protocolo para priorização de medicamentos, que eles desenvolveram com sucesso anteriormente, para testar 353 alvos de drogas que possivelmente interagem com o vírus. Eles queriam observar como essas drogas causavam outros efeitos visíveis da infecção, bem como como eles alcançaram os efeitos pretendidos e não pretendidos em doenças complexas.
Eles primeiro construíram um atlas de doenças exibindo as proteínas e genes humanos que participam da entrada viral. Isso foi por meio de estudos de randomização de Mendel, fornecendo mais de 372, 000 previsões únicas de como a droga afeta uma doença. Isso foi baseado na proteômica do plasma, bem como na transcriptômica específica do tecido.
Como resultado, eles foram capazes de avaliar como essas 353 drogas potenciais podem agir em 49 fenótipos de infecção viral, como eles podem afetar mais de 500 doenças complexas, e alterar 72 fenótipos da doença. Esses resultados foram avaliados em relação aos dados de ensaios de drogas, bem como o genoma drogável, para identificar os principais medicamentos com maior possibilidade de reaproveitamento, e o mínimo de efeitos colaterais.
Eles criaram uma plataforma online de acesso aberto que contém os resultados de todos os testes, de modo a permitir que qualquer pessoa examine os resultados de qualquer uma das drogas rapidamente.
O atlas de interações medicamentos-alvo-doença fornece mais de 370, 000 associações de doenças-alvo em 11 tecidos que são relevantes no cenário COVID-19. Deles, 833 tinham fortes evidências de imagens de ressonância magnética dos 11 tecidos. 726 destes também mostraram colocalização robusta, para uma probabilidade de colocalização de mais de 70%. Estas foram as descobertas mais robustas do estudo.
A importância de detectar tais associações é a capacidade de realizar análises de como a expressão de certos alvos afeta doenças específicas, dependendo do tecido. Por exemplo, os efeitos dos alvos da droga na doença de Crohn, hipertensão, distúrbios atópicos, e diabetes pode ser avaliada. Em qualquer lugar de 11-17 dos genes-alvo tiveram associações com essas quatro doenças, com base em qual tecido foi estudado.
Em segundo lugar, os alvos da droga foram analisados quanto à associação com 49 fenótipos de infecção viral. Havia duas associações fortes, nomeadamente, o gene NEU1 com hepatite crônica e o gene DPY19L1 com enterite viral. Havia também três associações menos fortes, mas sugestivas, como o gene JAK2 com hepatite crônica.
Em terceiro lugar, o estudo mostrou 45 formas potenciais nas quais as proteínas podem afetar características da doença e 430 associações semelhantes com a expressão de mRNA. Entre estes, havia 95 alvos associados a 105 doenças ou expressões de doenças. O gene JAK2, por exemplo, está associado a nove fenótipos de doenças, variando de atopia a obesidade, o que sugere ações potencialmente pleiotrópicas para este gene.
Finalmente, eles encontraram 249 associações em que o alvo da droga afetava o fenótipo de uma doença de maneira diferente, dependendo do tecido analisado. Entre eles estavam 52 genes únicos expressos em 7 tecidos para afetar 47 doenças únicas.
Houve 29 efeitos dependentes de tecido fortemente associados do alvo da droga sobre a doença em mais de um único tecido, entre os quais apenas dois falharam em mostrar a mesma direção de efeito quando expressa no sangue, bem como em uma variedade de outros tecidos.
Por exemplo, o gene DHODH afeta o colesterol de lipoproteína de baixa densidade (LDL). Uma droga sendo comercializada contra níveis elevados de LDL, chamado Leflunomida, atua inibindo esse gene. A leflunomida também está sendo considerada como uma terapia COVID-19.
A análise mostrou que esta droga se expressa apenas em relação ao LDL sem muitas outras ações diversas, em um amplo espectro de tecidos do pulmão ao cólon.
Os pesquisadores avaliaram as 726 associações encontradas por RM entre o alvo e a doença, usando dados de ensaios clínicos, bem como a evidência putativa de que eles causaram diferentes efeitos fenotípicos em uma variedade de tecidos, para criar as associações mais drogáveis. 499 deles eram pares únicos de alvo e doença, com os demais sendo observados em mais de um tecido.
Eles criaram quatro classes de pontuação, como a pontuação ômicas, a pontuação do julgamento, a pontuação de drogabilidade, e a pontuação de infecção. Cada pontuação foi escalada de 1 a 100. Houve pontuações altas para 2 das 499 associações em 3 de 4 classes, o que os tornou os alvos com a maior prioridade de desenvolvimento. 77 pontuações altas em duas classes e 97 em uma. Os 323 restantes tiveram pontuações universalmente baixas e, portanto, são considerados os alvos de medicamentos de prioridade mais baixa.
Alguns alvos incluem o gene ITGB5 que é direcionado pela droga Cilengitide, que se destinava a glioblastomas e tumores semelhantes. Suas pontuações altas e o perfil genético sugerem que ele tem potencial para reduzir a pressão alta. Entre os 5 primeiros, todos careciam de fortes associações com condições como arritmias cardíacas, o que pode afetar seu uso no COVID-19.
Por outro lado, o gene TLR9, que é direcionado pela droga hidroxicloroquina tem pontuações altas em duas categorias, mas uma pontuação baixa nas outras duas. Nenhuma evidência clínica foi acumulada quanto ao benefício antiviral ou clínico de uma combinação deste medicamento com azitromicina. Além disso, este gene pode aumentar a chance de acidente vascular cerebral embólico, asma, e certas condições imunológicas.
O estudo foi capaz de promover a priorização de alvos de medicamentos de três maneiras:examinando os problemas de segurança que podem surgir da reutilização de medicamentos para o tratamento com COVID-19; identificar alvos de drogas promissores; e descobrir como o alvo da droga afeta o fenômeno humano em diferentes tecidos.
Usando essa abordagem, uma droga potencial, Baricitinibe, está sendo testado quanto à sua eficácia no COVID-19. Acredita-se que iniba a proteína JAK2, e assim reduzir a inflamação sistêmica. Contudo, o estudo atual propôs que também poderia causar hepatite crônica. Na verdade, a literatura sugere que a hepatite B é reativada após o tratamento com o inibidor de JAK 2 ruxolitinibe.
Os três medicamentos de alto potencial deste estudo incluem o medicamento imunossupressor Leflunomida, usado na artrite reumatóide, entre outras condições, e Cilengitide. O primeiro tem atividade antiviral contra vários vírus, e o estudo atual também sugere que tem propriedades hipolipemiantes, enquanto o último tem atividade anti-hipertensiva, possivelmente.
Finalmente, alguns desses alvos são expressos em vários tecidos para produzir o mesmo fenótipo, mas outros mostram mudança de expressão específica para o tecido.
Embora existam algumas limitações, o estudo fornece um canal para estudo de genética estatística e uma plataforma de acesso aberto para organizar alvos de drogas contra COVID-19 em ordem de prioridade. Os estudos de associação do genoma (GWAS) podem melhorar ainda mais a qualidade dos dados, tornando-o ainda mais útil na descoberta de alvos de drogas promissores entre drogas potencialmente reutilizadas.
medRxiv publica relatórios científicos preliminares que não são revisados por pares e, Portanto, não deve ser considerado conclusivo, orientar a prática clínica / comportamento relacionado à saúde, ou tratadas como informações estabelecidas.
 Os coronavírus humanos precisam de materiais orgânicos para uma transferência eficiente entre as superfícies
Os coronavírus humanos precisam de materiais orgânicos para uma transferência eficiente entre as superfícies
 A vibração de todo o corpo ajuda a reduzir a inflamação,
A vibração de todo o corpo ajuda a reduzir a inflamação,
 Maçãs orgânicas têm propriedades probióticas
Maçãs orgânicas têm propriedades probióticas
 A disbiose na microbiota intestinal pode causar infecção secundária grave em pacientes com COVID-19
A disbiose na microbiota intestinal pode causar infecção secundária grave em pacientes com COVID-19
 Alimentos que estimulam o intestino podem acabar com a desnutrição infantil em todo o mundo
Alimentos que estimulam o intestino podem acabar com a desnutrição infantil em todo o mundo
 Destaques e principais conclusões do Boston Bacterial Meeting (BBM) 2019
Destaques e principais conclusões do Boston Bacterial Meeting (BBM) 2019
 Desinfetantes domésticos podem contribuir para o risco de obesidade em crianças
Pesquisadores canadenses demonstraram que os produtos de limpeza doméstica comumente usados podem estar deixando as crianças acima do peso, causando alterações em sua microflora intestinal. p
Desinfetantes domésticos podem contribuir para o risco de obesidade em crianças
Pesquisadores canadenses demonstraram que os produtos de limpeza doméstica comumente usados podem estar deixando as crianças acima do peso, causando alterações em sua microflora intestinal. p
 Micróbios intestinais em vespas ajudam a superar os pesticidas
Um estudo intrigante publicado em fevereiro de 2020 na revista Hospedeiro celular e micróbio relata que quando as vespas são expostas à atrazina, um pesticida comumente usado, o microbioma intestina
Micróbios intestinais em vespas ajudam a superar os pesticidas
Um estudo intrigante publicado em fevereiro de 2020 na revista Hospedeiro celular e micróbio relata que quando as vespas são expostas à atrazina, um pesticida comumente usado, o microbioma intestina
 Higiene oral e severidade de COVID-19 - a conexão
Pesquisadores britânicos descobriram uma ligação entre a má higiene oral e a gravidade da doença COVID-19 causada por infecção por síndrome respiratória aguda grave por coronavírus 2 (SARS-CoV-2). O e
Higiene oral e severidade de COVID-19 - a conexão
Pesquisadores britânicos descobriram uma ligação entre a má higiene oral e a gravidade da doença COVID-19 causada por infecção por síndrome respiratória aguda grave por coronavírus 2 (SARS-CoV-2). O e