Effektiv Drogenentwécklung muss d'Zuel vun de Kandidatdrogen, déi an den Zyklus erakommen, streamlinéieren, d'Käschte an d'Zäit vum Prozess erofzesetzen. Rezent Studien empfeelen eng Vielfalt vun Techniken z'integréieren fir Pipelines fir Fuerschung an Entwécklung (R&D) z'entwéckelen souwéi genetesch Donnéeën ze benotzen fir déi wahrscheinlech erfollegräich nei Medikamenter z'identifizéieren. Proteomics an Transkriptomik gehéieren zu de wäertvollste Felder fir dëst Enn.
Am Moment, et ginn iwwer 150 klinesch Studien, déi Medikamenter testen, déi geduecht gi wier méiglecherweis effektiv fir d'Iwwerliewe ze stäerken an d'Erhuelung vun de COVID-19 Patienten ze verbesseren. Dës enthalen Hydroxychloroquin, Chlorochin, a Baricitinib.
En anere Wee fir Beweiser ze sammelen iwwer potenziell nëtzlech Medikamenter géint COVID-19 ass andeems Dir d'Hostproteine fënnt, déi viral Entrée an Infektioun erliichteren, an andeems d'Méiglechkeet ënnersicht gëtt fréier Medikamentziler am SARS-CoV nei opzebauen fir den aktuelle Virus ze bekämpfen, schwéier akut Atmungssyndrom Coronavirus 2 (SARS-CoV-2).
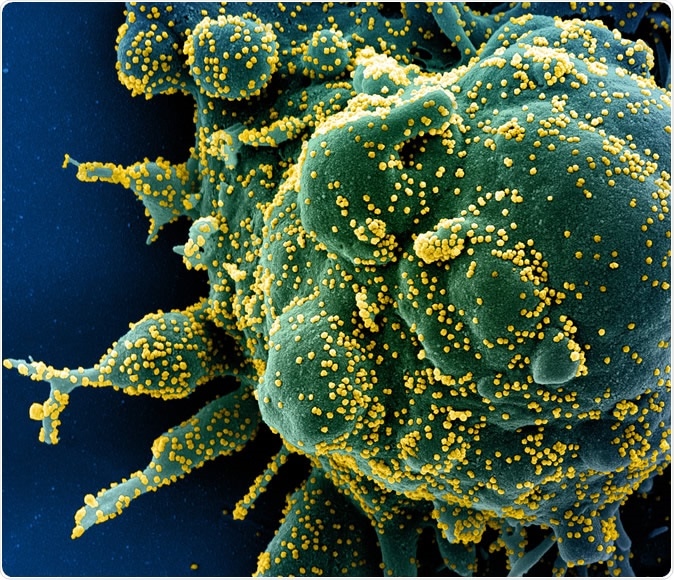 Roman Coronavirus SARS-CoV-2 Faarweg Scannenelektronmikrograph vun enger apoptotescher Zell (gréng) schwéier infizéiert mat SARS-COV-2 Viruspartikelen (giel), isoléiert vun engem Patientprobe. Bild ageholl an der NIAID Integrated Research Facility (IRF) zu Fort Detrick, Maryland. Kreditt:NIAID
Roman Coronavirus SARS-CoV-2 Faarweg Scannenelektronmikrograph vun enger apoptotescher Zell (gréng) schwéier infizéiert mat SARS-COV-2 Viruspartikelen (giel), isoléiert vun engem Patientprobe. Bild ageholl an der NIAID Integrated Research Facility (IRF) zu Fort Detrick, Maryland. Kreditt:NIAID Eng rezent Studie huet iwwer 330 mënschlech Hostproteine fonnt déi noutwendeg si fir de Virus Mënschen z'infizéieren. Dës interagéieren mat 26 virale Proteinen. Dëst kéint hëllefen R&D laanscht déi éischt Streck ze förderen.
Déi zweet Method gouf vun e puer Studien benotzt, déi 59 Mausgenen erginn hunn, déi mat der fréierer SARS-CoV Infektioun verbonne sinn. Ënnert dësen, et gi 44 déi Äquivalente am mënschleche Genom hunn. Duerch d'Blockéierung vu viral-mënschleche Protein Interaktiounen, et kann méiglech sinn viral Infektiounsmechanismen méi effektiv ze zielen mat enger niddereger Chance fir Drogenresistenz, am Verglach mam direkt viséieren vum Virus.
E primär Thema mat dëser Approche ass d'Gefor vun onbedéngt aner Effekter ze produzéieren déi komplex Krankheetskonditioune verschlechtere kënnen - oder souguer dovu profitéieren. Déi aktuell Studie zielt fir ze bewäerten wéi dës Medikamentziler de Fonctionnement vum mënschleche Kierper beaflosse kënnen, baséiert op engem Verständnis vun der ënnerierdescher Genetik.
D'Fuerscher hunn de Protokoll benotzt fir Medikamenter Prioritéit, déi se erfollegräich virdru entwéckelt hunn, fir 353 Medikamentziler ze testen déi méiglecherweis mam Virus interagéieren. Si wollte observéieren wéi dës Medikamenter aner no baussen erkennbar Effekter vun der Infektioun verursaacht hunn, wéi och wéi se béid virgesinn an onbedéngt Effekter op komplex Krankheeten erreecht hunn.
Si hunn als éischt e Krankheetatlas konstruéiert mat de mënschleche Proteinen a Genen, déi un der viraler Entrée deelhuelen. Dëst war iwwer Mendelian Randomiséierungsstudien, bitt iwwer 372, 000 eenzegaarteg Prognosen iwwer wéi d'Droge eng Krankheet beaflosst. Dëst war baséiert op Plasma Proteomik souwéi Tissu-spezifesch Transkriptomik.
Als Resultat vun, si konnten evaluéieren wéi dës 353 potenziell Medikamenter a 49 Phänotypen vun enger viraler Infektioun kéinte handelen, wéi se iwwer 500 komplex Krankheeten beaflosse kënnen, an 72 Phänotypen vun der Krankheet z'änneren. Dës Resultater goufen bewäert mat Respekt un Daten aus Medikamentstudien, wéi och den druggable Genom, fir déi Top Medikamenter ze identifizéieren mat der héchster Méiglechkeet fir nei ze benotzen, an déi mannst Nebenwirkungen.
Si hunn eng Online Open-Access Plattform erstallt déi d'Resultater vun allen Tester enthält, sou datt jidderengem erlaabt d'Resultater fir iergendeng vun den Drogen séier z'iwwerpréiwen.
Den Atlas vun Drogenziel-Krankheet Interaktiounen liwwert iwwer 370, 000 Zil-Krankheet Associatiounen an 11 Stoffer, déi relevant sinn am COVID-19 Szenario. Vun deenen, 833 hat staark Beweiser vu MR Imaging vun den 11 Stoffer. 726 vun dësen hunn och robust Kolokaliséierung gewisen, fir eng Kolokaliséierung Wahrscheinlechkeet vun iwwer 70%. Dëst waren déi robustst Resultater vun der Studie.
D'Wichtegkeet fir sou Associatiounen z'entdecken ass d'Fäegkeet Analysen ze maachen wéi den Ausdrock vu bestëmmten Ziler spezifesch Krankheeten beaflosst, ofhängeg vum Tissu. Zum Beispill, d'Auswierkunge vun den Drogenziler op Crohn's Krankheet, Hypertonie, atopesch Stéierungen, an Diabetis kéint bewäert ginn. Iwwerall vun 11-17 vun den Zilgenen haten Associatiounen mat dëse véier Krankheeten, baséiert op deem Tissu studéiert gouf.
Zweetens, d'Drogenziler goufen analyséiert fir Associatioun mat 49 virale Infektiounsphenotypen. Et waren zwou staark Associatiounen, nämlech, den NEU1 Gen mat chronescher Hepatitis an den DPY19L1 Gen mat viraler Enteritis. Et waren och dräi manner staark awer suggestiv Associatiounen, wéi de JAK2 Gen mat chronescher Hepatitis.
Drëttens, d'Studie huet 45 potenziell Weeër gewisen, op wéi d'Proteine Krankheetseigenschaften a 430 ähnlech Associatioune mam mRNA Ausdrock beaflosse kënnen. Ënnert dësen, et war 95 Zil verbonne mat 105 Krankheeten oder Krankheet Ausdréck. De JAK2 Gen, zum Beispill, ass mat néng Krankheetphenotypen verbonnen, rangéiert vun Atopie zu Adipositas, wat potenziell pleiotrop Aktiounen fir dëst Gen proposéiert.
Endlech, si hu 249 Associatiounen fonnt, wou d'Droge Zil e Krankheetphenotyp anescht beaflosst ofhängeg vum analyséierten Tissu. Ënnert dësen waren 52 eenzegaarteg Genen ausgedréckt a 7 Stoffer fir 47 eenzegaarteg Krankheeten ze beaflossen.
Et waren 29 staark assoziéiert Tissu-ofhängeg Effekter vum Medikamentziel op d'Krankheet a méi wéi engem eenzegen Tissu, ënner deenen nëmmen zwee net déiselwecht Effektrichtung gewisen hunn wann se a Blutt ausgedréckt goufen wéi och eng Rei vun aneren Tissuen.
Zum Beispill, den DHODH Gen beaflosst niddreg Dicht Lipoprotein Cholesterin (LDL). E Medikament vermaart géint héich LDL, Leflunomide genannt, funktionnéiert andeems dëst Gen hemmt. Leflunomide gëtt och als eng COVID-19 Therapie ugesinn.
D'Analyse huet gewisen datt dëst Medikament nëmmen a Relatioun mam LDL ausgedréckt gëtt ouni vill aner ënnerschiddlech Aktiounen, iwwer e breede Spektrum vun Tissue vun der Lunge bis zum Colon.
D'Fuerscher hunn d'726 Associatiounen vum MR tëscht Zil a Krankheet fonnt, Benotze vu klineschen Testdaten souwéi dem putative Beweis datt se verschidde phenotypesch Effekter iwwer eng Rei vu Stoffer verursaacht hunn, fir mat den drogbarsten Associatiounen ze kommen. 499 vun hinnen waren eenzegaarteg Paarunge vu Zil a Krankheet, mat deenen aneren a méi wéi engem Tissu observéiert ginn.
Si hunn véier Scoreklassen ageriicht, wéi den Omics Score, den Test Score, den Drogabilitéitsscore, an d'Infektiounsscore. All Score gouf vun 1 op 100 geschleidert. Et waren High Scores fir 2 vun de 499 Associatiounen an 3 vun 4 Klassen, déi hinnen d'Ziler mat der héchster Entwécklungsprioritéit gemaach hunn. 77 hunn héich an zwou Klassen an 97 an enger. Déi verbleiwen 323 haten universell niddereg Noten a ginn dofir als déi niddregst prioritär Medikamentziler ugesinn.
E puer Ziler enthalen den ITGB5 Gen dat vum Medikament Cilengitide gezielt ass, déi fir Glioblastomen an ähnlech Tumoren geduecht war. Seng héich Partituren an de genetesche Profil suggeréieren datt et de Potenzial huet den héije Blutdrock ze reduzéieren. Ënnert den Top 5, all feelen staark Associatiounen mat Bedéngungen wéi Herzarrhythmien, déi hir Notzung am COVID-19 beaflosse kënnen.
Op der anerer Säit, den TLR9 Gen, déi vum Droge hydroxychloroquine gezielt ass, huet héich Scores an zwou Kategorien awer e nidderegen Score fir déi aner zwee. Keng klinesch Beweiser sinn nach opgaang iwwer den antiviralen oder klineschen Virdeel vun enger Kombinatioun vun dësem Medikament mat Azithromycin. Ausserdeem, dëst Gen kann d'Chance op e embolesche Schlag erhéijen, Asthma, a bestëmmte Immunbedéngungen.
D'Studie konnt d'Prioritéit vun Drogenziler op dräi Weeër förderen:Ënnersicht d'Sécherheetsfroen, déi aus der Ëmwandlung vun Drogen fir d'COVID-19 Behandlung entstoe kënnen; verspriechend Medikamentziler z'identifizéieren; an ze fannen wéi d'Droge Zil de mënschleche Phenome a verschiddene Stoffer beaflosst.
Benotzt dës Approche, e potenziell Medikament, Baricitinib, gëtt getest fir seng Effektivitéit am COVID-19. Et gëtt geduecht datt de JAK2 Protein hemmt, an domat systemesch Entzündung reduzéieren. Wéi och ëmmer, déi aktuell Etude proposéiert datt et och chronesch Hepatitis verursaache kann. Tatsächlech, d'Literatur suggeréiert datt Hepatitis B no der Behandlung mam JAK 2 Inhibitor ruxolitinib reaktivéiert gëtt.
Déi dräi héich potenziell Medikamenter aus dëser Studie enthalen immunosuppressiv Medikament Leflunomide, benotzt fir rheumatoider Arthritis, ënner anerem Bedéngungen, a Cilengitide. Déi fréier huet antiviral Aktivitéit géint verschidde Virussen, an déi aktuell Studie seet och datt et Lipid-senkend Eegeschaften huet, wärend déi lescht antihypertensiv Aktivitéit huet, méiglecherweis.
Endlech, e puer vun dësen Ziler ginn a multiple Stoffer ausgedréckt fir dee selwechte Phenotyp ze produzéieren, awer anerer weisen änneren Ausdrock spezifesch fir den Tissu.
Wärend e puer Aschränkungen existéieren, d'Studie bitt eng Pipeline fir statistesch Genetikstudie an eng Open-Access Plattform fir Medikamentziler géint COVID-19 an der Prioritéit Uerdnung ze arrangéieren. Genom-breet Associatiounsstudien (GWAS) kéint d'Qualitéit vun den Donnéeë weider verbesseren, mécht et nach ëmmer méi nëtzlech fir verspriechend Medikamentziler ze fannen ënner potenziell nei verschriwwene Medikamenter.
medRxiv verëffentlecht virleefeg wëssenschaftlech Berichter déi net peer-iwwerschafft sinn an, dofir, soll net als schlussendlech ugesi ginn, guidéiert d'klinesch Praxis/Gesondheetsverhalen, oder als etabléiert Informatioun behandelt.
 Wëssenschaftler entwéckelen Peptiden déi d'Gläichgewiicht an den Darmbakterien restauréieren an d'Atherosklerose ëmgoen
Wëssenschaftler entwéckelen Peptiden déi d'Gläichgewiicht an den Darmbakterien restauréieren an d'Atherosklerose ëmgoen
 Ieweschte Endoskopie
Ieweschte Endoskopie
 Gewiichtsverloscht Medikament Wegovy vun der FDA guttgeheescht
Gewiichtsverloscht Medikament Wegovy vun der FDA guttgeheescht
 Mamm-a-Puppelchen SARS-CoV-2 Iwwerdroung an der Schwangerschaft méiglech awer selten,
Mamm-a-Puppelchen SARS-CoV-2 Iwwerdroung an der Schwangerschaft méiglech awer selten,
 Nei Fuerschung identifizéiert e Link tëscht dem Darmmikrobiom a Strokes
Nei Fuerschung identifizéiert e Link tëscht dem Darmmikrobiom a Strokes
 Déi westlech Diät kann de Risiko vun 'déidlecher Sepsis' erhéijen,
Déi westlech Diät kann de Risiko vun 'déidlecher Sepsis' erhéijen,
 Vaginale Flëssentransplantatioun kann hëllefe fir widderhuelend bakteriell Vaginose ze behandelen
Bakteriell Vaginose ass e gemeinsamen an irksome Problem fir vill Fraen. Elo hunn dFuerscher dTransplantéierend Vaginale Flëssegkeeten vun enger gesonder Fra u Frae mat schwéierer bakterieller Vaginos
Vaginale Flëssentransplantatioun kann hëllefe fir widderhuelend bakteriell Vaginose ze behandelen
Bakteriell Vaginose ass e gemeinsamen an irksome Problem fir vill Fraen. Elo hunn dFuerscher dTransplantéierend Vaginale Flëssegkeeten vun enger gesonder Fra u Frae mat schwéierer bakterieller Vaginos
 Verdauungsmanifestatiounen heefeg awer mëll ënner hospitaliséierten COVID-19 Patienten
Eng Equipe vun 121 Fuerscher aus den USA a Kanada bericht datt wärend Verdauungsmanifestatiounen üblech sinn ënner Leit hospitaliséiert mat Coronavirus Krankheet 2019 (COVID-19), dMajoritéit schéngt m
Verdauungsmanifestatiounen heefeg awer mëll ënner hospitaliséierten COVID-19 Patienten
Eng Equipe vun 121 Fuerscher aus den USA a Kanada bericht datt wärend Verdauungsmanifestatiounen üblech sinn ënner Leit hospitaliséiert mat Coronavirus Krankheet 2019 (COVID-19), dMajoritéit schéngt m
 Gesondste Darmbakterien mat Planzbaséierter oder mediterraner Diät
Eng nei Studie weist datt spezifesch Liewensmëttel, déi entweder vun enger Planzbaséierter oder enger mediterraner Diät geliwwert ginn, den Darm géint entzündlech Stéierunge schützen, andeems se selek
Gesondste Darmbakterien mat Planzbaséierter oder mediterraner Diät
Eng nei Studie weist datt spezifesch Liewensmëttel, déi entweder vun enger Planzbaséierter oder enger mediterraner Diät geliwwert ginn, den Darm géint entzündlech Stéierunge schützen, andeems se selek