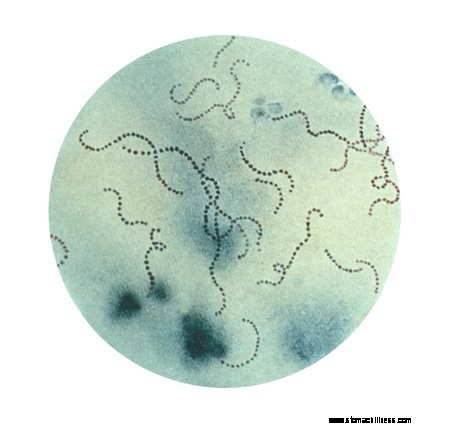
 Figur 1:Foto av Streptococcus pyogenes (GAS). KILDE:CDC
Figur 1:Foto av Streptococcus pyogenes (GAS). KILDE:CDC

Tegn og symptomer på gruppe A Streptococcus-infeksjon avhenger av stedet i kroppen hvor infeksjonen er lokalisert. Typiske symptomer og tegn kan omfatte
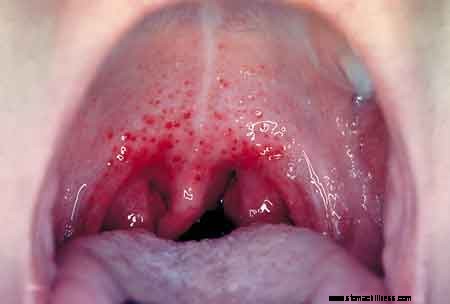 Figur 2:Bilde av en Streptococcus pyogenes (strep hals) infeksjon. KILDE:CDC/Dr. Heinz F. Eichenwald
Figur 2:Bilde av en Streptococcus pyogenes (strep hals) infeksjon. KILDE:CDC/Dr. Heinz F. Eichenwald
Gruppe A Streptococcus er definert som en gram-positiv bakterieslekt sammensatt av Streptococcus pyogenes stammer. Gruppe A Streptococcus stammer har et lignende overflateantigen gjenkjent av spesifikke laboratorietester, kalt Lancefield gruppe A-antigen. Lancefield-grupper (ca. 18 Lancefield-grupper) er sammensatt av forskjellige Streptococcus artsgrupper med spesifikke antigener og kjennetegnes ved spesifikke antistofftester. Dessuten gruppe A streptokokker stammer er beta-hemolytiske (beta-hemolytiske betyr at bakteriene lyserer røde blodceller suspendert i agarplater med utskilte stoffer, se for eksempel fig. 3). Disse testene er nevnt fordi de ofte brukes til å skille gruppe A Streptococcus bakterier fra gruppe B, gruppe C og andre streptokokker grupper. Gruppe A Streptococcus bakterier vises som par og kjeder når de er gramfarget (se fig. 1); disse bakteriene kalles også "beta-strep, GAS og GABHS." Selv om disse bakteriene ufarlig kan kolonisere mennesker på halsen og huden, kan de noen ganger forårsake milde til alvorlige sykdommer. GAS-bakterier har forårsaket sykdommer hos mennesker sannsynligvis siden mennesket først utviklet seg.
Streptococcus pyogenes (GAS) bakterier har mange komponenter som bidrar til patogenets evne til å forårsake sykdom:
Eksotoksiner forårsaker skarlagensfeberutslett, skader organer, kan forårsake sjokk og hemme det menneskelige immunsystemet, mens de menneskelige immunsystemstimulatorene kan stimulere immunsystemet til å produsere antistoffer som sannsynligvis spiller en rolle i utviklingen av autoimmune responser som kan føre til glomerulonefritt eller akutt revmatisk feber. S. pyogenes (GAS) har over 100 serotyper som kan variere noe i deres evne til å produsere de ovennevnte komponentene som bidrar til patogenisiteten til hver bakteriestamme. I 2015 ble en ny GAS-stamme, kjent som genotype emm89, notert i Storbritannia; de genetiske endringene så ut til å forbedre stammens evne til å forårsake sykdom og ser ut til å erstatte eldre GAS-genotyper.
I de fleste tilfeller blir GAS-bakterier kontrahert via person-til-person kontakt med slim, hud eller infiserte lesjoner. Spredning av GAS-organismene skjer sjelden av gjenstander som har fått kontakt med infiserte mennesker. Imidlertid er mange mennesker kolonisert (har bakteriene på kroppsoverflater, men er ikke infisert) med GAS-bakterier. Spedbarn og barn får ofte først disse organismene fra sine koloniserte mødre.
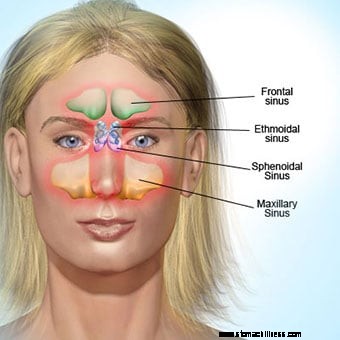 Sinusitt er en av de vanligste tilstandene som kan ramme mennesker gjennom hele livet. Kilde:iStock / MedicineNet
Sinusitt er en av de vanligste tilstandene som kan ramme mennesker gjennom hele livet. Kilde:iStock / MedicineNet
Det finnes en rekke sykdommer som GAS-organismer kan forårsake. De dominerende sykdommene er som følger:
Denne listen er ikke uttømmende da GAS-bakterier har blitt funnet i mange andre sykdomsprosesser. I tillegg kan mange av sykdommene nevnt ovenfor også være forårsaket av mange andre patogener, selv om de tre førstnevnte (faryngitt, skarlagensfeber og revmatisk feber) hovedsakelig er forårsaket av GAS. Noen etterforskere anser de fleste av disse sykdommene som komplikasjoner av en første GAS-hud- eller halsinfeksjon.
Generelt er streptokokkinfeksjoner i gruppe A smittsomt, men det er noen kvalifikasjoner for dette svaret. For eksempel er halsbetennelse smittsom, men andre infeksjonstyper som toksisk sjokksyndrom anses generelt som ikke-smittsom; følgelig avhenger svaret av den spesifikke typen infeksjon og eventuelle formildende omstendigheter.
For de infeksjonene som anses å være smittsomme, er personen smittsom i inkubasjonstiden (før eventuelle symptomer på infeksjonen utvikler seg) og gjennom den akutte fasen av infeksjonen mens pasienten har symptomer. Når symptomene stopper, er personen vanligvis ikke-smittsom med mindre personen blir en bærer (kolonisert med gruppe A streptokokker, men uten symptomer).
Inkubasjonstiden for GAS-faryngitt og cellulitt varierer fra omtrent én til fem dager. Andre typer GAS-infeksjon kan utvikle seg raskt (nekrotiserende fasciitt), mens andre (skarlagensfeber) kan ta en uke eller mer å utvikle.
GAS-infeksjoner kan gi mange forskjellige tegn og symptomer:
De fleste sykdommene som er oppført her for GAS-infeksjon oppstår vanligvis etter en initial faryngitt, med nekrotiserende fasciitt og toksisk sjokk som noen ganger oppstår uten en påvisbar initial faryngittinfeksjon. Andre sykdomsprosesser som involverer GAS-organismer (for eksempel hjernehinnebetennelse, beininfeksjoner, lungebetennelse, sårinfeksjoner og andre) produserer de typiske symptomene forbundet med disse sykdomsprosessene og er klinisk ikke unike for GAS eller andre patogene organismer.
Invasiv GAS-sykdom er når GAS-organismer invaderer og infiserer organer eller organsystemer i kroppen (for eksempel GAS-infeksjoner i blodet, muskler, fettvev eller lungene). Dette er alvorlige infeksjoner, og dødeligheten (dødsraten) varierer fra ca. 10%-60%, avhengig av området(e) av kroppen som er infisert. De mest alvorlige formene for invasive GAS-infeksjoner er nekrotiserende fasciitt og streptokokktoksisk sjokksyndrom beskrevet nedenfor. Personer med høyere risiko for å få invasive former for GAS er personer med kroniske sykdommer og immunsupprimerte pasienter (for eksempel pasienter med kreft, diabetes og nyresvikt, og personer som tar medisiner av steroidtype). De fleste friske mennesker får ikke denne typen GAS-sykdom, men hvis de har hudbrudd (kutt, skrubbsår, nylige operasjonssteder), har disse personene en høyere risiko for GAS-sykdom enn personer uten hudbrudd.
Andre pasienter som er i faresonen for invasiv GAS-sykdom er pasienter med GAS-infeksjoner som lett kan utvikle seg til dypt fett og muskler (for eksempel en GAS-infeksjon nær pungen eller anus eller en abscess i huden) og kan utvikle seg til nekrotiserende fasciitt. Toksisk sjokksyndrom ble først funnet å være assosiert med vaginale infeksjoner sekundært til tampongbruk (eller upassende bruk som å la en tampong ligge i skjeden i lengre tid). Imidlertid har enhver pasient som har et sår eller operasjon som krever pakking for å redusere blødning (for eksempel nesepakning for alvorlig neseblødning) økt risiko for toksisk sjokksyndrom. Toksisk sjokksyndrom kan også være forårsaket av en annen bakterie kalt Staphylococcus .
Følgelig inkluderer risikofaktorer for at GAS-organismer forårsaker infeksjon undertrykkelse av immunsystemet (se ovenfor), åpne sår eller sårpakking, eller tamponger som kan fremme GAS-overlevelse og spredning. Barn og eldre har høyere risiko for å bli smittet med GAS.
Tidlige tegn og symptomer på nekrotiserende fasciitt inkluderer feber, sterke smerter, hevelse og erytem (rødhet) på sårstedet eller stedet der GAS-organismer kom inn i kroppen. Smerten og hevelsen kan strekke seg langt utover erytem. Hudforandringer kan i utgangspunktet ligne på cellulitt, men sårdannelse, skorper og væskedrenering fra stedet utvikles, noen ganger raskt (fig. 3). GAS-organismer kan deretter spre seg til blodet og pasienten kan utvikle bakteriemi og septisk sjokk med høy feber og lavt blodtrykk. Omtrent 20 % av pasientene med nekrotiserende fasciitt forårsaket av GAS vil dø av infeksjonen.
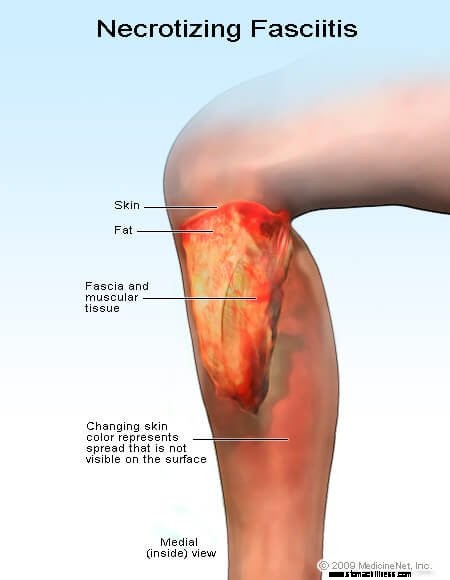 Figur 3:Bilde av nekrotiserende fasciitt (kjøttspisende sykdom)
Figur 3:Bilde av nekrotiserende fasciitt (kjøttspisende sykdom)
Tidlige symptomer på TSS er uspesifikke og begynner ofte med influensalignende symptomer på mild feber og ubehag. Imidlertid utvikler TSS seg ofte plutselig med symptomer på høy feber, kvalme, oppkast, diaré, hudutslett og lavt blodtrykk. Hvis det utvikler seg, kan det oppstå forvirring, hodepine, anfall og hudtap fra håndflatene og fra fotsålene. Blodtrykket kan bli farlig lavt slik at kroppsorganene ikke blir overfylt med nok blod, og hvis multiorgansvikt utvikler seg, dør pasienten ofte. Dødsraten varierer mye, avhengig av hvor godt pasienten kan reagere på behandlingen. GAS-bakterier og Staphylococcus aureus er de dominerende bakteriene som forårsaker TSS.
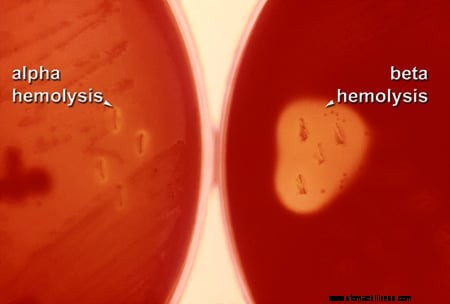 Figur 4:Bilde av beta-hemolyse. KILDE:CDC/Richard R. Facklam, PhD
Figur 4:Bilde av beta-hemolyse. KILDE:CDC/Richard R. Facklam, PhD Etter en anamnese og fysisk undersøkelse, diagnostiserer mange klinikere presumptivt halsbetennelse fra symptomproduksjonen og halsens utseende (se fig. 2). Imidlertid danner kulturer fra halsen eller et annet infeksjonssted grunnlaget for definitiv testing. For eksempel vil GAS-organismer vokse på saueblodagarplater som inneholder to forskjellige antibiotika og forårsake beta-hemolyse (fullstendig røde blodceller fra sau for å danne et klart område) av sauens røde blodceller (se fig. 3). I tillegg er det hurtigtester (RADT eller rask antigendeteksjonstest) som tar bare noen få minutter å fullføre som oppdager et karbohydratoverflateantigen produsert av GAS, med spesifisitet på ca. 95 % eller bedre og ganske god sensitivitet på ca. 80 %- 90 %
Fordi det er mange andre grupper av streptokokker spp., er positiv identifikasjon av de infiserte bakteriene nødvendig for å skille ut andre bakterier som kan forårsake noen lignende symptomer, men som kan kreve en annen opparbeiding, annen behandling og produsere andre komplikasjoner.
Disse testene hjelper med å skille GAS fra Streptococcus pneumoniae og andre organismer.
Antibiotika behandler invasive GAS-infeksjoner så vel som ikke-invasive gruppe A strep-infeksjoner. Selv om mange antibiotika kan være adekvat behandling for GAS-infeksjoner, vil den beste praksismetoden være å bestemme antibiotikafølsomheten til GAS-bakterier for å være sikker på at bakteriene er mottakelige for antibiotika.
Besides, early diagnosis and treatment of invasive GAS infections yield the best patient outcomes. Many clinicians consult with an infectious disease specialist to help determine the best antibiotic therapy for individual patients. More GAS strains are being reported to have some resistance to one or more antibiotics so the treatment may require alterations in antibiotics. The infectious disease specialist can help choose the most effective antibiotic combinations to treat antibiotic-resistant GAS organisms.
The specialists that treat group A streptococcal infections are infectious-disease specialists. However, depending on the severity and the type of infection, other specialists may be involved. For example, if hospitalization is needed, a critical care specialist may join the team; if the person is pregnant, an OB/GYN specialist and/or a pediatric specialist may be needed. If surgical debridement is needed (necrotizing fasciitis), a surgical specialist would be consulted. Other types of medical specialists that may care for patients with GAS infections include emergency-medicine specialists, dermatologists, internal-medicine specialists, family-medicine specialists, nephrologists, and ear, nose, and throat specialists.
Many of the complications of GAS infections are considered to be diseases themselves. For example, scarlet fever, rheumatic fever, necrotizing fasciitis, toxic shock syndrome, and many others can complicate or be triggered by GAS infection. Other post-streptococcal complications can include the necessity to remove tonsils, renal damage, abscess formation, seizures, and other organ damage; some researchers suggest that severe GAS infections in children may lead to permanent or long-lasting brain changes. Although GAS infections in pregnant females during pregnancy and delivery are infrequent, they require immediate treatment to avoid post-streptococcal complications such as endometritis, sepsis, necrotizing fasciitis, or toxic shock syndrome.
Many GAS infections can be prevented by reducing the spread of organisms from one person to another. Washing hands frequently is one of the major ways to reduce bacterial transmission. Also, not sharing the same food and drink containers with others may be effective. For those people with a GAS infection, covering the mouth and nose when sneezing or coughing can reduce the chance of transmitting the bacteria to others. Washing material that comes in contact with GAS-infected people is also another way to reduce exposure to GAS organisms.
Early treatment of deep infections (for example, excision, drainage, and antibiotic treatment of rectal abscesses) helps prevent invasive GAS disease. Besides, appropriate and timely removal of tampons and surgical packing may reduce the incidence of toxic shock syndrome.
Currently, there is no vaccine commercially available for GAS, but researchers are working on developing vaccines. At least four different major approaches are being researched. There has been some success with a related experimental vaccine against GAS bacterial antigens coupled to cholera toxin subunits. However, the GAS vaccine, by Vaxent, a vaccine company, prepared by recombinant technology, maybe going into human clinical trials. The new experimental vaccines may become available in the future to prevent GAS infections.
The prognosis for mild GAS infections is usually good to excellent. The prognosis for patients with chronic diseases, such as diabetes or cancer, or for those who are immunosuppressed, is more guarded, but often is still good with early treatment. However, the prognosis for patients developing necrotizing fasciitis or toxic shock syndrome ranges from good with early effective treatment to poor when the diseases are diagnosed and treated late in the disease process.
The following sites can provide additional information about GAS infections:
"Strep Throat," MedicineNet.com
"Rapid Strep Test," MedicineNet.com
 Perfectus Biomed skal stille ut på IPS -konferansen i Liverpool
Perfectus Biomed -teamet stiller ut på konferansen Infection Prevention Society (IPS) i Liverpool denne måneden. Konferansen vil finne sted på Arena and Convention Center i Liverpool 22. - 24. septemb
Perfectus Biomed skal stille ut på IPS -konferansen i Liverpool
Perfectus Biomed -teamet stiller ut på konferansen Infection Prevention Society (IPS) i Liverpool denne måneden. Konferansen vil finne sted på Arena and Convention Center i Liverpool 22. - 24. septemb
 Nye WGO-retningslinjer:hvordan kostholdet ditt kan hjelpe deg med å ta vare på tarmmikrobiotaen din
Når magen er urolig, tenker du ofte tilbake på hva du spiste. Med flere og flere mennesker som lider av fordøyelsesproblemer, er det ikke rart at de henvender seg til matbaserte løsninger for å håndte
Nye WGO-retningslinjer:hvordan kostholdet ditt kan hjelpe deg med å ta vare på tarmmikrobiotaen din
Når magen er urolig, tenker du ofte tilbake på hva du spiste. Med flere og flere mennesker som lider av fordøyelsesproblemer, er det ikke rart at de henvender seg til matbaserte løsninger for å håndte
 Forbereder for en koloskopi
Hvordan forberede seg på en koloskopi Når du forbereder deg på en koloskopi, er det veldig viktig å følge alle instruksjonene nøye. Du vil motta en pakke med informasjon ved din første konsultasjon h
Forbereder for en koloskopi
Hvordan forberede seg på en koloskopi Når du forbereder deg på en koloskopi, er det veldig viktig å følge alle instruksjonene nøye. Du vil motta en pakke med informasjon ved din første konsultasjon h