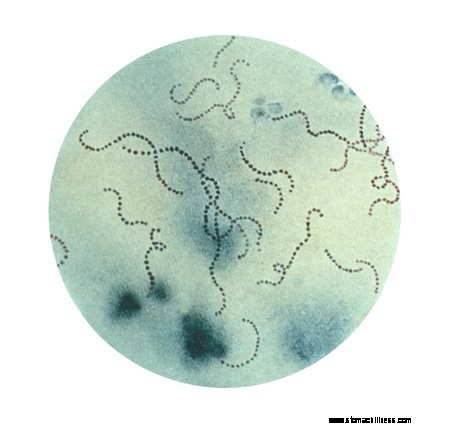
 Figure 1 :Photo de Streptococcus pyogenes (GAS). SOURCE :CDC
Figure 1 :Photo de Streptococcus pyogenes (GAS). SOURCE :CDC

Les signes et les symptômes d'une infection à streptocoque du groupe A dépendent du site du corps où se situe l'infection. Les symptômes et signes typiques peuvent inclure
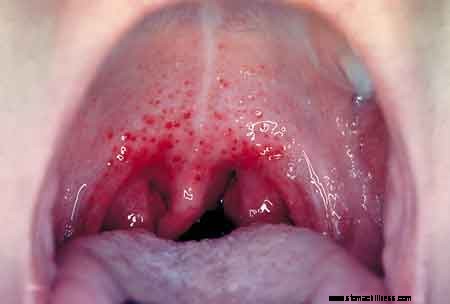 Figure 2 :Image d'une infection à Streptococcus pyogenes (angine streptococcique). SOURCE :CDC/Dr. Heinz F. Eichenwald
Figure 2 :Image d'une infection à Streptococcus pyogenes (angine streptococcique). SOURCE :CDC/Dr. Heinz F. Eichenwald
Groupe A Streptocoque est défini comme un genre bactérien Gram positif composé de Streptococcus pyogenes souches. Groupe A Streptocoque souches ont un antigène de surface similaire reconnu par des tests de laboratoire spécifiques, appelé antigène du groupe A de Lancefield. Les groupes de Lancefield (environ 18 groupes de Lancefield) sont composés de différents Streptococcus groupes d'espèces avec des antigènes spécifiques et se distinguent par des tests d'anticorps spécifiques. Par ailleurs, groupe A Streptococcus les souches sont bêta-hémolytiques (bêta-hémolytique signifie que les bactéries lysent les globules rouges en suspension dans des plaques de gélose avec des substances sécrétées, voir, par exemple, Fig. 3). Ces tests sont mentionnés car ils sont fréquemment utilisés pour distinguer les streptocoques du groupe A bactéries du groupe B, du groupe C et d'autres streptocoques groupes. Groupe A Streptocoque les bactéries apparaissent sous forme de paires et de chaînes lorsqu'elles sont colorées au gramme (voir Fig. 1); ces bactéries sont également appelées « streptocoque bêta, GAS et GABHS ». Bien que ces bactéries puissent coloniser sans danger les gens sur leur gorge et leur peau, elles peuvent parfois provoquer des maladies légères à graves. Les bactéries GAS causent des maladies chez l'homme probablement depuis que l'homme s'est développé pour la première fois.
Streptococcus pyogènes (GAS) les bactéries ont de nombreux composants qui contribuent à la capacité de l'agent pathogène à provoquer des maladies :
Les exotoxines provoquent une éruption de scarlatine, endommagent les organes, peuvent provoquer un choc et inhibent le système immunitaire humain, tandis que les stimulateurs du système immunitaire humain peuvent stimuler le système immunitaire à produire des anticorps qui jouent probablement un rôle dans le développement de réponses auto-immunes pouvant conduire à la glomérulonéphrite. ou rhumatisme articulaire aigu. S. pyogènes (GAS) a plus de 100 sérotypes qui peuvent varier quelque peu dans leur capacité à produire les composants ci-dessus qui contribuent à la pathogénicité de chaque souche de bactérie. En 2015, une nouvelle souche de GAS, connue sous le nom de génotype emm89, a été notée au Royaume-Uni; les modifications génétiques semblaient améliorer la capacité de la souche à provoquer des maladies et semblent remplacer les génotypes GAS plus anciens.
Dans la plupart des cas, les bactéries GAZ sont contractées par contact de personne à personne avec du mucus, de la peau ou des lésions infectées. La propagation des organismes GAS se produit rarement par des objets qui ont été en contact avec des personnes infectées. Cependant, de nombreuses personnes sont colonisées (ont la bactérie sur les surfaces corporelles mais ne sont pas infectées) par des bactéries SGA. Les nourrissons et les enfants acquièrent souvent d'abord ces organismes de leurs mères colonisées.
 La sinusite est l'une des conditions les plus courantes qui peuvent affecter les gens tout au long de leur vie.Source :iStock / MedicineNet
La sinusite est l'une des conditions les plus courantes qui peuvent affecter les gens tout au long de leur vie.Source :iStock / MedicineNet
Il existe un certain nombre de maladies que les organismes SGA peuvent causer. Les maladies prédominantes sont les suivantes :
Cette liste n'est pas exhaustive car des bactéries GAS ont été trouvées dans de nombreux autres processus pathologiques. De plus, bon nombre des maladies énumérées ci-dessus peuvent également être causées par de nombreux autres agents pathogènes, bien que les trois premiers énumérés (pharyngite, scarlatine et rhumatisme articulaire aigu) soient principalement causés par le SGA. Certains chercheurs considèrent la plupart de ces maladies comme des complications d'une infection initiale à SGA de la peau ou de la gorge.
En général, les infections à streptocoque du groupe A sont contagieuses, mais il y a quelques qualificatifs à cette réponse. Par exemple, l'angine streptococcique est contagieuse, mais d'autres types d'infection tels que le syndrome de choc toxique sont généralement considérés comme non contagieux; par conséquent, la réponse dépend du type spécifique d'infection et de toute circonstance atténuante.
Pour les infections considérées comme contagieuses, la personne est contagieuse pendant la période d'incubation (avant que tout symptôme de l'infection ne se développe) et pendant la phase aiguë de l'infection pendant que le patient présente des symptômes. Lorsque les symptômes cessent, la personne est généralement non contagieuse à moins qu'elle ne devienne porteuse (colonisée par le streptocoque du groupe A mais sans symptômes).
La période d'incubation de la pharyngite et de la cellulite à SGA varie d'environ un à cinq jours. D'autres types d'infections à SGA peuvent se développer rapidement (fasciite nécrosante) tandis que d'autres (scarlatine) peuvent prendre une semaine ou plus à se développer.
Les infections à SGA peuvent produire de nombreux signes et symptômes différents :
La plupart des maladies répertoriées ici pour l'infection à SGA surviennent généralement après une pharyngite initiale, avec une fasciite nécrosante et un choc toxique survenant parfois sans infection initiale détectable de la pharyngite. D'autres processus pathologiques impliquant des organismes SGA (par exemple, la méningite, les infections osseuses, la pneumonie, les infections de plaies et autres) produisent les symptômes typiques associés à ces processus pathologiques et ne sont cliniquement pas uniques au SGA ou à d'autres organismes pathogènes.
La maladie invasive à SGA survient lorsque des organismes à SGA envahissent et infectent des organes ou des systèmes d'organes du corps (par exemple, des infections à SGA du sang, des muscles, des tissus adipeux ou des poumons). Ce sont des infections graves et le taux de mortalité (taux de mortalité) varie d'environ 10% à 60%, selon la ou les zones du corps infectées. Les formes les plus graves d'infections invasives à SGA sont la fasciite nécrosante et le syndrome de choc toxique streptococcique décrits ci-dessous. Les personnes les plus à risque de contracter des formes invasives de SGA sont les personnes atteintes de maladies chroniques et les patients immunodéprimés (par exemple, les patients atteints de cancer, de diabète et d'insuffisance rénale, et les personnes prenant des médicaments de type stéroïde). La plupart des personnes en bonne santé ne contractent pas ce type de maladie à SGA, mais si elles ont des lésions cutanées (coupures, abrasions, sites chirurgicaux récents), ces personnes ont un risque plus élevé de maladie à SGA que les personnes sans lésions cutanées.
Les autres patients à risque de maladie invasive à SGA sont les patients atteints d'infections à SGA qui peuvent facilement évoluer vers les tissus adipeux et musculaires profonds (par exemple, une infection à SGA près du scrotum ou de l'anus ou un abcès cutané) et peuvent évoluer vers une fasciite nécrosante. Le syndrome de choc toxique s'est d'abord avéré associé à des infections vaginales secondaires à l'utilisation de tampons (ou à une utilisation inappropriée, comme laisser un tampon dans le vagin pendant une période prolongée). Cependant, tout patient qui a une plaie ou une intervention chirurgicale nécessitant un pansement pour réduire le saignement (par exemple, un pansement nasal en cas de saignement de nez sévère) présente un risque accru de syndrome de choc toxique. Le syndrome de choc toxique peut également être causé par une autre bactérie appelée Staphylococcus .
Par conséquent, les facteurs de risque pour les organismes SGA de provoquer une infection comprennent la suppression du système immunitaire (voir ci-dessus), les plaies ouvertes ou le pansement des plaies, ou les tampons qui peuvent favoriser la survie et la prolifération du SGA. Les enfants et les personnes âgées sont plus à risque d'être infectés par le SGA.
Les premiers signes et symptômes de la fasciite nécrosante comprennent de la fièvre, une douleur intense, un gonflement et un érythème (rougeur) au site de la plaie ou au site où les organismes SGA ont pénétré dans le corps. La douleur et l'enflure peuvent s'étendre bien au-delà de l'érythème. Les changements cutanés peuvent initialement ressembler à une cellulite, mais des ulcérations, des croûtes et du liquide s'écoulant du site se développent, parfois rapidement (Fig. 3). Les organismes GAS peuvent alors se propager dans la circulation sanguine et le patient peut développer une bactériémie et un choc septique avec une forte fièvre et une pression artérielle basse. Environ 20 % des patients atteints de fasciite nécrosante causée par le SGA mourront des suites de l'infection.
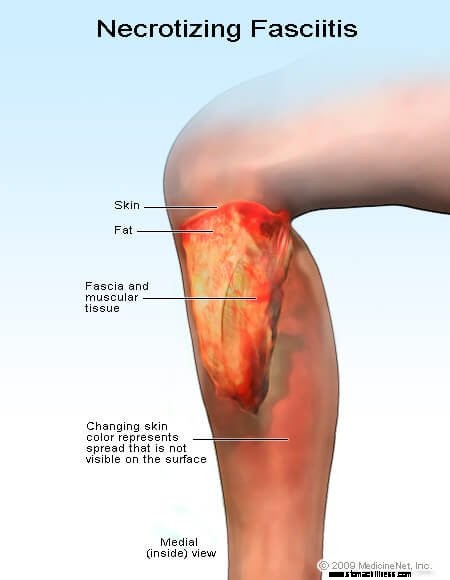 Figure 3 :Photo d'une fasciite nécrosante (maladie mangeuse de chair)
Figure 3 :Photo d'une fasciite nécrosante (maladie mangeuse de chair)
Les premiers symptômes du SCT ne sont pas spécifiques et commencent souvent par des symptômes pseudo-grippaux de fièvre légère et de malaise. Cependant, le SCT progresse souvent soudainement avec des symptômes de forte fièvre, de nausées, de vomissements, de diarrhée, d'éruptions cutanées et d'hypotension artérielle. Si elle progresse, une confusion, des maux de tête, des convulsions et une perte de peau de la paume des mains et de la plante des pieds peuvent survenir. La pression artérielle peut devenir dangereusement basse, de sorte que les organes du corps ne sont pas suffisamment imprégnés de sang, et si une défaillance multiviscérale se développe, le patient meurt souvent. Le taux de mortalité varie considérablement, en fonction de la capacité du patient à répondre au traitement. Bactéries GAS et Staphylococcus aureus sont les principales bactéries responsables du SCT.
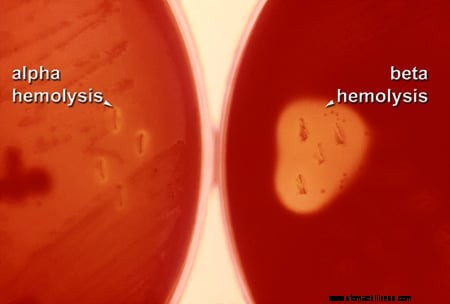 Figure 4 :Image de la bêta-hémolyse. SOURCE :CDC/Richard R. Facklam, PhD
Figure 4 :Image de la bêta-hémolyse. SOURCE :CDC/Richard R. Facklam, PhD Après une anamnèse et un examen physique, de nombreux cliniciens diagnostiquent par présomption l'angine streptococcique à partir de la production de symptômes et de l'apparence de la gorge (voir Fig. 2). Cependant, les cultures de la gorge ou d'un autre site d'infection constituent la base des tests définitifs. Par exemple, les organismes GAS se développeront sur des plaques de gélose au sang de mouton qui contiennent deux antibiotiques différents et provoqueront une bêta-hémolyse (lyse complète des globules rouges du sang de mouton pour former une zone claire) des globules rouges du mouton (voir Fig. 3). De plus, il existe des tests rapides (RADT ou test de détection rapide d'antigène) qui ne prennent que quelques minutes pour détecter un antigène de surface glucidique produit par le GAS, avec une spécificité d'environ 95 % ou mieux et une assez bonne sensibilité d'environ 80 % - 90 %.
Parce qu'il existe de nombreux autres groupes de Streptococcus spp., une identification positive des bactéries infectantes est nécessaire pour séparer les autres bactéries qui peuvent provoquer des symptômes similaires, mais peuvent nécessiter un bilan différent, un traitement différent et entraîner des complications différentes.
Ces tests permettent de distinguer le SGA de Streptococcus pneumoniae et d'autres organismes.
Les antibiotiques traitent les infections invasives à SGA ainsi que les infections non invasives à streptocoque du groupe A. Bien que de nombreux antibiotiques puissent constituer un traitement adéquat pour les infections à SGA, les meilleures pratiques consisteraient à déterminer la sensibilité aux antibiotiques des bactéries à SGA pour s'assurer que les bactéries sont sensibles aux antibiotiques.
Besides, early diagnosis and treatment of invasive GAS infections yield the best patient outcomes. Many clinicians consult with an infectious disease specialist to help determine the best antibiotic therapy for individual patients. More GAS strains are being reported to have some resistance to one or more antibiotics so the treatment may require alterations in antibiotics. The infectious disease specialist can help choose the most effective antibiotic combinations to treat antibiotic-resistant GAS organisms.
The specialists that treat group A streptococcal infections are infectious-disease specialists. However, depending on the severity and the type of infection, other specialists may be involved. For example, if hospitalization is needed, a critical care specialist may join the team; if the person is pregnant, an OB/GYN specialist and/or a pediatric specialist may be needed. If surgical debridement is needed (necrotizing fasciitis), a surgical specialist would be consulted. Other types of medical specialists that may care for patients with GAS infections include emergency-medicine specialists, dermatologists, internal-medicine specialists, family-medicine specialists, nephrologists, and ear, nose, and throat specialists.
Many of the complications of GAS infections are considered to be diseases themselves. For example, scarlet fever, rheumatic fever, necrotizing fasciitis, toxic shock syndrome, and many others can complicate or be triggered by GAS infection. Other post-streptococcal complications can include the necessity to remove tonsils, renal damage, abscess formation, seizures, and other organ damage; some researchers suggest that severe GAS infections in children may lead to permanent or long-lasting brain changes. Although GAS infections in pregnant females during pregnancy and delivery are infrequent, they require immediate treatment to avoid post-streptococcal complications such as endometritis, sepsis, necrotizing fasciitis, or toxic shock syndrome.
Many GAS infections can be prevented by reducing the spread of organisms from one person to another. Washing hands frequently is one of the major ways to reduce bacterial transmission. Also, not sharing the same food and drink containers with others may be effective. For those people with a GAS infection, covering the mouth and nose when sneezing or coughing can reduce the chance of transmitting the bacteria to others. Washing material that comes in contact with GAS-infected people is also another way to reduce exposure to GAS organisms.
Early treatment of deep infections (for example, excision, drainage, and antibiotic treatment of rectal abscesses) helps prevent invasive GAS disease. Besides, appropriate and timely removal of tampons and surgical packing may reduce the incidence of toxic shock syndrome.
Currently, there is no vaccine commercially available for GAS, but researchers are working on developing vaccines. At least four different major approaches are being researched. There has been some success with a related experimental vaccine against GAS bacterial antigens coupled to cholera toxin subunits. However, the GAS vaccine, by Vaxent, a vaccine company, prepared by recombinant technology, maybe going into human clinical trials. The new experimental vaccines may become available in the future to prevent GAS infections.
The prognosis for mild GAS infections is usually good to excellent. The prognosis for patients with chronic diseases, such as diabetes or cancer, or for those who are immunosuppressed, is more guarded, but often is still good with early treatment. However, the prognosis for patients developing necrotizing fasciitis or toxic shock syndrome ranges from good with early effective treatment to poor when the diseases are diagnosed and treated late in the disease process.
The following sites can provide additional information about GAS infections:
"Strep Throat," MedicineNet.com
"Rapid Strep Test," MedicineNet.com
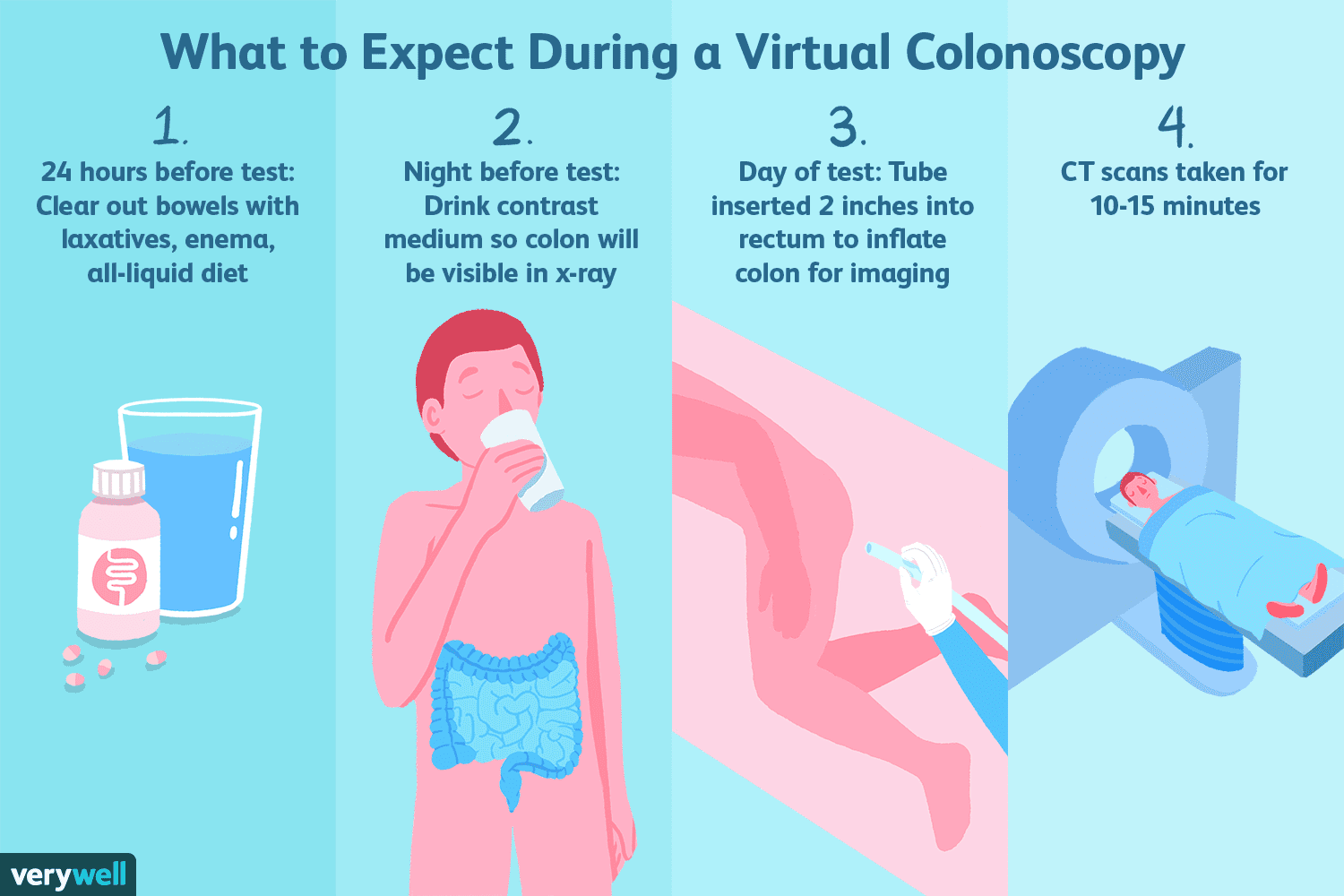 Qu'est-ce qu'une coloscopie virtuelle ?
Qu'est-ce qu'une coloscopie virtuelle ?
 Un intestin sain pour un cœur sain ? Une étude de 10 ans examine la connexion intestin-cœur
Un intestin sain pour un cœur sain ? Une étude de 10 ans examine la connexion intestin-cœur
 Types de sondes d'alimentation et leurs utilisations
Types de sondes d'alimentation et leurs utilisations
 Symptômes, signes, causes et traitement de l'hypertrophie de la rate (splénomégalie)
Symptômes, signes, causes et traitement de l'hypertrophie de la rate (splénomégalie)
 Nutrition et ballonnements :ce que vous devez savoir
Nutrition et ballonnements :ce que vous devez savoir
 22 remèdes maison pour la digestion
22 remèdes maison pour la digestion
 Gérer sa vie avec le syndrome du côlon irritable
Le syndrome du côlon irritable est une affection chronique. Sa cause est inconnue. Parlons de la façon de le tenir en laisse. Quest-ce que le syndrome du côlon irritable ? Le syndrome du côlon irrit
Gérer sa vie avec le syndrome du côlon irritable
Le syndrome du côlon irritable est une affection chronique. Sa cause est inconnue. Parlons de la façon de le tenir en laisse. Quest-ce que le syndrome du côlon irritable ? Le syndrome du côlon irrit
 5 façons simples de vaincre le reflux acide aujourd'hui
Le reflux acide est un trouble dans lequel une variété de symptômes couramment ressentis peuvent sadditionner et entraîner la maladie elle-même. Des symptômes tels que brûlures destomac, ballonnements
5 façons simples de vaincre le reflux acide aujourd'hui
Le reflux acide est un trouble dans lequel une variété de symptômes couramment ressentis peuvent sadditionner et entraîner la maladie elle-même. Des symptômes tels que brûlures destomac, ballonnements
 Quels sont les signes avant-coureurs de la maladie de Crohn ?
La maladie de Crohn peut provoquer ces signes et symptômes ; cependant, seul un médecin peut vous diagnostiquer correctement. La maladie de Crohn est une maladie inflammatoire de lintestin (MICI) q
Quels sont les signes avant-coureurs de la maladie de Crohn ?
La maladie de Crohn peut provoquer ces signes et symptômes ; cependant, seul un médecin peut vous diagnostiquer correctement. La maladie de Crohn est une maladie inflammatoire de lintestin (MICI) q