Die Darmmikrobiota beeinflusst die Funktionsweise vieler Körperprozesse, wie Immunfunktion, normaler Stoffwechsel, und die Entwicklung des Organismus. Es beeinflusst auch das Verhalten des Wirts, einschließlich sozialer Aktivität und Stressreaktionen, die mit vielen verschiedenen Störungen des Gehirns und/oder des Geistes verbunden sind. Jedoch, Es gibt nicht viel Wissen über die zugrunde liegenden Mechanismen, durch die Darmbakterien die Funktionsweise der Gehirnzellen verändern können, oder das Verhalten des größeren Organismus.
Frühere Forschungen liefern starke Hinweise auf den Zusammenhang zwischen der Darmgesundheit und einer Reihe von Krankheiten, die so unterschiedlich sind wie ASS und posttraumatische Belastungsstörung. Viele Studien haben gezeigt, dass Autoimmunerkrankungen mit einem abnormalen Darmmikrobiom verbunden sind. und auch zu mehreren psychiatrischen und neurologischen Erkrankungen. Zum Beispiel, entzündliche Darmerkrankung, Multiple Sklerose und Psoriasis sind alle Erkrankungen der Autoimmunität, und diese Personen haben ein höheres Risiko, eine geringere Anzahl verschiedener Darmbakterien zu haben, sowie eine größere Wahrscheinlichkeit von Angst, Stimmungsstörungen und Depressionen. Gemeinsame Gene scheinen auch sowohl bei psychiatrischen als auch bei Autoimmunerkrankungen vorhanden zu sein.
In der vorliegenden Studie, die Wissenschaftler untersuchten die Gehirne von zwei Arten von Mäusen mit abnormaler Darmmikrobiota:Mäusen, die Antibiotika erhalten hatten, um das Bakterienwachstum im Darm zu reduzieren, oder Mäuse, die in einer völlig sterilen Umgebung gezüchtet wurden, um keimfrei zu sein (GF). Sie setzten diese Mäusepopulationen zunächst einer Gefahr aus, und dann entfernt. Bei der Untersuchung der Lernreaktionen in diesen Mauspopulationen, sie stellten fest, dass beide eine verringerte Lernfähigkeit zeigten, dass eine Gefahr, die sie bedrohte, nicht mehr zu befürchten war (sogenanntes Angstauslöschungslernen). Mit anderen Worten, normale Mäuse entwickeln eine reflexartige Angstreaktion auf eine drohende Gefahr, aber im Laufe der Zeit, da der Stimulus nach der Exposition keinen Schaden anrichtete, ihre konditionierten Angstreaktionen nehmen ab. Dieses Lernen war bei den mit GF oder Antibiotika behandelten Mäusen nicht offensichtlich, die im Laufe der Zeit weiterhin konditionierte Angstreaktionen zeigten.
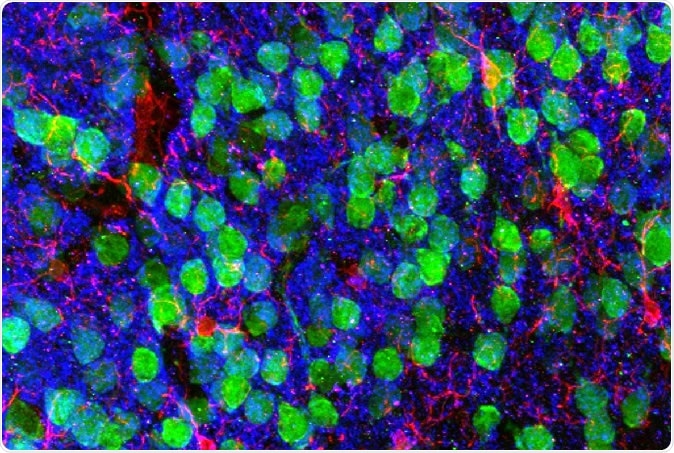 Bildgebung des Gehirns. Medialer präfrontaler Kortex mit kortikalen Neuronen (grün), Mikroglia (rot), und der postsynaptische Marker PSD95 (blau). Bild mit freundlicher Genehmigung von Dr. Christopher Parkhurst und David Artis (WCM).
Bildgebung des Gehirns. Medialer präfrontaler Kortex mit kortikalen Neuronen (grün), Mikroglia (rot), und der postsynaptische Marker PSD95 (blau). Bild mit freundlicher Genehmigung von Dr. Christopher Parkhurst und David Artis (WCM). Um herauszufinden, warum, die Forscher sequenzierten die RNA innerhalb von Mikroglia, die Immunzellen des Gehirns. RNA ist das Zwischenmolekül zwischen dem genetischen Bauplan im Zellkern und dem letzten Protein im Zytoplasma. aus dem kodierten Gen hergestellt. Somit zeigt eine RNA-Sequenz ein Gen, das in dieser bestimmten Zelle exprimiert wird.
Die RNA-Sequenzierung zeigte ein anderes Muster der Genexpression in den Gehirnzellen dieser Mauspopulationen, was wiederum die normale Umgestaltung beeinflusste, die als Teil des Lernens auftritt. Gehirnzellen bilden Verbindungen oder Synapsen, um Informationen untereinander auszutauschen. Jedoch, wie das Lernen fortschreitet, bestimmte Synapsen werden entfernt und andere hinzugefügt, entsprechend dem Impulsverkehr auf diesem Weg. Dies wird als Synapsenbeschneidung bezeichnet und ist ein wichtiger Prozess beim Lernen.
Bei der Untersuchung der Unterschiede in der Genexpression im medialen präfrontalen Kortex des Mausgehirns, entdeckten die Wissenschaftler, dass im Gegensatz zu Mikroglia bei gesunden Mäusen diese Mikroglia zeigten keine normalen Schnittveränderungen, und dies wiederum reduzierte die Anzahl neuer Synapsen, die während einer Lernerfahrung gebildet wurden. Diese Veränderung wirkte sich negativ auf ihre Lernfähigkeit aus.
Postsynaptische dendritische Dornen wurden auch nicht normal umgebaut, und cue-kodierende Neuronen in diesem Teil des Gehirns zeigten keine normalen Aktivitätsniveaus. Zusammen mit Mikroglia, erregende Neuronen und andere Gehirnzelltypen zeigten ähnliche Veränderungen.
Zusätzlich, Die Forscher fanden heraus, dass sich die Konzentrationen von vier Chemikalien im Gehirn der GF-Mäuse veränderten. Diese Chemikalien werden typischerweise mit neuropsychiatrischen Erkrankungen wie Schizophrenie und Autismus-Spektrum-Störung in Verbindung gebracht. Veränderungen dieser Chemikalien sind daher eng mit Veränderungen der Gehirnfunktion verbunden, die wiederum entscheidet, wie wir unsere Umgebung wahrnehmen und wie wir darauf reagieren. Die Tatsache, dass ein verändertes Darmmikrobiom mit etwas so Grundlegendem wie der Gehirnchemie verbunden ist, ist daher wichtig, um das zugrunde liegende Muster zu entschlüsseln. Wie der Forscher Frank Schroeder sagt:„Die Gehirnchemie bestimmt im Wesentlichen, wie wir unsere Umwelt fühlen und auf sie reagieren. und es gibt immer mehr Beweise dafür, dass Chemikalien, die aus Darmmikroben stammen, eine wichtige Rolle spielen.“
Auf zu Stufe 3 – die Forscher versuchten nun, bei Mäusen die normale Lernfähigkeit wiederherzustellen, indem sie Darmorganismen zurücksetzten, um die verlorenen zu ersetzen. in der ersten Gruppe, oder durch Transplantation normaler Mikrobiome, in der GF-Population. Sie waren erfolgreich, wenn das Darmmikrobiom unmittelbar nach der Geburt wieder normalisiert wurde. wobei die behandelten Mäuse normale Lernmuster zeigten. Auf der anderen Seite, die fehlende Verbesserung bei späteren Interventionen legt nahe, dass sofort nach der Geburt des Babys Signale von einem gesunden Darmmikrobiom an das sich entwickelnde Gehirn gesendet werden müssen.
Forscher Conor Liston kommentiert:„Das war eine interessante Erkenntnis, Angesichts der Tatsache, dass viele psychiatrische Erkrankungen, die mit Autoimmunerkrankungen in Verbindung gebracht werden, mit Problemen während der frühen Gehirnentwicklung verbunden sind.“
Der Forscher David Artis sagt:„Die Darm-Hirn-Achse beeinflusst jeden einzelnen Menschen jeden Tag seines Lebens. Niemand hat bisher verstanden, wie IBD und andere chronische Magen-Darm-Erkrankungen das Verhalten und die psychische Gesundheit beeinflussen. Unsere Studie liefert ein neues Verständnis dafür, wie die Mechanismen funktionieren.“
Die Aufklärung der Art und Weise, wie die Darmdysbiose die Funktion des Gehirns auf molekularer und zellulärer Ebene beeinflusst, wird hoffnungsvoll, die Identifizierung von Zielmolekülen oder Signalwegen zur zukünftigen Behandlung betroffener Menschen beschleunigen.
 Kaffee hilft bei der Entwicklung gesunder Darmmikroben und unterstützt den Stuhlgang
Kaffee hilft bei der Entwicklung gesunder Darmmikroben und unterstützt den Stuhlgang
 Nahrung beeinflusst selektiv Darmmikroben, Studienergebnisse
Nahrung beeinflusst selektiv Darmmikroben, Studienergebnisse
 Die Parkinson-Krankheit könnte durch Darmmikroben verhindert werden
Die Parkinson-Krankheit könnte durch Darmmikroben verhindert werden
 Starkes Mikrobiom im frühen Leben in Verbindung mit weniger Atemwegsinfektionen
Starkes Mikrobiom im frühen Leben in Verbindung mit weniger Atemwegsinfektionen
 Apoptose ist ein wichtiger Mediator der Pathogenese bei der Infektion mit dem Coronavirus bei Tieren
Apoptose ist ein wichtiger Mediator der Pathogenese bei der Infektion mit dem Coronavirus bei Tieren
 Menschliches Mikrobiom trimmt Schleimhautglykane,
Menschliches Mikrobiom trimmt Schleimhautglykane,
 Das Bakterienprofil des Darms kann Darmschäden nach einer Strahlentherapie vorhersagen
Wie ein physischer Fingerabdruck, das mikrobielle Muster im Darm kann verwendet werden, um bestimmte Schwachstellen bei Patienten zu identifizieren, die sich einer Strahlentherapie wegen Prostata- ode
Das Bakterienprofil des Darms kann Darmschäden nach einer Strahlentherapie vorhersagen
Wie ein physischer Fingerabdruck, das mikrobielle Muster im Darm kann verwendet werden, um bestimmte Schwachstellen bei Patienten zu identifizieren, die sich einer Strahlentherapie wegen Prostata- ode
 Keine Angst vor der Koloskopie
Wurzelkanäle und Koloskopien haben etwas gemeinsam – sie sind in der Öffentlichkeit allgemein gefürchtet. Aber im Bereich zahnärztlicher Eingriffe und routinemäßiger notwendiger Untersuchungen, bzw, b
Keine Angst vor der Koloskopie
Wurzelkanäle und Koloskopien haben etwas gemeinsam – sie sind in der Öffentlichkeit allgemein gefürchtet. Aber im Bereich zahnärztlicher Eingriffe und routinemäßiger notwendiger Untersuchungen, bzw, b
 Wird das Coronavirus über den Kot übertragen?
Eine verblüffende Studie aus China, in der Zeitschrift veröffentlicht Gastroenterologie im März 2020, berichtet, dass sich das neuartige Coronavirus SARS-CoV-2 sowohl über den Kot als auch über den
Wird das Coronavirus über den Kot übertragen?
Eine verblüffende Studie aus China, in der Zeitschrift veröffentlicht Gastroenterologie im März 2020, berichtet, dass sich das neuartige Coronavirus SARS-CoV-2 sowohl über den Kot als auch über den