Tarmmikrobiota påvirker den måde, hvorpå mange kropslige processer fungerer, såsom immunfunktion, normalt stofskifte, og udviklingen af organismen. Det påvirker også værtens adfærd, herunder social aktivitet og stressreaktioner, som er forbundet med mange forskellige lidelser i hjernen og/eller sindet. Imidlertid, der er ikke meget viden om de underliggende mekanismer, hvormed tarmbakterier kan ændre måden, hjernecellerne fungerer på, eller adfærden hos den større organisme.
Tidligere forskning giver stærke indikationer på sammenhængen mellem tarmsundhed og en række forskellige sygdomme som ASD og posttraumatisk stresslidelse. Mange undersøgelser har vist, at autoimmune sygdomme er knyttet til et unormalt tarmmikrobiom, og også til flere psykiatriske og neurologiske tilstande. For eksempel, inflammatorisk tarmsygdom, multipel sklerose og psoriasis er alle lidelser i autoimmunitet, og disse personer har en højere risiko for at have et lavere antal forskellige tarmbakterier, samt større odds for angst, humørsvingninger og depression. Almindelige gener ser også ud til at være til stede under både psykiatriske og autoimmune tilstande.
I denne undersøgelse, forskerne kiggede på hjernen hos to typer mus med unormal tarmmikrobiota:mus, der havde modtaget antibiotika for at reducere bakterievækst i tarmen, eller mus, der er avlet i et totalt sterilt miljø for at være bakteriefri (GF). De udsatte først disse muspopulationer for en fare, og fjernede det derefter. Ved at studere læringsresponserne i disse muspopulationer, de fandt ud af, at begge viste en nedsat evne til at lære, at en fare, der truede dem, ikke længere var til frygt (kaldet frygtudslettelseslæring). Med andre ord, normale mus udvikler en refleks frygtrespons på en truet fare, men efterhånden som stimulus ikke formodede nogen skade efter eksponering, deres betingede frygtrespons falder. Denne indlæring var ikke tydelig hos GF eller antibiotikabehandlede mus, der fortsatte med at vise betingede frygtresponser over tid.
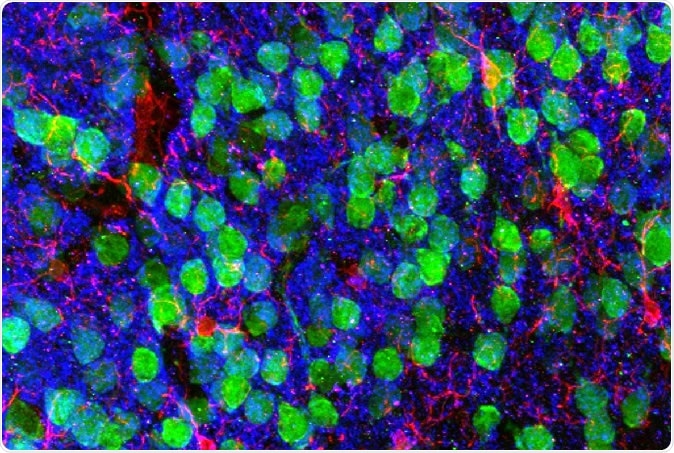 Billeddannelse af hjernen. Medial præfrontal cortex, der demonstrerer kortikale neuroner (grøn), microglia (rød), og den postsynaptiske markør PSD95 (blå). Billede med tilladelse fra Dr. Christopher Parkhurst og David Artis (WCM).
Billeddannelse af hjernen. Medial præfrontal cortex, der demonstrerer kortikale neuroner (grøn), microglia (rød), og den postsynaptiske markør PSD95 (blå). Billede med tilladelse fra Dr. Christopher Parkhurst og David Artis (WCM). For at finde ud af hvorfor, forskerne sekventerede RNA inden for mikroglia, hjernens immunceller. RNA er det mellemliggende molekyle mellem den genetiske plan i kernen og det endelige protein i cytoplasmaet, fremstillet af det kodede gen. Således viser en RNA -sekvens et gen udtrykt i den pågældende celle.
RNA -sekventering viste et andet mønster for genekspression i hjernecellerne i disse muspopulationer, hvilket igen påvirkede den normale ombygning, der sker som en del af læringen. Hjerneceller danner forbindelser eller synapser for at videregive information indbyrdes. Imidlertid, efterhånden som læringen skrider frem, visse synapser fjernes og andre tilføjes, ifølge impulstrafikken langs den vej. Dette kaldes synapsbeskæring og er en vigtig proces i læring.
Ved undersøgelse af forskellene i genekspression i den mediale præfrontale cortex i musens hjerne, forskerne opdagede, at i modsætning til mikroglia hos raske mus, disse mikroglia viste ikke normale beskæringsændringer, og dette reducerede igen antallet af nye synapser, der blev dannet under en læringsoplevelse. Denne ændring påvirkede deres evne til at lære negativt.
Postsynaptiske dendritiske rygsøjler blev heller ikke ombygget normalt, og cue-kodende neuroner i denne del af hjernen undlod at vise normale aktivitetsniveauer. Sammen med microglia, excitatoriske neuroner og andre hjernecelletyper viste lignende ændringer.
Ud over, forskerne fandt ud af, at der var ændringer i niveauerne af fire kemikalier i hjernen på GF -musene. Disse kemikalier er typisk forbundet med neuropsykiatriske sygdomme, såsom skizofreni og autismespektrumforstyrrelse. Ændringer i disse kemikalier er derfor tæt forbundet med ændringer i hjernens funktion, som igen bestemmer, hvordan vi fornemmer vores omgivelser, og hvordan vi reagerer på dem. Det faktum, at et ændret tarmmikrobiom er knyttet til noget så fundamentalt som hjernekemi, er derfor vigtigt for at opklare det underliggende mønster. Som forsker Frank Schroeder siger, "Hjernekemi bestemmer i det væsentlige, hvordan vi føler og reagerer på vores miljø, og beviser bygger på, at kemikalier afledt af tarmmikrober spiller en stor rolle. ”
Videre til trin 3 - forskerne forsøgte nu at genoprette normal indlæringskapacitet hos mus ved at lægge tarmorganismer tilbage for at erstatte dem, der gik tabt, i den første gruppe, eller ved at transplantere normale mikrobiomer, i GF -befolkningen. Det lykkedes, hvis tarmmikrobiomet blev genoprettet til det normale umiddelbart efter fødslen, med de behandlede mus, der viser normale læringsmønstre. På den anden side, den manglende forbedring med senere indgreb tyder på det væsentlige behov for signaler fra et sundt tarmmikrobiom til den udviklende hjerne, så snart barnet er født.
Forsker Conor Liston kommenterer, ”Dette var et interessant fund, i betragtning af at mange psykiatriske tilstande, der er forbundet med autoimmun sygdom, er forbundet med problemer under tidlig hjernens udvikling. ”
Forsker David Artis siger, ”Tarm-hjerne-aksen påvirker hvert eneste menneske hver dag i deres liv. Ingen har endnu forstået, hvordan IBD og andre kroniske gastrointestinale tilstande påvirker adfærd og mental sundhed. Vores undersøgelse giver et nyt stykke forståelse for, hvordan mekanismerne fungerer. ”
Afklaringen af den måde tarmdysbiose påvirker hjernens funktion på molekylært og cellulært niveau vil, forhåbentlig, fremskynde identifikationen af målmolekyler eller veje til behandling af berørte mennesker i fremtiden.
 Sædmikrobiom afsløret med RNA -sekventering
Sædmikrobiom afsløret med RNA -sekventering
 Strategisering af pædiatrisk sundhedsberedskab til den anden bølge af COVID-19-pandemien
Strategisering af pædiatrisk sundhedsberedskab til den anden bølge af COVID-19-pandemien
 Hvorfor du bør inkludere naturlige fiberkilder i din kost
Hvorfor du bør inkludere naturlige fiberkilder i din kost
 Tarmmikrobiom ændrer sig ved tilberedning af vegetabilske fødevarer,
Tarmmikrobiom ændrer sig ved tilberedning af vegetabilske fødevarer,
 Forskere bruger fagterapi til succesfuld behandling af alkoholisk leversygdom
Forskere bruger fagterapi til succesfuld behandling af alkoholisk leversygdom
 Crohns sygdom
Crohns sygdom
 Mennesker kontra vira - Kan vi undgå udryddelse i nær fremtid?
Ekspert hævder, at menneskeskabte ændringer i miljøet kan føre til fremkomsten af patogener, ikke kun udefra, men også fra vores eget mikrobiom, som kan bane vejen for storstilet ødelæggelse af menn
Mennesker kontra vira - Kan vi undgå udryddelse i nær fremtid?
Ekspert hævder, at menneskeskabte ændringer i miljøet kan føre til fremkomsten af patogener, ikke kun udefra, men også fra vores eget mikrobiom, som kan bane vejen for storstilet ødelæggelse af menn
 Råt foder til kæledyr er en risiko for mennesker og dyr
Forskere har fundet i en ny undersøgelse, at hunde og katte, der spiser råt kød, kan sprede antibiotikaresistente bakteriestammer til mennesker. Deres undersøgelse med titlen, “Råt kødbaseret kost til
Råt foder til kæledyr er en risiko for mennesker og dyr
Forskere har fundet i en ny undersøgelse, at hunde og katte, der spiser råt kød, kan sprede antibiotikaresistente bakteriestammer til mennesker. Deres undersøgelse med titlen, “Råt kødbaseret kost til
 Lungemikrober kan hjælpe med at forudsige resultater hos alvorligt syge
En ny undersøgelse offentliggjort i American Journal of Respiratory and Critical Care Medicine viser, at registrering af den måde, organismerne, der lever i lungerne, ændrer i type og antal, kunne a
Lungemikrober kan hjælpe med at forudsige resultater hos alvorligt syge
En ny undersøgelse offentliggjort i American Journal of Respiratory and Critical Care Medicine viser, at registrering af den måde, organismerne, der lever i lungerne, ændrer i type og antal, kunne a