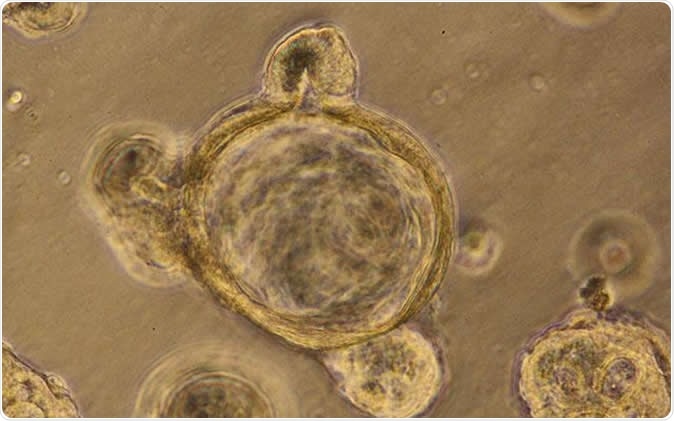
 Jedná sa o mini-črevný organoid generovaný v laboratóriu z ľudských kmeňových buniek. Obrazový kredit:UC San Diego Health Sciences
Jedná sa o mini-črevný organoid generovaný v laboratóriu z ľudských kmeňových buniek. Obrazový kredit:UC San Diego Health Sciences Tím zistil, že môžu použiť trojrozmerné črevné bunky v Petriho miske vo forme črevných organoidov a testovať účinnosť liekov na deravé črevá. Tieto organoidy môžu úspešne obnoviť molekulárny systém v laboratóriu vrátane buniek črevnej výstelky atď. Tieto bunky sú normálne utesnené, aby sa zabránilo úniku. Za určitých chorobných stavov, tesnenia môžu byť nefunkčné, čo môže viesť k vytečeniu čriev, napísali vedci. Tieto stavy sa bežne vyskytujú u rakoviny a u starších ľudí, vysvetlili. V tomto stave môže dôjsť k úniku mikróbov, ako aj životne dôležitých molekúl z čriev do brušných dutín.
Na vytvorenie týchto organoidov tím použil darované črevné bunky od pacientov. Črevá majú typicky hrebeň a krypty s vrcholmi a údoliami. Z krypt mohli izolovať kmeňové bunky. Tieto bunky boli použité na vytvorenie trojrozmerných organoidov v laboratóriách, napísal tím. Kmeňové bunky rástli a stali sa z nich štyri typy buniek, ktoré sú normálne zaznamenané v čreve. Tieto bunky sa potom zrolovali a stali sa malými vnútornosťami v Petriho miskách, ktoré napísali. Organoidy bolo teraz možné testovať.
Môže existovať niekoľko chorobných stavov, ktoré vedú k oslabeniu väzieb medzi bunkami a spojovacími bunkami medzi dvoma črevnými bunkami, napísali vedci. To vedie k úniku molekúl z čriev a k úniku mikróbov. To môže spustiť imunitný systém a viesť k stavu chronického zápalu. Zápalové ochorenia čriev, ako je ulcerózna kolitída a Crohnova choroba, ako aj ďalšie stavy, ako je poškodenie pečene, rakoviny, cukrovka, ateroskleróza, Vedci tvrdia, že artritída a dokonca demencia môžu byť spojené s netesnými črevnými bunkami. Do dnešného dňa nebolo možné tento problém študovať, nehovoriac o vyriešení, napísali vedci. Táto nová štúdia konečne otvára cestu, kde by sa tento stav dal replikovať v laboratóriu a študovať na jeho molekulárnej úrovni.
Pre túto štúdiu tím vzal mini organoidy a otvoril zvinuté gule, aby odhalil črevný povrch. Cez tieto použili baktérie a iné stresory na oslabenie spojovacích buniek a vytvorenie netesných otvorov. Teraz mohli študovať molekulárne mechanizmy a lieky, ktoré by mohli pomôcť utiahnuť tieto väzby medzi bunkami, aby sa zabránilo úniku.
Vedci Lekárskej fakulty Kalifornskej univerzity v San Diegu teda použili 3D modely ľudských čriev v Petriho miskách. Tieto bunky darovali skutoční pacienti s netesným črevom. Bunky boli vytvorené do 3D mini organoidov, aby mohli napodobňovať skutočné črevá. Tím potom našiel určité biomarkery, ktoré boli charakteristické pre črevá, ktoré mali problém s únikom. Tím špekuluje, že tieto markery by mohli pomôcť vedcom diagnostikovať tento stav včas a tiež sledovať progresiu ochorenia v priebehu času.
Na svoju štúdiu použili bežne používaný liek na cukrovku Metformin, aby sa pokúsili uzavrieť úniky v črevných stenách. Štúdia, ktorú viedol Pradipta Ghosh, MD, profesor bunkovej a molekulárnej medicíny na UC San Diego School of Medicine a Moores Cancer Center, a senior autor Soumita Das, PhD., docent patológie na Lekárskej fakulte UC San Diego, odhalil, že tento bežne používaný liek by mohol pomôcť pacientom s deravým črevom.
Ghosh a Das mali predtým, v ďalšej štúdii ukázal, že mechanizmus nazývaný signálna dráha polarity napätia by mohol pomôcť uzavrieť medzery medzi bunkami a zabrániť úniku. V tejto štúdii tiež poznamenali, že spojenia a väzby medzi bunkami sa rozpadli v dôsledku stresu.
Táto nová štúdia odhalila, že metformín môže fungovať na aktivácii určitých chemických reakcií, ktoré by mohli tieto spoje utiahnuť a zabrániť tak úniku. Tím tvrdí, že ich úspech bol zatiaľ videný iba v Petriho miskách na mini organoidoch čreva. Potrebujú ho replikovať u ľudí, aby zistili, či liek skutočne môže pomôcť pacientom s deravým črevným stavom. Dodali však, že úspech lieku v týchto organoidech je veľkým krokom k dokázaniu, že liek skutočne môže pomôcť. Metformín, napísali, že zvyšujú hladiny proteínu nazývaného oklúzia, ktorý môže sprísniť spoje medzi bunkami. Ak bude úspešný, mohlo by to pomôcť veľkému počtu pacientov, vysvetlili.
Ghosh povedal:"Veľa výskumu sa robí na myšiach, ktoré sú inbredné, takže sú geneticky identické," všetko v jednej klietke, jesť rovnakú diétu, s cieľom odstrániť tieto premenné zo štúdií. Laboratórne myši sú však zo dňa na deň oveľa viac štandardizované ako ten istý človek, alebo pacientov, ktorých vidíme na klinikách. Tu, náš model je lepšou reprezentáciou ľudstva. Na druhej strane, znamená to tiež, že každý organoid je svoj vlastný jedinečný experiment. Aby sme mohli urobiť akékoľvek tvrdenie, musíme otestovať mnoho organoidov, čo sme urobili v našej štúdii. “ Dodal Das, "Myslím, že by ste ťažko hľadali chorobu, pri ktorej by nebol príčinou systémový zápal." Preto, Aj keď je toľko vecí, ktoré stále nevieme, sme nadšení zo širokého potenciálu tohto modelu a týchto zistení, ktoré sa otvárajú pre vývoj personalizovaných terapeutík deravého čreva, ktoré sa zameriavajú na AMPK a signálnu cestu polarity stresu. “
 Črevný mikrobióm sa mení varením rastlinných potravín,
Črevný mikrobióm sa mení varením rastlinných potravín,
 Štúdia s dvojčatami ukazuje, že symptómy COVID-19 majú genetický prínos
Štúdia s dvojčatami ukazuje, že symptómy COVID-19 majú genetický prínos
 Ultrafialové svetlo B je dobré pre črevný mikrobióm
Ultrafialové svetlo B je dobré pre črevný mikrobióm
 Elektronická pilulka na detekciu plynu na diagnostiku gastrointestinálnych ochorení
Elektronická pilulka na detekciu plynu na diagnostiku gastrointestinálnych ochorení
 Otvorenie úzkeho pažeráka
Otvorenie úzkeho pažeráka
 Črevný mikrobióm spojený s problémami správania u detí
Črevný mikrobióm spojený s problémami správania u detí
 Model novonarodených myší poskytuje vodítka k príčine devastujúcej črevnej choroby u anemických preemií
Lekári majú už dlho podozrenie, že transfúzie červených krviniek podávané predčasne narodeným deťom s anémiou môžu ohroziť rozvoj nekrotizujúcej enterokolitídy, alebo NEC, potenciálne smrteľné zápalov
Model novonarodených myší poskytuje vodítka k príčine devastujúcej črevnej choroby u anemických preemií
Lekári majú už dlho podozrenie, že transfúzie červených krviniek podávané predčasne narodeným deťom s anémiou môžu ohroziť rozvoj nekrotizujúcej enterokolitídy, alebo NEC, potenciálne smrteľné zápalov
 Perfectus Biomed bude vystavovať na konferencii IPS v Liverpoole
Tím Perfectus Biomed bude tento mesiac vystavovať na konferencii Spoločnosti pre prevenciu infekcií (IPS) v Liverpoole. Konferencia sa uskutoční v aréne a kongresovom centre v Liverpoole v dňoch 22. -
Perfectus Biomed bude vystavovať na konferencii IPS v Liverpoole
Tím Perfectus Biomed bude tento mesiac vystavovať na konferencii Spoločnosti pre prevenciu infekcií (IPS) v Liverpoole. Konferencia sa uskutoční v aréne a kongresovom centre v Liverpoole v dňoch 22. -
 Strava a výživa ovplyvňujú mikrobiómy v sliznici hrubého čreva
Strava je dôležitá pre udržanie zdravia ľudí, ale jeho základný mechanizmus ešte nie je úplne pochopený. Teraz, tím vedcov osvetľuje spojenie stravy a zdravia, a má to niečo spoločné s mikrobiómovým z
Strava a výživa ovplyvňujú mikrobiómy v sliznici hrubého čreva
Strava je dôležitá pre udržanie zdravia ľudí, ale jeho základný mechanizmus ešte nie je úplne pochopený. Teraz, tím vedcov osvetľuje spojenie stravy a zdravia, a má to niečo spoločné s mikrobiómovým z