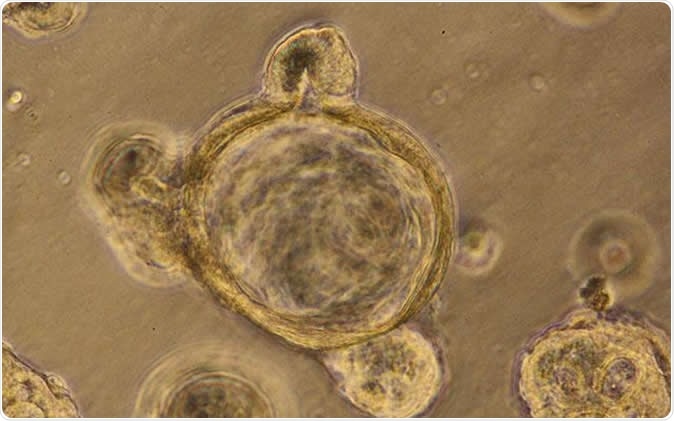
 Dit is een mini-darmorganoïde die in het laboratorium is gegenereerd uit menselijke stamcellen. Afbeelding tegoed:UC San Diego Health Sciences
Dit is een mini-darmorganoïde die in het laboratorium is gegenereerd uit menselijke stamcellen. Afbeelding tegoed:UC San Diego Health Sciences Het team ontdekte dat ze driedimensionale darmcellen in een petrischaal in de vorm van darmorganoïden konden gebruiken en de medicijnen konden testen op hun werkzaamheid op lekkende ingewanden. Deze organoïden kunnen met succes het moleculaire systeem in het laboratorium recreëren, inclusief darmwandcellen enz. Deze cellen zijn normaal gesproken verzegeld om lekkage te voorkomen. Bij bepaalde ziektebeelden de afdichtingen kunnen disfunctioneel zijn, wat leidt tot lekkende ingewanden, schreven de onderzoekers. Deze aandoeningen worden vaak gezien bij kankers en bij ouderen, legden ze uit. In deze toestand kunnen er zowel microben als vitale moleculen uit de darmen in de buikholte lekken.
Om deze organoïden te maken, gebruikte het team gedoneerde darmcellen van de patiënten. De darmen hebben meestal toppen en crypten met pieken en dalen. Uit de crypten konden ze stamcellen isoleren. Deze cellen werden gebruikt om de driedimensionale organoïden in de laboratoria te maken, schreef het team. De stamcellen groeiden uit tot vier soorten cellen die normaal gesproken in de darm worden opgemerkt. Deze cellen rolden vervolgens op om mini-ingewanden te worden in de petrischalen die ze schreven. Nu konden de organoïden worden getest.
Er kunnen verschillende ziektetoestanden zijn die leiden tot verzwakking van de bindingen tussen de cellen en de verbindingscellen tussen twee darmcellen, schreven de onderzoekers. Dit leidt tot lekkage van de moleculen vanuit de darmen en tot lekkage van microben. Dit kan het immuunsysteem activeren, wat leidt tot een toestand van chronische ontsteking. Inflammatoire darmaandoeningen zoals colitis ulcerosa en de ziekte van Crohn, evenals andere aandoeningen zoals leverbeschadiging, kankers, suikerziekte, atherosclerose, artritis en zelfs dementie kunnen in verband worden gebracht met lekkende darmcellen, zeggen onderzoekers. Tot op heden was er geen manier om dit probleem te bestuderen, laat staan opgelost, schreven de onderzoekers. Deze nieuwe studie effent eindelijk een manier waarop de aandoening in het laboratorium kan worden gerepliceerd en op moleculair niveau kan worden bestudeerd.
Voor deze studie nam het team de mini-organoïden en opende de opgerolde ballen om het darmoppervlak bloot te leggen. Hierover gebruikten ze bacteriën en andere stressoren om de junctionele cellen te verzwakken en lekkende openingen te creëren. Nu konden ze de moleculaire mechanismen bestuderen, evenals de medicijnen die zouden kunnen helpen deze bindingen tussen de cellen te verstevigen om lekkage te voorkomen.
Onderzoekers van de University of California San Diego School of Medicine gebruikten daarom 3D-modellen van menselijke darmen in de petrischalen. Deze cellen zijn geschonken door echte patiënten die lijden aan een lekkende darm. De cellen werden gemaakt in 3D mini-organoïden, zodat ze de echte darmen konden nabootsen. Het team vond vervolgens bepaalde biomarkers die kenmerkend waren voor darmen die het lekkageprobleem hadden. Het team speculeert dat deze markers onderzoekers kunnen helpen deze aandoening vroeg te diagnosticeren en ook de progressie van de ziekte in de loop van de tijd te volgen.
Voor hun onderzoek gebruikten ze een veelgebruikt diabetesmedicijn Metformine om de lekken in de darmwand te dichten. De studie onder leiding van Pradipta Ghosh, MD, hoogleraar cellulaire en moleculaire geneeskunde aan de UC San Diego School of Medicine en Moores Cancer Center, en senior auteur Soumita Das, doctoraat, universitair hoofddocent pathologie aan de UC San Diego School of Medicine, onthulde dat dit veelgebruikte medicijn patiënten met een lekkende darm zou kunnen helpen.
Ghosh en Das hadden eerder, in een andere studie toonde aan dat een mechanisme dat de signaalroute voor stress-polariteit wordt genoemd, kan helpen de openingen tussen de cellen te dichten en lekkage te voorkomen. In dat onderzoek hadden ze ook opgemerkt dat de verbindingen en bindingen tussen de cellen door de stress uit elkaar vielen.
Deze nieuwe studie onthulde dat Metformine bepaalde chemische reacties kan activeren die deze verbindingen kunnen vernauwen en zo lekkage kunnen voorkomen. Het team zegt dat hun succes tot nu toe alleen is gezien in de petrischalen op de mini-organoïden van de darm. Ze moeten het bij mensen repliceren om te zien of het medicijn patiënten met lekkende darmaandoeningen echt kan helpen. Ze voegden er echter aan toe dat het succes van het medicijn in deze organoïden een grote stap is om te bewijzen dat het medicijn daadwerkelijk zou kunnen helpen. Metformine, ze schreven het verhogen van de niveaus van een eiwit dat occlusie wordt genoemd en dat de verbindingen tussen cellen kan verstevigen. Indien succesvol, dit zou een groot aantal patiënten kunnen helpen, legden ze uit.
Ghosh zei, “Er wordt veel onderzoek gedaan bij muizen die zijn ingeteeld zodat ze genetisch identiek zijn, allemaal in dezelfde kooi, hetzelfde dieet eten, om deze variabelen uit de studies te verwijderen. Maar laboratoriummuizen zijn van dag tot dag veel meer gestandaardiseerd dan dezelfde mens, of patiënten die we in de klinieken zien. Hier, ons model is een betere representatie van de mensheid. Anderzijds, het betekent ook dat elke organoïde zijn eigen unieke experiment is. We moeten veel organoïden testen om enige claim te kunnen maken, wat we in onze studie hebben gedaan.” Das heeft toegevoegd, “Ik denk dat het moeilijk zal zijn om een ziekte te vinden waarbij systemische ontsteking geen aanjager is. Dat is waarom, ook al zijn er zoveel dingen die we nog niet weten, we zijn enthousiast over het brede potentieel van dit model en deze bevindingen openen voor het ontwikkelen van gepersonaliseerde lekkende darmtherapieën die gericht zijn op AMPK en de stress-polariteit signaleringsroute."
 Biologische appels hebben probiotische eigenschappen
Biologische appels hebben probiotische eigenschappen
 FLUOstar Omega gebruiken om nieuwe darmbacteriën te bestuderen die onze gezondheid kunnen beïnvloeden
FLUOstar Omega gebruiken om nieuwe darmbacteriën te bestuderen die onze gezondheid kunnen beïnvloeden
 Spingif-peptide kan helpen pijn bij het prikkelbare darm syndroom te stoppen
Spingif-peptide kan helpen pijn bij het prikkelbare darm syndroom te stoppen
 Orgaanchiptechnologie verbetert de studie van de darm voor gepersonaliseerde geneeskunde
Orgaanchiptechnologie verbetert de studie van de darm voor gepersonaliseerde geneeskunde
 Nieuw onderzoek identificeert een verband tussen het darmmicrobioom en beroertes
Nieuw onderzoek identificeert een verband tussen het darmmicrobioom en beroertes
 Veranderingen in de darmbacteriën beïnvloeden de resultaten van de lupusbehandeling tijdens de zwangerschap
Veranderingen in de darmbacteriën beïnvloeden de resultaten van de lupusbehandeling tijdens de zwangerschap
 Diagnose van virale infecties met behulp van technologieën op micro- en nanoschaal
De behoefte aan bevolkingsbrede, snel, gevoelig, en kosteneffectieve diagnostische tests zijn aanzienlijk toegenomen als gevolg van het ernstige acute respiratoire syndroom coronavirus 2 (SARS-CoV-2),
Diagnose van virale infecties met behulp van technologieën op micro- en nanoschaal
De behoefte aan bevolkingsbrede, snel, gevoelig, en kosteneffectieve diagnostische tests zijn aanzienlijk toegenomen als gevolg van het ernstige acute respiratoire syndroom coronavirus 2 (SARS-CoV-2),
 Darmmicrobioom verandert bij het koken van plantaardig voedsel,
zegt nieuwe studie Toen onderzoekers van UC San Francisco en Harvard samenwerkten om erachter te komen hoe het darmmicrobioom wordt beïnvloed door koken, ze ontdekten dat er zowel bij mensen als bij m
Darmmicrobioom verandert bij het koken van plantaardig voedsel,
zegt nieuwe studie Toen onderzoekers van UC San Francisco en Harvard samenwerkten om erachter te komen hoe het darmmicrobioom wordt beïnvloed door koken, ze ontdekten dat er zowel bij mensen als bij m
 Nieuwe tool om het darmmicrobioom te ontcijferen
De miljoenen bacteriën die zich in de darmen bevinden, spelen een zeer belangrijke rol bij gezondheid en ziekte. Echter, een constant probleem was het gebrek aan begrip van de feitelijke samenstelling
Nieuwe tool om het darmmicrobioom te ontcijferen
De miljoenen bacteriën die zich in de darmen bevinden, spelen een zeer belangrijke rol bij gezondheid en ziekte. Echter, een constant probleem was het gebrek aan begrip van de feitelijke samenstelling