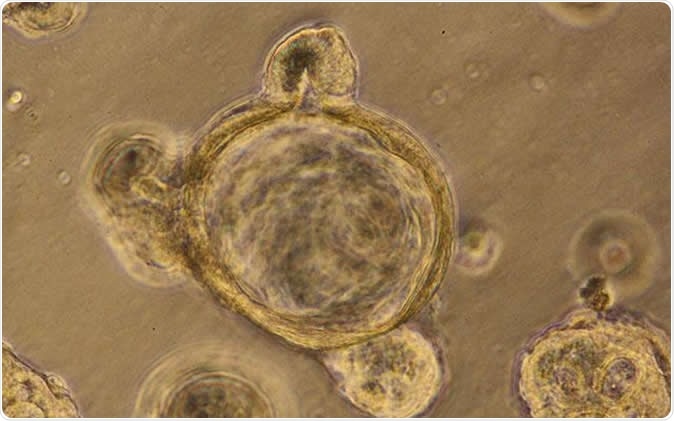
 Dette er en mini-tarmorganoid generert i laboratoriet fra menneskelige stamceller. Bildekreditt:UC San Diego Health Sciences
Dette er en mini-tarmorganoid generert i laboratoriet fra menneskelige stamceller. Bildekreditt:UC San Diego Health Sciences Teamet fant ut at de kunne bruke tredimensjonale tarmceller i en petriskål i form av tarmorganoider og teste stoffene for deres effekt på lekkende tarm. Disse organoidene kan lykkes med å gjenskape det molekylære systemet i laboratoriet, inkludert tarmforingsceller etc. Disse cellene er normalt forseglet for å forhindre lekkasje. Ved visse sykdomstilstander, selene kan være dysfunksjonelle og føre til lekkasje i tarmen, skrev forskerne. Disse tilstandene er ofte sett hos kreftformer og blant eldre, forklarte de. I denne tilstanden kan det være lekkasje av mikrober så vel som vitale molekyler fra tarmen inn i bukhulen.
For å lage disse organoidene brukte teamet donerte tarmceller fra pasientene. Tarmene har vanligvis kam og krypter med topper og daler. Fra kryptene kunne de isolere stamceller. Disse cellene ble brukt til å lage de tredimensjonale organoidene i laboratoriene, laget skrev. Stamcellene vokste til å bli fire typer celler som normalt er notert i tarmen. Disse cellene rullet deretter sammen for å bli mini -tarm i petriskålene de skrev. Nå kunne organoidene testes.
Det kan være flere sykdomstilstander som fører til svekkelse av bindingene mellom cellene og forbindelsescellene mellom to tarmceller, skrev forskerne. Dette fører til lekkasje av molekylene fra tarmene, samt lekkasje av mikrober. Dette kan utløse immunsystemet som fører til en tilstand av kronisk betennelse. Inflammatoriske tarmsykdommer som ulcerøs kolitt og Crohns sykdom samt andre tilstander som leverskade, kreft, diabetes, åreforkalkning, forskere sier leddgikt og til og med demens kan være assosiert med utette tarmceller. Hittil har det ikke vært mulig å studere dette problemet, enn si løst, skrev forskerne. Denne nye studien baner endelig en måte der tilstanden kan replikeres i laboratoriet og studeres på molekylært nivå.
For denne studien tok teamet miniorganoider og åpnet de rullede ballene for å avsløre tarmoverflaten. Over disse brukte de bakterier og andre stressorer for å svekke forbindelsescellene og skape utette åpninger. Nå kunne de studere de molekylære mekanismene så vel som legemidlene som kan bidra til å stramme disse bindingene mellom cellene for å forhindre lekkasje.
University of California San Diego School of Medicine forskere brukte dermed 3D -modeller av tarmene i petriskålene. Disse cellene ble donert av virkelige pasienter som lider av tarmlekkasje. Cellene ble skapt til 3D miniorganoider slik at de kunne etterligne de virkelige tarmene. Teamet fant deretter visse biomarkører som var karakteristiske for tarmene som hadde lekkasjeproblemet. Teamet spekulerer i at disse markørene kan hjelpe forskere med å diagnostisere denne tilstanden tidlig og også spore sykdommens utvikling over tid.
I studien brukte de en vanlig medisin mot diabetes for å prøve å tette lekkasjene i tarmveggene. Studien ledet av Pradipta Ghosh, MD, professor i cellulær og molekylær medisin ved UC San Diego School of Medicine og Moores Cancer Center, og seniorforfatter Soumita Das, PhD, førsteamanuensis i patologi ved UC San Diego School of Medicine, avslørte at dette ofte brukte stoffet kan hjelpe pasienter med lekkasje i tarmen.
Ghosh og Das hadde tidligere, i en annen studie viste at en mekanisme kalt stress-polaritetssignalveien kan bidra til å lukke hullene mellom cellene og forhindre lekkasje. I den studien hadde de også bemerket at forbindelsene og bindingene mellom cellene løsnet på grunn av stresset.
Denne nye studien avslørte at Metformin kan arbeide for å aktivere visse kjemiske reaksjoner som kan stramme disse veikryssene og dermed forhindre lekkasje. Teamet sier at suksessen deres bare har blitt sett i petriskålene på tarmens miniorganoider ennå. De må replikere det hos mennesker for å se om stoffet faktisk kan hjelpe pasienter med lekkende tarmtilstander. De la imidlertid til at suksessen til stoffet i disse organoidene er et stort skritt i å bevise at stoffet faktisk kan hjelpe. Metformin, de skrev øker nivåene av et protein som kalles okklusjon som kan stramme kryssene mellom cellene. Hvis det lykkes, Dette kan hjelpe et stort antall pasienter, forklarte de.
Ghosh sa, "Det forskes mye på mus som er innavlet slik at de er genetisk identiske, alle i samme bur, spise det samme kostholdet, for å fjerne disse variablene fra studiene. Men laboratoriemus er langt mer standardiserte enn det samme mennesket fra dag til dag, eller pasienter vi ser på klinikkene. Her, modellen vår er en bedre representasjon av menneskeheten. På den andre siden, det betyr også at hvert organoid er sitt eget unike eksperiment. Vi må teste mange organoider for å kunne påstå noe, som vi gjorde i studien vår. ” Das la til, "Jeg tror du vil bli hardt presset for å finne en sykdom der systemisk betennelse ikke er en driver. Derfor, selv om det er så mange ting vi fortsatt ikke vet, Vi er begeistret for det brede potensialet denne modellen og disse funnene åpner for å utvikle personlig lekkasje i tarmen som er rettet mot AMPK og signalveien for stress-polaritet. ”
 Plantebasert diett kan helbrede din revmatoid artritt
Plantebasert diett kan helbrede din revmatoid artritt
 Rotavirus -vaksinasjon er ikke knyttet til risiko for type 1 diabetes mellitus
Rotavirus -vaksinasjon er ikke knyttet til risiko for type 1 diabetes mellitus
 Mor-til-baby SARS-CoV-2-overføring under graviditet mulig, men sjelden,
Mor-til-baby SARS-CoV-2-overføring under graviditet mulig, men sjelden,
 Studier knytter gjæret grønnsakskonsum til lav dødelighet av COVID-19
Studier knytter gjæret grønnsakskonsum til lav dødelighet av COVID-19
 Plantebaserte dietter forbedrer hjertehelsen via tarmmikrobiomet
Plantebaserte dietter forbedrer hjertehelsen via tarmmikrobiomet
 Hvis du er over 50,
Hvis du er over 50,
 Tiopuriner kan hjelpe til med å stoppe virusreplikasjon hos menneskelige koronavirus
Forskere fra Institutt for mikrobiologi og immunologi, Dalhousie universitet, University of Calgary, og Institutt for biokjemi og molekylærbiologi, University of British Columbia, Canada, jobbet med m
Tiopuriner kan hjelpe til med å stoppe virusreplikasjon hos menneskelige koronavirus
Forskere fra Institutt for mikrobiologi og immunologi, Dalhousie universitet, University of Calgary, og Institutt for biokjemi og molekylærbiologi, University of British Columbia, Canada, jobbet med m
 Gassdetekterende elektronisk pille for diagnose av gastrointestinale plager
Forskere fra RMIT University, Melbourne, har laget en elektronisk pille som kan oppdage spesielle gasser i tarmen og hjelpe leger med å diagnostisere gastrointestinale plager som irritabel tarm.
Gassdetekterende elektronisk pille for diagnose av gastrointestinale plager
Forskere fra RMIT University, Melbourne, har laget en elektronisk pille som kan oppdage spesielle gasser i tarmen og hjelpe leger med å diagnostisere gastrointestinale plager som irritabel tarm.
 Hvite blodlegemer og deres rolle i hjernen
I en banebrytende studie, en gruppe internasjonale forskere har funnet ut at hjernen har spesifikke interne immunceller som hjelper i normal hjernens utvikling og spiller en rolle i visse nevrologiske
Hvite blodlegemer og deres rolle i hjernen
I en banebrytende studie, en gruppe internasjonale forskere har funnet ut at hjernen har spesifikke interne immunceller som hjelper i normal hjernens utvikling og spiller en rolle i visse nevrologiske