 Storosios žarnos vėžys yra trečia pagrindinė vėžio priežastis JAV.
Storosios žarnos vėžys yra trečia pagrindinė vėžio priežastis JAV.Gaubtinės žarnos vėžio požymiai ir simptomai paprastai nėra specifiniai. Kitaip tariant, požymiai ir simptomai gali atsirasti dėl įvairių sąlygų. Kai gaubtinės žarnos vėžys nustatomas ankstyvose stadijose, jis gali net nesukelti simptomų. Simptomai taip pat gali skirtis priklausomai nuo konkrečios gaubtinės žarnos vietos, kurioje yra navikas.
Kai kurie gaubtinės žarnos vėžio simptomai ir požymiai yra:

Kiekvieną dieną mūsų kūne vyksta didžiulis naikinimo ir taisymo procesas. Žmogaus kūną sudaro apie 15 trilijonų ląstelių, o kasdien milijardai ląstelių susidėvi arba sunaikinamos. Daugeliu atvejų kiekvieną kartą, kai ląstelė sunaikinama, kūnas sukuria naują ląstelę, kuri ją pakeis, bandydamas sukurti ląstelę, kuri būtų tobula sunaikintos ląstelės kopija, nes pakaitinė ląstelė turi atlikti tą pačią funkciją kaip ir sunaikinta ląstelė. Sudėtingo ląstelių keitimo proceso metu įvyksta daug klaidų. Nepaisant nepaprastai elegantiškų klaidų prevencijos sistemų, korpusas vis tiek kasdien daro dešimtis tūkstančių klaidų keisdamas ląsteles arba dėl atsitiktinių klaidų, arba dėl to, kad pakeitimo procesui daromas išorinis spaudimas, skatinantis klaidas. Dauguma šių klaidų yra ištaisomos papildomomis elegantiškomis sistemomis arba dėl klaidos naujai pagaminta ląstelė miršta ir susidaro kita normali nauja ląstelė. Tačiau kartais daroma klaida ir ji neištaisoma. Daugelis neištaisytų klaidų turi mažai įtakos sveikatai, tačiau jei dėl klaidos naujai pagaminta ląstelė gali dalytis nepriklausomai nuo normalių ląstelių augimą kontroliuojančių patikrinimų ir balansų, ta ląstelė gali pradėti nekontroliuojamai daugintis. Kai taip nutinka, gali išsivystyti navikas (iš esmės nenormalių ląstelių masė).
Navikai skirstomi į dvi kategorijas:yra gerybiniai (ne vėžiniai) ir piktybiniai (vėžiniai) navikai. Taigi koks skirtumas? Atsakymas yra tas, kad gerybinis navikas auga tik tame audinyje, iš kurio jis atsiranda. Gerybiniai navikai kartais gali išaugti gana dideli arba greitai ir sukelti sunkius simptomus, net mirtį, nors dauguma to nedaro. Pavyzdžiui, fibroidinis navikas moters gimdoje yra gerybinio naviko tipas. Jis gali sukelti kraujavimą ar skausmą, tačiau jis niekada neišeis už gimdos ir augs kaip naujas auglys kitur. Miomoms, kaip ir visiems gerybiniams navikams, trūksta gebėjimo išmesti ląsteles į kraują ir limfinę sistemą, todėl jos negali nukeliauti į kitas kūno vietas ir augti. Kita vertus, vėžys gali išmesti ląsteles, kurios gali keliauti per kraują ar limfinę sistemą, nusileisti audiniuose, esančiuose toli nuo pirminio naviko, ir išaugti į naujus navikus šiuose tolimuose audiniuose. Šis plitimo į tolimus audinius procesas, vadinamas metastazėmis, yra būdinga vėžinio ar piktybinio naviko savybė.
Gerybinės naviko ląstelės dažnai atrodo gana normalios, kai tiriamos mikroskopu. Piktybinės arba vėžinės ląstelės paprastai atrodo nenormaliai, kai panašiai žiūrima pro mikroskopą.
Vėžys yra daugiau nei 100 skirtingų ligų grupė, panašiai kaip infekcinės ligos. Vėžys įvardijamas pagal audinius, iš kurių atsiranda pirmasis navikas. Taigi plaučių vėžys, plintantis į kepenis, nėra kepenų vėžys, o apibūdinamas kaip plaučių vėžys, metastazavęs kepenyse, o krūties vėžys, išplitęs į smegenis, apibūdinamas ne kaip smegenų auglys, o kaip krūties vėžys, metastazavęs į kepenis. smegenys. Kiekvienas vėžys yra skirtinga liga su skirtingomis gydymo galimybėmis ir skirtingomis prognozėmis (tikėtini rezultatai arba gyvenimo trukmė). Tiesą sakant, kiekvienas vėžiu sergantis asmuo turi unikalią ligą, o santykinė gydymo sėkmė arba nebuvimas pacientams, kuriems diagnozuota ta pati diagnozė, gali labai skirtis. Todėl svarbu kiekvieną asmenį, kuriam diagnozuotas vėžys, gydyti kaip individą, neatsižvelgiant į vėžio tipą.
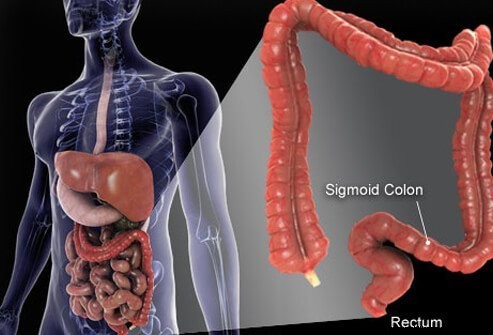
 Storosios žarnos (kolorektalinio) vėžio vaizdas.
Storosios žarnos (kolorektalinio) vėžio vaizdas.
Storoji ir tiesioji žarna yra paskutinės vamzdelio dalys, besitęsiančios nuo burnos iki išangės. Maistas patenka į burną, kur jis kramtomas, o paskui nuryjamas. Tada jis keliauja per stemplę ir patenka į skrandį. Skrandyje maistas sumalamas į smulkesnes daleles, o tada kruopščiai kontroliuojamai patenka į plonąją žarną. Plonojoje žarnoje vyksta galutinis maisto virškinimas ir maiste esančių maistinių medžiagų įsisavinimas. Nesuvirškintas ir neįsisavinamas maistas patenka į storąją žarną (storąją žarną) ir galiausiai į tiesiąją žarną. Storoji žarna pirmiausia veikia kaip atliekų saugykla; tačiau papildomai pašalinamas vanduo, druskos ir kai kurie vitaminai. Be to, dalį nesuvirškinto maisto, pavyzdžiui, skaidulų, virškina storosios žarnos bakterijos, o kai kurie virškinimo produktai pasisavinami iš gaubtinės žarnos ir patenka į organizmą. (Apskaičiuota, kad 10 % su maistu gaunamos energijos gaunama iš šių bakterijų virškinimo produktų storojoje žarnoje.) Likęs nesuvirškintas maistas, mirštančios žarnų gleivinės ląstelės ir daug bakterijų kaupiasi storojoje žarnoje ir tada periodiškai patenka į tiesiąją žarną. Jiems patekus į tiesiąją žarną prasideda tuštinimasis, dėl kurio storosios žarnos turinys iš organizmo pašalinamas kaip išmatos.
Nors storoji žarna yra vamzdis, struktūriškai jis yra sudėtingas vamzdis, labiau panašus į plieninę diržinę radialinę padangą, o ne į sodo žarną. Vamzdis susideda iš keturių sluoksnių. Pirmasis – vidinis ląstelių sluoksnis, išklojęs ertmę, per kurią keliauja nesuvirškintas ir virškinamas maistas, vadinamas gleivine. Gleivinė prisitvirtina prie plono antrojo sluoksnio – submucosa, kuri prisitvirtina prie raumenų sluoksnio – raumens. Visą vamzdelį supa pluoštinis (į randą panašus) audinys, vadinamas seroze. Dažniausias storosios žarnos vėžys (tipas vadinamas adenokarcinoma) atsiranda iš gleivinės, vidinio ląstelių sluoksnio. Šios ląstelės yra veikiamos toksinų iš maisto ir bakterijų, taip pat mechaninio nusidėvėjimo ir santykinai greitai virsta (miršta ir pakeičiamos). Klaidos (dažniausiai daugybė klaidų, susijusių su pakaitinių ląstelių genais) sukelia nenormalias ląsteles ir nekontroliuojamą nenormalių ląstelių, kurios sukelia vėžį, dauginimąsi. Greita kaita leidžia padaryti daugiau klaidų, palyginti su audiniais, kurie ne taip greitai virsta (pavyzdžiui, kepenų audiniu).
Didžioji storosios žarnos dalis yra pilvo ertmėje, vadinamoje pilvaplėvės ertme. Kai kurios storosios žarnos dalys gali laisvai judėti pilvaplėvės ertmėje, kai pro ją patenka nesuvirškintas maistas. Kai gaubtinė žarna nukreipta link tiesiosios žarnos, ji pritvirtinama prie audinių, esančių už pilvaplėvės ertmės, vadinamos retroperitoneumi. Galinė storosios žarnos dalis, dalis, esanti retroperitoneum, yra tiesioji žarna. Skirtingai nuo daugelio likusios storosios žarnos dalies, tiesiąją žarną savo vietoje fiksuoja ją supantys audiniai. Dėl savo vietos tiesiosios žarnos vėžio gydymas dažnai skiriasi nuo likusios gaubtinės žarnos vėžio gydymo.
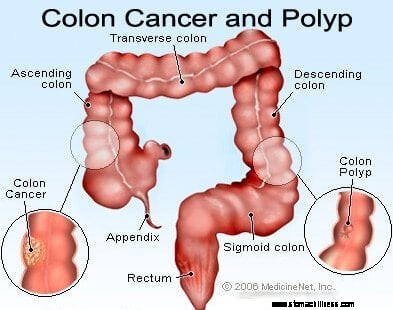
 Storosios žarnos skerspjūvio vaizdas.
Storosios žarnos skerspjūvio vaizdas. 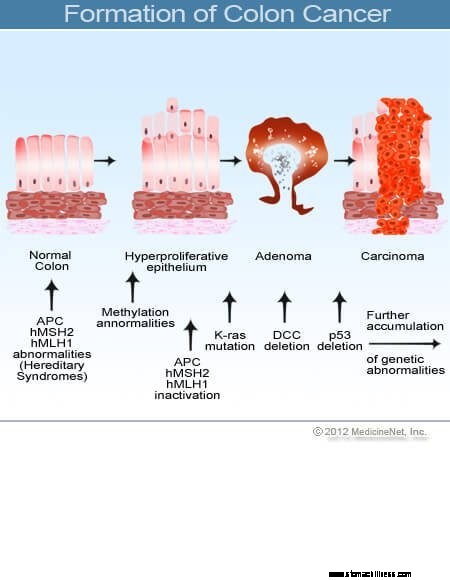 Storosios žarnos vėžio formavimosi nuotrauka.
Storosios žarnos vėžio formavimosi nuotrauka.
Žmogaus storoji žarna (storoji žarna) yra maždaug 6 pėdų ilgio.
Storosios ir tiesiosios žarnos vėžys (kolorektalinis vėžys) prasideda, kai sutrinka normalus gaubtinės žarnos gleivinės ląstelių pakeitimo procesas. Ląstelių dalijimosi klaidų pasitaiko dažnai. Dėl prastai suprantamų priežasčių kartais pasitaiko klaidų, kurios nepastebi mūsų redagavimo sistemų. Kai tai įvyksta, šios ląstelės pradeda dalytis nepriklausomai nuo įprastų patikrinimų ir balansų, kurie kontroliuoja augimą. Kai šios nenormalios ląstelės auga ir dalijasi, jos gali sukelti storosios žarnos augimą, vadinamą polipais. Polipų tipas skiriasi, tačiau daugelis jų yra ikivėžiniai navikai, kurie bėgant metams auga lėtai ir neplinta. Polipams augant, papildomos genetinės mutacijos dar labiau destabilizuoja ląsteles. Kai šie ikivėžiniai navikai pakeičia kryptį (išauga į vamzdelio sienelę, o ne į jo viduryje esančią erdvę) ir įsiveržia į kitus storosios žarnos sluoksnius (pvz., poodinį ar raumenų sluoksnį), ikivėžinis polipas tapo vėžiniu. Daugeliu atvejų šis procesas yra lėtas, užtrunka mažiausiai aštuonerius–10 metų, kad išsivystytų nuo tų ankstyvų nenormalių ląstelių iki atviro vėžio. Kolorektalinis vėžys paprastai yra adenokarcinoma, terminas, reiškiantis vėžį, susiformavusį tam tikro tipo kūno gleivinės audiniuose.
Susiformavęs gaubtinės ir tiesiosios žarnos vėžys pradeda augti dviem būdais. Pirma, vėžys gali augti lokaliai ir plisti per žarnyno sienelę bei įsiskverbti į gretimas struktūras, todėl masė (vadinama pirminiu naviku) tampa didesne problema ir ją sunkiau pašalinti. Vietinis išplėtimas gali sukelti papildomų simptomų, tokių kaip skausmas ar pilnumas, gaubtinės žarnos perforacija arba gaubtinės žarnos ar šalia esančių struktūrų užsikimšimas. Antra, augdamas vėžys pradeda metastazių procesą, per dieną į kraują ir limfinę sistemą išskirdamas tūkstančius ląstelių, dėl kurių vėžys gali susidaryti tolimose vietose. Kolorektalinis vėžys dažniausiai išplinta į vietinius limfmazgius prieš keliaujant į tolimus organus. Kai pažeidžiami vietiniai limfmazgiai, jie plinta į kepenis, pilvo ertmę ir plaučius yra kitos dažniausiai metastazavusios plitimo vietos.
Kolorektalinis vėžys yra trečia dažniausia vėžio priežastis JAV tiek vyrams, tiek moterims. Kasmet ja serga daugiau nei 135 000 žmonių, o tai sudaro 8% visų vėžio atvejų. Maždaug 4,3 % žmonių tam tikru gyvenimo momentu bus diagnozuotas gaubtinės arba tiesiosios žarnos vėžys.
Spustelėdamas „Pateikti“ sutinku su MedicineNet taisyklėmis ir sąlygomis bei privatumo politika. Taip pat sutinku gauti el. laiškus iš MedicineNet ir suprantu, kad galiu bet kada atsisakyti MedicineNet prenumeratos.
Sveikatos priežiūros specialistai įsitikinę, kad gaubtinės ir tiesiosios žarnos vėžys nėra užkrečiamas (žmogus negali užsikrėsti vėžiu sergančiu ligoniu). Kai kurie žmonės labiau linkę susirgti gaubtinės ir tiesiosios žarnos vėžiu nei kiti. Veiksniai, didinantys asmens riziką susirgti gaubtinės ir tiesiosios žarnos vėžiu, yra vyresnis amžius, afroamerikiečių rasė, didelis riebalų suvartojimas, storosios žarnos vėžio ir polipų šeimos istorija, polipų buvimas storojoje žarnoje ir uždegiminės žarnyno ligos, pirmiausia lėtinis opinis kolitas.
Didėjantis amžius yra pagrindinis kolorektalinio vėžio rizikos veiksnys. Maždaug 90 % gaubtinės ir tiesiosios žarnos vėžio atvejų diagnozuojami sulaukus 50 metų.
Afroamerikiečiai kolorektaliniu vėžiu serga dažniau nei kitų rasių žmonės.
Daugybė tyrimų parodė, kad dietos, kuriose yra daug riebalų, skatina žmones susirgti gaubtinės ir tiesiosios žarnos vėžiu. Šalyse, kuriose yra daug storosios žarnos vėžio atvejų, gyventojų riebalų suvartojimas yra daug didesnis nei šalyse, kuriose vėžio atvejų yra mažai. Manoma, kad virškinant riebalus, kurie atsiranda plonojoje žarnoje ir storojoje žarnoje, susidaro vėžį sukeliančios cheminės medžiagos (kancerogenai). Be to, moksliniai tyrimai taip pat atskleidžia, kad dietose, kuriose yra daug daržovių ir daug skaidulų turinčio maisto, pavyzdžiui, pilno grūdo duonos ir grūdų, yra mažiau riebalų, kurie gamina šiuos kancerogenus ir gali kovoti su kancerogenų poveikiu. Abu poveikiai padėtų sumažinti vėžio riziką.
Tyrimai parodė, kad dauguma gaubtinės ir tiesiosios žarnos vėžio formuojasi gaubtinės ir tiesiosios žarnos polipuose. Todėl pašalinus gerybinius (bet ikivėžinius) gaubtinės ir tiesiosios žarnos polipus galima išvengti gaubtinės ir tiesiosios žarnos vėžio. Ikivėžiniai kolorektaliniai polipai dažniausiai vadinami adenomatiniais polipais. Jie išsivysto, kai chromosomų pažeidimas atsiranda gaubtinės žarnos vidinio pamušalo ląstelėse. Pažeidus susidaro nenormalios ląstelės, tačiau ląstelės dar nėra išsiugdusios gebėjimo plisti – tai yra vėžio požymis. Vietoj to, augantis audinys lieka lokalizuotas polipo viduje. Kai chromosomų pažeidimas dar labiau didėja polipo viduje, ląstelių augimas tampa nekontroliuojamas, o ląstelės pradeda plisti, tai yra, tampa vėžiu. Taigi gaubtinės žarnos polipai, kurie iš pradžių buvo gerybiniai, įgyja papildomų chromosomų pažeidimų ir tampa vėžiniais.
Lėtinis opinis kolitas sukelia vidinės gaubtinės žarnos gleivinės uždegimą. Žarnyno vėžys yra pripažinta lėtinio opinio kolito komplikacija. Vėžio rizika pradeda didėti po 8–10 metų sergant kolitu. Paciento, sergančio opiniu kolitu, rizika susirgti storosios žarnos vėžiu taip pat yra susijusi su jo ar jos ligos vieta ir mastu.
Pacientai, kuriems yra didesnė vėžio rizika, yra tie, kurių šeimoje yra buvę gaubtinės žarnos vėžio atvejų, ilgai sergantys opiniu kolitu, plačiai sergantys opiniu kolitu, taip pat tie, kurie serga su opiniu kolitu susijusia kepenų liga, sklerozuojančiu cholangitu.
Kadangi vėžys, susijęs su opiniu kolitu, turi palankesnę baigtį, kai susergama ankstyvoje stadijoje, kasmet rekomenduojama tirti gaubtinę žarną po aštuonerių metų, kai buvo žinoma plačiai liga. Šių tyrimų metu imami audinių mėginiai (biopsijos), ieškant ikivėžinių pakitimų storosios žarnos ląstelėse. Nustačius ikivėžinių pakitimų, norint išvengti gaubtinės žarnos vėžio, gali prireikti pašalinti visą gaubtinę žarną.
Žmogaus genetinis pagrindas yra svarbus storosios žarnos vėžio rizikos veiksnys. Jei pirmos eilės giminaičiai serga gaubtinės ir tiesiosios žarnos vėžiu, ypač jei vėžys buvo diagnozuotas iki 55 metų amžiaus, rizika susirgti šia liga padidėja maždaug dvigubai.
Nors šeimos istorija storosios žarnos vėžiu yra svarbus rizikos veiksnys, dauguma (80%) gaubtinės žarnos vėžio atvejų pasitaiko sporadiškai pacientams, kurių šeimoje nėra gaubtinės žarnos vėžio atvejų. Maždaug 20 % vėžio atvejų yra susiję su storosios žarnos vėžio šeimos istorija.
Chromosomose yra genetinės informacijos, o chromosomų pažeidimai sukelia genetinius defektus, dėl kurių susidaro storosios žarnos polipai, o vėliau – gaubtinės žarnos vėžys. Esant sporadiniams polipams ir vėžiui (polipai ir vėžys, kurie išsivysto nesant šeimos istorijos), chromosomų pažeidimai yra įgyjami (išsivysto ląstelėje suaugusio žmogaus gyvenimo metu). Pažeistas chromosomas galima rasti tik polipuose ir vėžiuose, kurie išsivysto iš tos ląstelės. Tačiau paveldimų gaubtinės žarnos vėžio sindromų atveju chromosomų defektai yra paveldimi gimus ir yra kiekvienoje kūno ląstelėje. Pacientams, paveldėjusiems paveldimo gaubtinės žarnos vėžio sindromo genus, gresia storosios žarnos polipų atsiradimas, dažniausiai jauname amžiuje, ir labai didelė rizika susirgti storosios žarnos vėžiu ankstyvame gyvenime; jiems taip pat gresia kitų organų vėžys.
Šeimos adenomatozinė polipozė (FAP) yra paveldimas gaubtinės ir tiesiosios žarnos vėžio sindromas, kai sergantiesiems šeimos nariams, pradedant paaugliu, išsivystys nesuskaičiuojamas skaičius (šimtai, kartais tūkstančiai) gaubtinės žarnos polipų. Jei būklė nenustatoma ir negydoma anksti (gydymas apima storosios žarnos pašalinimą), asmuo, paveiktas FAP, yra beveik tikras, kad dėl šių polipų išsivystys gaubtinės žarnos vėžys. Vėžys beveik neabejotinai išsivysto žmogui sulaukus 40 metų. Šiems pacientams taip pat gresia kitų vėžio formų, pvz., skydliaukės, skrandžio ir ampulės (tulžies latako dalis, kur jis iš kepenų nuteka į plonąją žarną), vėžys, taip pat gerybiniai navikai, vadinami desmoidiniais navikais. FAP atsiranda dėl specifinio geno, vadinamo APC genu, mutacijos. Konkrečią mutaciją galima nustatyti daugeliui žmonių, atlikus atitinkamus tyrimus, ir tokius tyrimus rekomenduojama atlikti asmenims, kuriems diagnozuotas FAP, ir jų šeimos nariams.
Susilpnėjusi šeiminė adenomatozinė polipozė (AFAP) yra švelnesnė FAP versija. Paveiktiems nariams susidaro mažiau nei 100 gaubtinės žarnos polipų. Nepaisant to, jie vis dar turi labai didelę riziką susirgti storosios žarnos vėžiu jauname amžiuje. Jiems taip pat gresia skrandžio ir dvylikapirštės žarnos polipai.
Paveldimas nepolipozinis gaubtinės žarnos vėžys (taip pat žinomas kaip Lynch sindromas arba HNPCC) yra paveldimas gaubtinės ir tiesiosios žarnos vėžio sindromas, kai paveiktiems šeimos nariams nuo 30 iki 40 metų gali išsivystyti storosios žarnos polipai ir vėžys, dažniausiai dešinėje storojoje žarnoje. Pacientams, sergantiems HNPCC, taip pat kyla rizika susirgti gimdos vėžiu, skrandžio vėžiu, kiaušidžių vėžiu ir šlapimtakių (vamzdelių, jungiančių inkstus su šlapimo pūsle) ir tulžies latakų vėžiu. Ironiška, kad nors storosios žarnos vėžys dažniau pasireiškia pacientams, sergantiems HNPCC, šie vėžys gali būti lengviau išgydomi nei „sporadinis“ gaubtinės žarnos vėžys. Buvo nustatyti specifiniai su HNPCC susiję genetiniai anomalijos, o pacientai ir šeimos nariai gali būti tiriami, siekiant nustatyti, ar yra HNPCC ir ar šeimos nariai turi šią anomaliją ir gali susirgti vėžiu.
MYH polipozės sindromas yra neseniai atrastas paveldimas gaubtinės ir tiesiosios žarnos vėžio sindromas. Sulaukę 40 metų sergantys nariai paprastai išsivysto nuo 10 iki 100 polipų ir jiems kyla didelė rizika susirgti gaubtinės žarnos vėžiu. Čia taip pat buvo nustatyta genetinė anomalija.
Svarbu atsiminti, kad didžioji dauguma gaubtinės ir tiesiosios žarnos vėžio atvejų neturi vieno identifikuojamo chromosomų anomalijos, kurios būtų galima ieškoti pas giminaičius, kad būtų galima nustatyti asmenis, kuriems gresia gaubtinės ir tiesiosios žarnos vėžys.
Su gaubtinės ir tiesiosios žarnos vėžiu susijusių simptomų yra daug ir jie nespecifiniai. Tai yra nuovargis, silpnumas, dusulys, žarnyno įpročių pasikeitimas, susiaurėjusios išmatos, viduriavimas arba vidurių užkietėjimas, raudonas arba tamsus kraujas išmatose, svorio kritimas, pilvo skausmas, mėšlungis ar pilvo pūtimas. Kitos būklės, pvz., dirgliosios žarnos sindromas (spazminis gaubtinės žarnos), opinis kolitas, Krono liga, divertikuliozė ir pepsinė opa, gali turėti žarnyno vėžį imituojančių simptomų.
Kolorektalinis vėžys gali pasireikšti keletą metų, kol pasireiškia simptomai. Simptomai skiriasi priklausomai nuo to, kurioje storosios žarnos vietoje yra navikas. Dešinė dvitaškis yra platesnis ir lankstesnis. Jis netgi gali būti vadinamas gana erdviu, palyginti su likusia dvitaškio dalimi. Dešiniosios gaubtinės žarnos vėžys gali išaugti iki didelių dydžių, kol nesukels jokių pilvo simptomų. Paprastai dešinės pusės vėžys sukelia geležies stokos anemiją dėl lėto kraujo netekimo ilgą laiką. Geležies stokos anemija sukelia nuovargį, silpnumą ir dusulį. Kairioji dvitaškis yra siauresnė nei dešinioji. Todėl kairiosios gaubtinės žarnos vėžys dažniau sukelia dalinį arba visišką žarnyno nepraeinamumą. Vėžys, sukeliantis dalinį žarnyno nepraeinamumą, gali sukelti vidurių užkietėjimo, susiaurėjusių išmatų, viduriavimo, pilvo skausmų, mėšlungio ir pilvo pūtimo simptomus. Ryškiai raudonas kraujas išmatose taip pat gali rodyti augimą netoli kairiosios gaubtinės arba tiesiosios žarnos galo.
Įtarus gaubtinės žarnos vėžį, paprastai atliekama kolonoskopija, siekiant patvirtinti diagnozę ir nustatyti naviko vietą.
Kolonoskopija – tai procedūra, kurios metu sveikatos priežiūros specialistas į tiesiąją žarną įkiša ilgą lankstų stebėjimo vamzdelį, kad apžiūrėtų visos storosios žarnos vidų. Kolonoskopija paprastai laikoma tikslesne nei bario klizmos rentgeno spinduliai, ypač nustatant mažus polipus. Jei randami storosios žarnos polipai, jie paprastai pašalinami per kolonoskopą ir siunčiami patologui. Patologas tiria polipus po mikroskopu, kad patikrintų, ar nėra vėžio. Kolonoskopija yra geriausia procedūra, kurią galima naudoti, kai įtariamas gaubtinės žarnos vėžys. Nors dauguma kolonoskopu pašalintų polipų yra gerybiniai, daugelis jų yra ikivėžiniai. Ikivėžinių polipų pašalinimas apsaugo nuo šių polipų gaubtinės žarnos vėžio išsivystymo ateityje.
Sigmoidoskopija yra procedūra, atliekama naudojant trumpesnę lanksčią sritį, kad būtų galima ištirti tik kairiąją dvitaškį ir tiesiąją žarną. Ji yra lengviau paruošiama ir atliekama nei visa kolonoskopija, tačiau ji turi akivaizdžių apribojimų, nes ji nėra pakankamai ilga, kad būtų galima įvertinti tiek dešinę, tiek skersinę dvitaškį. Naudojant sigmoidoskopą galima atlikti polipų pašalinimą ir vėžio biopsiją.
Jei kolonoskopijos metu randama vėžinių darinių, galima paimti mažus audinių mėginius (biopsijas), kuriuos galima ištirti mikroskopu, siekiant nustatyti, ar polipas yra vėžinis. Jei gaubtinės žarnos vėžys patvirtinamas atlikus biopsiją, atliekami stadijų tyrimai, siekiant nustatyti, ar vėžys jau išplitęs į kitus organus. Kadangi gaubtinės ir tiesiosios žarnos vėžys linkęs plisti į plaučius ir kepenis, sustojimo testai paprastai apima plaučių, kepenų ir pilvo kompiuterinę tomografiją. Pozitronų emisijos tomografijos (PET) skenavimas – naujesnis testas, kuriuo ieškoma padidėjusio metabolinio aktyvumo, būdingo vėžiniams audiniams, taip pat dažnai naudojami siekiant nustatyti gaubtinės žarnos vėžio išplitimą į limfmazgius ar kitus organus.
Kartais sveikatos priežiūros specialistas gali atlikti "naviko žymenų" kraujo tyrimą, vadinamą karcinoembrioniniu antigenu (CEA), jei yra įtarimas dėl vėžio. CEA yra medžiaga, kurią gamina kai kurios gaubtinės ir tiesiosios žarnos vėžio ląstelės, taip pat kai kurios kitos vėžio rūšys. Jis kartais randamas dideliais kiekiais pacientams, sergantiems gaubtinės ir tiesiosios žarnos vėžiu, ypač kai liga išplitusi. Tai gali būti naudingas testas, kurį reikia atlikti, jei nustatoma, kad jis yra padidėjęs prieš pašalinant vėžį. Tačiau ne visiems pacientams, sergantiems gaubtinės ir tiesiosios žarnos vėžiu, CEA bus padidėjęs, net jei vėžys išplito. (Kai kurie gaubtinės ir tiesiosios žarnos vėžys jo nesukelia.) Be to, kai kurie pacientai be vėžiui gali būti padidintas CEA kraujo tyrimas. Pavyzdžiui, apie 15 % rūkančiųjų bus padidėjęs CEA be gaubtinės žarnos vėžio. Taigi CEA naudojamas ne diagnozuoti gaubtinės ir tiesiosios žarnos vėžį, o sekti gaubtinės ir tiesiosios žarnos vėžio gydymo poveikį asmenims, kuriems yra žinoma ligos istorija, nes kai kuriems pacientams vėžinio audinio kiekis koreliuoja su CEA lygiu. /P>
Diagnozavus storosios žarnos vėžį, atliekami papildomi tyrimai ligos mastui nustatyti. Šis procesas vadinamas inscenizacija. Stadija nustato, kaip progresavo gaubtinės ir tiesiosios žarnos vėžys. Kolorektalinio vėžio stadija svyruoja nuo I stadijos, mažiausiai pažengusio vėžio, iki IV stadijos, labiausiai pažengusio vėžio.
Su kiekviena sekančia gaubtinės žarnos vėžio stadija didėja vėžio pasikartojimo ir mirties dėl vėžio plitimo (metastazių) rizika. Kaip minėta, ankstesni vėžio atvejai turi mažesnę pasikartojimo ir mirties riziką. Tuo metu, kai asmuo serga IV stadijos gaubtinės ir tiesiosios žarnos vėžiu, prognozė yra prasta. Tačiau net ir sergant IV stadijos gaubtinės ir tiesiosios žarnos vėžiu (atsižvelgiant į tai, kur vėžys išplito) yra galimybė jį išgydyti.
Chirurgija yra labiausiai paplitęs pradinis kolorektalinio vėžio gydymas. Operacijos metu pašalinamas auglys, nedidelis aplinkinio sveikojo žarnyno kraštas ir šalia esantys limfmazgiai. Tada chirurgas vėl sujungia sveikas žarnyno dalis. Pacientams, sergantiems tiesiosios žarnos vėžiu, tiesioji žarna kartais pašalinama visam laikui, jei vėžys atsiranda per žemai tiesiojoje žarnoje. Tada chirurgas sukuria angą (kolostomiją) ant pilvo sienelės, per kurią pašalinamos kietosios gaubtinės žarnos atliekos. Specialiai apmokytos slaugytojai (enterostominiai terapeutai) gali padėti pacientams prisitaikyti prie kolostomijų, o dauguma pacientų, kuriems atlikta kolostomija, grįžta prie įprasto gyvenimo būdo.
Ankstyvojo žarnyno vėžio atveju rekomenduojamas gydymas yra chirurginis pašalinimas. Daugumai žmonių, sergančių ankstyvos stadijos gaubtinės žarnos vėžiu (I stadija ir dauguma II stadijos), vienintelis reikalingas gydymas yra operacija. Chemoterapija gali būti pasiūlyta kai kuriems II stadijos vėžiu sergantiems žmonėms, kurie turi veiksnių, leidžiančių manyti, kad jų augliui gali būti didesnė pasikartojimo rizika. Tačiau storosios žarnos vėžiui išplitus į vietinius limfmazgius (III stadija), vėžio pasikartojimo rizika išlieka didelė, net jei chirurgas pašalino visus matomus vėžio požymius. Taip yra dėl padidėjusios tikimybės, kad mažytės vėžio ląstelės galėjo pabėgti prieš operaciją ir yra per mažos, kad būtų galima tuo metu aptikti kraujo tyrimais, skenavimu ar net tiesioginiu tyrimu. Jų buvimas išplaukia iš didesnės gaubtinės žarnos vėžio pasikartojimo rizikos vėliau (atkryčio). Vėžio gydytojai (medicinos onkologai) rekomenduoja papildomai gydyti gaubtinės žarnos vėžį chemoterapija, kad sumažintų vėžio pasikartojimo riziką. Chemoterapijai naudojami vaistai patenka į kraują ir atakuoja visas gaubtinės žarnos vėžio ląsteles, kurios prieš operaciją buvo pasklidusios į kraują ar limfinę sistemą, bandydami jas nužudyti, kol jos neatsinaujina kituose organuose. Įrodyta, kad ši strategija, vadinama adjuvantine chemoterapija, sumažina vėžio pasikartojimo riziką ir rekomenduojama visiems III stadijos gaubtinės žarnos vėžiu sergantiems pacientams, kurie yra pakankamai sveiki, kad galėtų jį atlikti, taip pat kai kuriems didesnės rizikos II stadijos pacientams, kurių navikas gali turėti. buvo nustatyta, kad prieš operaciją buvo užkimšta arba perforuota žarnyno sienelė.
Yra keletas skirtingų adjuvantinės chemoterapijos variantų gaubtinės žarnos vėžiui gydyti. Gydymas apima chemoterapinių vaistų derinį, vartojamą per burną arba į veną. Gydymas paprastai skiriamas iš viso šešis mėnesius. Svarbu susitikti su onkologu, kuris galėtų paaiškinti adjuvantinės chemoterapijos galimybes ir šalutinį poveikį, į kurį reikia atkreipti dėmesį, kad būtų galima tinkamai pasirinkti pacientui kaip asmenybei.
Chemoterapija paprastai atliekama sveikatos priežiūros specialisto klinikoje, ligoninėje ambulatoriškai arba namuose. Chemoterapija paprastai skiriama gydymo ciklais, po kurių seka atsigavimo periodai be gydymo. Šalutinis chemoterapijos poveikis kiekvienam žmogui skiriasi ir taip pat priklauso nuo vartojamų medžiagų. Šiuolaikiniai chemoterapiniai vaistai paprastai yra gerai toleruojami, o šalutinis poveikis daugeliui žmonių yra valdomas. Apskritai vaistai nuo vėžio sunaikina ląsteles, kurios greitai auga ir dalijasi. Todėl chemoterapija gali paveikti normalius raudonuosius kraujo kūnelius, trombocitus ir baltuosius kraujo kūnelius, kurie taip pat greitai auga. Dėl to dažnas šalutinis poveikis yra anemija, energijos praradimas ir mažas atsparumas infekcijoms. Plaukų šaknyse ir žarnyne esančios ląstelės taip pat greitai dalijasi. Todėl chemoterapija gali sukelti plaukų slinkimą, burnos opų, pykinimą, vėmimą ir viduriavimą, tačiau šis poveikis yra laikinas.
Kai gaubtinės ir tiesiosios žarnos vėžys išplito toli nuo pirminio naviko vietos, jis apibūdinamas kaip IV stadijos liga. Šios tolimos naviko sankaupos, išsiskirtos iš pirminio naviko, nukeliavo per kraują arba limfinę sistemą, sudarant naujus navikus kituose organuose. Tuo metu gaubtinės ir tiesiosios žarnos vėžys nebėra vietinė problema, o sisteminė vėžio ląstelių problema, kuri yra matoma nuskaitymo metu ir neaptinkama, bet greičiausiai yra kitur visame kūne. Dėl to daugeliu atvejų geriausias gydymas yra chemoterapija, kuri yra sisteminė terapija. Įrodyta, kad metastazavusio gaubtinės ir tiesiosios žarnos vėžio chemoterapija prailgina gyvenimą ir pagerina gyvenimo kokybę. Jei gerai valdoma, chemoterapijos šalutinis poveikis paprastai yra daug mažesnis nei nekontroliuojamo vėžio šalutinis poveikis. Vien chemoterapija negali išgydyti metastazavusio gaubtinės žarnos vėžio, tačiau ji gali padvigubinti gyvenimo trukmę ir užtikrinti gerą gyvenimo kokybę gydymo metu.
Kolorektalinio vėžio gydymo chemoterapijos galimybės skiriasi priklausomai nuo kitų sveikatos problemų, su kuriomis susiduria asmuo. Sergantiems žmonėms dažniausiai rekomenduojami kelių chemoterapinių vaistų deriniai, o sergantiesiems geriausiai tiktų paprastesnis gydymas. Įvairios kelių vaistų schemos derina agentus, kurių poveikis gaubtinės ir tiesiosios žarnos vėžiui įrodytas, pvz., 5-fluorouracilą (5-FU), kuris dažnai skiriamas kartu su vaistu leukovorinu (taip pat vadinamu folino rūgštimi) arba panašiu vaistu, vadinamu levoleukovorinu, kuris padeda geriau veikti.
Kapecitabinas (Xeloda) yra chemoterapinis vaistas, vartojamas tablečių pavidalu. Patekęs į organizmą, jis pakeičiamas į 5-FU, kai patenka į naviko vietą. Kiti chemoterapiniai vaistai nuo gaubtinės ir tiesiosios žarnos vėžio yra irinotekanas (Camptosar), oksaliplatina (eloksatinas) ir trifluridinas bei tipiracilas (Lonsurf), kombinuotas vaistas tablečių pavidalu. Chemoterapijos režimai dažnai turi akronimus, kad supaprastintų jų nomenklatūrą (pvz., FOLFOX, FOLFIRI ir FLOX).
Targeted therapies are newer treatments that target specific aspects of the cancer cell, which may be more important to the tumor than the surrounding tissues, offering potentially effective treatments with fewer side effects than traditional chemotherapy. Bevacizumab (Avastin), cetuximab (Erbitux), panitumumab (Vectibix), ramucirumab (Cyramza), regorafenib (Stivarga), and ziv-aflibercept (Zaltrap) are targeted therapies that have been used in the management of advanced colorectal cancer. These newer chemotherapeutic agents most often are combined with standard chemotherapy to enhance their effectiveness.
If the first treatment is not effective, second- and third-line options are available that can confer a benefit to people living with colorectal cancer.
Radiation therapy is the primary treatment of colorectal cancer has been limited to treating cancer of the rectum. As noted earlier, whereas parts of the colon move freely within the abdominal cavity, the rectum is fixed in place within the pelvis. It is in an intimate relationship with many other structures and the pelvis is a more confined space. For these reasons, a tumor in the rectum often is harder to remove surgically because space is smaller and other structures can be involved with cancer. As a result, for all but the earliest rectal cancers, initial chemotherapy and radiation treatments (a local treatment to a defined area) are recommended to try and shrink cancer, allowing for easier removal and lowering the risk of cancer returning locally. Radiation therapy is typically given under the guidance of a radiation specialist called a radiation oncologist. Initially, individuals undergo a planning session, a complicated visit as the doctors and technicians determine exactly where to give the radiation and which structures to avoid. Chemotherapy usually is administered daily while the radiation is delivered. Side effects of radiation treatment include fatigue, temporary or permanent pelvic hair loss, and skin irritation in the treated areas.
Radiation therapy will occasionally be used as a palliative treatment to reduce pain from the recurrent or metastatic colon or rectal cancer.
Follow-up exams are important for people with colorectal cancer. The cancer can come back near the original site, although this is unusual. If the cancer returns, it typically does so in a distant location such as the lymph nodes, liver, or lungs. Individuals diagnosed with colorectal cancer remain at risk of their cancer returning for up to 10 years after their original diagnosis and treatment, although the risk of recurrence is much higher in the first few years. Medical providers in the United States follow patients with physical examinations and blood tests including the CEA (if it was elevated before surgery) tumor marker every three months for the first two years and then with decreasing frequency thereafter. Patients are also followed with colonoscopies (starting one year after their diagnosis) and with CT scans (typically performed at least once yearly for the first two to five years).
If a recurrence is noted either locally or with metastatic spread, individuals may still be treated with the intention of cure. For example, if a new tumor were to recur in the liver, individuals can be treated with a combination of chemotherapy and surgery (or sophisticated radiation techniques) in hopes of eradicating the cancer completely. Evaluation in hospitals of excellence that specialize in liver surgery can help guide these complicated treatment decisions and increase the chances of cure even in the setting of metastatic disease.
In addition to checking for cancer recurrence, patients who have had bowel cancer may have an increased risk of cancer of the prostate, breast, and ovary. Therefore, follow-up examinations in the clinic should include cancer screening for these diseases, as well.
Colorectal cancers are typically slow-growing cancers that take years to develop. Because they grow most often in a step-wise manner, screening can greatly reduce the likelihood of death associated with the disease. Whether with virtual colonoscopy or newer screening techniques, the future must focus first and foremost on better, more comprehensive screening programs that find polyps and early cancers before they become life-threatening. The public also must be educated on the value of screening programs.
For those living with cancer, intensive research is ongoing to better understand cancer biology and genetics so that specific approaches can be developed to attack specific types of cancers and, more importantly, specific individuals' cancers. Each person living with cancer has a disease with a unique biology and genetic code and the secret to better treatments involves unlocking that code. Cancer is very complex and scientists are just beginning to unravel its secrets. Progress is frustratingly slow for those battling the disease. With each passing year, however, our understanding increases and treatments become more refined. If you or your family member is living with colorectal cancer, speak with your doctor about ways you can participate in research through clinical trials to help increase our knowledge and improve our therapies for this difficult disease.
Survival rates for any cancer are often reported by stage, the extent of spread when the cancer is identified. For colon and rectum cancer, around 39% are diagnosed at the local stage, before the cancer has spread outside the local area. The five-year survival for these patients with localized colon and rectum cancer is around 90%.
When the cancer has spread to the regional lymph nodes near the site of origin, the five-year survival rate is about 71%. When the cancer has metastasized to distant sites in the body (stage IV cancer), the five-year survival rate lowers to about 14%.
The most effective prevention for colorectal cancer is early detection and removal of precancerous colorectal polyps before they turn cancerous. Even in cases where cancer has already developed, early detection still significantly improves the chances of a cure by surgically removing the cancer before the disease spreads to other organs.
Regular physical activity is associated with lower risk of colon cancer. Aspirin use also appears to lower the risk of bowel cancer. The use of combined estrogen and progestin in hormone replacement therapy lowers the risk of colon cancer in postmenopausal women. Hormone replacement therapy has risks which must be weighed against this effect, and should be discussed with a doctor.
Blood tests are now available to test for hereditary colon cancer syndromes. Families with multiple members having colon cancers, multiple colon polyps, cancers at young ages, and other cancers such as cancers of the ureters, uterus, duodenum, and more, may take advantage of resources such as genetic counseling, followed possibly by genetic testing. Genetic testing without prior counseling is discouraged because of the extensive family education that is involved and the complicated nature of interpreting the test results.
The advantages of genetic counseling followed by genetic testing include:(1) identifying family members at high risk of developing colon cancer to begin colonoscopies early; (2) identifying high-risk members so that screening may begin to prevent other cancers such as ultrasound tests for uterine cancer, urine examinations for ureter cancer, and upper endoscopies for stomach and duodenal cancers; and (3) alleviating concern for members who test negative for the hereditary genetic defects.
People can change their eating habits by reducing fat intake and increasing fiber (roughage) in their diet. Major sources of fat are meat, eggs, dairy products, salad dressings, and oils used in cooking. Fiber is the insoluble, nondigestible part of plant material present in fruits, vegetables, and whole-grain breads and cereals. It is postulated that high fiber in the diet leads to the creation of bulky stools which can rid the intestines of potential carcinogens. In addition, fiber leads to the more rapid transit of fecal material through the intestine, thus allowing less time for a potential carcinogen to react with the intestinal lining.
The term "screening" is properly applied only to the use of testing to look for evidence of cancer or pre-cancerous polyps in individuals who are asymptomatic and at only average risk for a type of cancer. Those patients who, for example, have a positive family history of colon cancer, or are symptomatic for a colon abnormality, undergo diagnostic testing rather than screening tests.
There are different types of screening tests for colorectal cancer:fecal (stool) occult blood testing, sigmoidoscopy, colonoscopy, digital colonoscopy, and DNA testing of the stool. The US Preventive Services Task Force (USPSTF) recommends strongly that screening begin at age 50 years for average-risk adults, but there is no specific recommendation for one screening test or strategy over another. The USPSTF advises that patients be offered a choice of screening options, using shared decision-making with the patient and physician to arrive at the best choice of screening programs for each individual.
Tumors of the colon and rectum tend to bleed slowly into the stool. The small amount of blood mixed into the stool usually is not visible to the naked eye. The commonly used stool occult blood tests rely on chemical color conversions to detect microscopic amounts of blood. These tests are both convenient and inexpensive. There are two kinds of fecal occult blood tests. The first is known as a guaiac FOBT. In this test, a small amount of stool is smeared on a special card for occult blood testing when a chemical is added to the card. Usually, three consecutive stool cards are collected. The other type of FOBT is an immunochemical test in which a special solution is added to the stool sample and analyzed in the laboratory using antibodies that can detect blood in a stool sample. The immunochemical test is a quantitative test that is more sensitive and specific for the diagnosis of polyps and cancer. It is preferred over the guaiac test.
A person who tests positive for stool occult blood has a 30%-45% chance of having a colon polyp and a 3%-5% chance of having a colon cancer. Colon cancers found under these circumstances tend to be small and not to have spread and have a better long-term prognosis.
It is important to remember that having stool tested positive for occult blood does not necessarily mean a person has colon cancer. Many other conditions can cause occult blood in the stool. However, patients with a positive stool occult blood test should undergo further evaluations to exclude colon cancer and to explain the source of the bleeding. It is also important to realize that stool that has tested negative for occult blood does not mean that colorectal cancer or polyps do not exist. Even under ideal testing conditions, a significant percentage of colon cancers can be missed by stool occult blood screening. Many patients with colon polyps do not have positive stool occult blood. In patients suspected of having colorectal polyps and in those at higher risk for developing colorectal polyps and cancer, screening flexible sigmoidoscopies or colonoscopies are performed even if the FOBT is negative.
Flexible sigmoidoscopy is an exam of the rectum and the lower colon (60 cm or about 2 feet in from the outside) using a viewing tube (a short version of colonoscopy). Research studies have shown that the use of screening flexible sigmoidoscopy can reduce mortality from colon cancer. This is a result of the detection of polyps or early cancers in people with no symptoms. If a polyp or cancer is found, a complete colonoscopy is recommended. The majority of colon polyps can be completely removed at the time of colonoscopy without surgery; however, polyps in the proximal colon that cannot be reached by the sigmoidoscope will be missed. Flexible sigmoidoscopy is often combined with fecal occult blood testing for colorectal cancer screening.
Colonoscopy uses a long (120 cm-150 cm) flexible tube, which can examine the entire length of the colon. Through this tube, the doctor (typically a gastroenterologist) can both view and take pictures of the entire colon and also can take biopsies of colon masses and remove polyps.
Patients with a high risk of developing colorectal cancer may undergo screening colonoscopies starting at earlier ages than 50. For example, patients with a family history of colon cancer are recommended to start screening colonoscopies at an age 10 years before the earliest colon cancer diagnosed in a first-degree relative or five years earlier than the earliest precancerous colon polyp discovered in a first-degree relative. Patients with hereditary colon cancer syndromes such as FAP, AFAP, HNPCC, and MYH are recommended to begin colonoscopies early. The recommendations differ depending on the genetic defect. For example, in people with FAP, colonoscopies may begin during teenage years to look for the development of colon polyps. Patients with a prior history of polyps or colon cancer may also undergo colonoscopies to exclude recurrence. Patients with a long history (greater than 10 years) of chronic ulcerative colitis have an increased risk of colon cancer and should have regular colonoscopies to look for precancerous changes in the colon lining.
Virtual colonoscopy (computerized tomographic or CT colonography) has been utilized in the clinic as a screening technique for colorectal cancer. Virtual colonoscopy employs a CT scan using low doses of radiation with special software to visualize the inside of the colon and look for polyps or masses. The procedure typically involves a bowel preparation with laxatives and/or enemas (although not always) followed by a CT scan after air is introduced into the colon. Because no sedation is necessary, individuals can return to work or other activities upon completion of the test. Virtual colonoscopies appear to be equally able to detect larger polyps (over 1 centimeter in size) as regular colonoscopies. The virtual colonoscopy cannot be used to biopsy or remove tissue from the colon. A follow-up sigmoidoscopy or colonoscopy must be done to accomplish that.
The Cologuard test is available in the U.S. for in-home sample collection for adults over 50 at average risk for colon cancer. The sample is sent to a laboratory for analysis of DNA changes in DNA from cells shed by the intestinal lining into the stool or hemoglobin in the sample. In a research study, the test was able to find 92% of colon cancers and 69% of precancers of the colon. False-negative and false-positive results are also possible.
 Kas sukelia ankilozuojantį spondilitą (ir kaip jį sustabdyti natūraliai)
Tiems, kuriems diagnozuota autoimuninė liga, tokia kaip ankilozuojantis spondilitas, piešiamas paveikslas dažnai būna niūrus. Sustingęs stuburas, ribotas mobilumas ir varginantis skausmas – tai tik k
Kas sukelia ankilozuojantį spondilitą (ir kaip jį sustabdyti natūraliai)
Tiems, kuriems diagnozuota autoimuninė liga, tokia kaip ankilozuojantis spondilitas, piešiamas paveikslas dažnai būna niūrus. Sustingęs stuburas, ribotas mobilumas ir varginantis skausmas – tai tik k
 3 neįvertintos mitybos plano priežastys (ir kodėl aš to vengiu)
„Tas, kuris nesugeba planuoti, planuoja žlugti“. ~ Vinstonas Čerčilis Ahhh... ta akimirka, kai stovi virtuvėje ir tuščiu žvilgsniu žiūri į šaldytuvą. Dažnai galvoju, kas nutiktų, jei staiga iš vidau
3 neįvertintos mitybos plano priežastys (ir kodėl aš to vengiu)
„Tas, kuris nesugeba planuoti, planuoja žlugti“. ~ Vinstonas Čerčilis Ahhh... ta akimirka, kai stovi virtuvėje ir tuščiu žvilgsniu žiūri į šaldytuvą. Dažnai galvoju, kas nutiktų, jei staiga iš vidau
 Kas yra protonų pluošto terapija sergant vėžiu?
Vėžio gydymas protonų pluoštu yra panašus į spindulinę terapiją, tačiau navikams pažeisti vietoj fotonų ar rentgeno spindulių naudojami didelės energijos protonai. Paprastai jis naudojamas ankstyvos s
Kas yra protonų pluošto terapija sergant vėžiu?
Vėžio gydymas protonų pluoštu yra panašus į spindulinę terapiją, tačiau navikams pažeisti vietoj fotonų ar rentgeno spindulių naudojami didelės energijos protonai. Paprastai jis naudojamas ankstyvos s