Sans thérapeutique efficace, les cliniciens ont étendu leurs recherches aux domaines des composés d'origine végétale. Médecine traditionnelle chinoise (MTC), par exemple, a produit plusieurs composés efficaces contre le SRAS-CoV antérieur et fait actuellement partie de l'approche thérapeutique de la maladie à coronavirus 20198 (COVID-19) en Chine.
 Étude :Acide glycyrrhizique :un ingrédient végétal naturel en tant que médicament candidat pour traiter le COVID-19. Crédit d'image :mirzamlk/Shutterstock.com
Étude :Acide glycyrrhizique :un ingrédient végétal naturel en tant que médicament candidat pour traiter le COVID-19. Crédit d'image :mirzamlk/Shutterstock.com
Le développement rapide des vaccins COVID-19 et leur déploiement ultérieur dans de nombreuses régions du monde ont fait des progrès considérables dans la réduction du nombre et de la gravité des cas de COVID-19. Malgré leur utilité, l'émergence de nouvelles variantes du SRAS-CoV-2 qui sont moins sensibles aux anticorps neutralisants (nAb) induits par la souche parentale Wuhan a remis en cause le succès de ces vaccins.
En plus de remettre en cause l'efficacité des vaccins actuels, bon nombre de ces nouvelles souches de SARS-CoV-2 sont également plus transmissibles que la souche de SARS-CoV-2 de type sauvage. Par conséquent, il y a eu une augmentation significative des infections au COVID-19 dans de nombreuses régions du monde, en particulier ceux qui n'ont pas encore vacciné la majorité de leur population.
Dans l'étude actuelle, qui a été publié dans Frontières en pharmacologie , les chercheurs se sont concentrés sur la réglisse, qui a le composé actif acide glycyrrhizique (GA). GA s'est avéré avoir une activité antivirale, notamment contre le SARS-CoV-2.
Dans l'étude actuelle, GA s'est avéré avoir à la fois des propriétés de ciblage des protéines et des propriétés immunomodulatrices. Il a également une activité synergique avec de nombreux médicaments qui ont amélioré son potentiel antiviral contre le SRAS-CoV-2. Cela indique le rôle potentiel de l'AG en tant que thérapie COVID-19.
En cas de COVID-19 sévère et critique, la tempête de cytokines a été bien documentée et est associée à un risque accru de dysfonctionnement ou de défaillance multiviscérale, associée à un syndrome de détresse respiratoire aiguë, et la mort. En milieu clinique, le puissant anti-inflammatoire dexaméthasone, qui est un corticostéroïde, a été trouvé pour améliorer les résultats de survie dans ce groupe de patients COVID-19.
La MTC a été largement utilisée lors de l'épidémie de SRAS de 2002, avec des allégations selon lesquelles il a réduit le taux de mortalité lorsqu'il est utilisé avec la médecine occidentale. Parmi les médicaments à base de plantes les plus couramment utilisés en MTC est la réglisse, qui est connu pour avoir des propriétés antivirales et antibactériennes.
GA a été montré in silico se lier à de nombreuses protéines clés du SRAS-CoV-2, y compris la pointe, domaine de liaison au récepteur, l'acide ribonucléique (ARN) polymérase, ainsi qu'au récepteur de l'enzyme de conversion de l'angiotensine 2 (ACE2), qui est le récepteur de la cellule hôte auquel le SARS-CoV-2 se lie lorsqu'il pénètre dans les cellules.
La présente étude montre que l'AG est un adjuvant à l'activation immunitaire, et améliore ainsi la réponse immunitaire antivirale pendant que le virus est en période d'incubation. GA coupe également la tempête de cytokines causée par le SRAS-CoV-2, tout en modulant l'invasion virale via son effet sur le métabolisme des stéroïdes.
Compte tenu de son effet synergique sur le SARS-CoV-2, L'AG pourrait réduire le taux de mortalité du COVID-19. Cependant, d'autres études sont nécessaires pour explorer son utilité comme adjuvant dans le traitement de cette condition.
Le SRAS-CoV-2 active les lymphocytes T CD4+ après avoir pénétré dans la cellule hôte; cependant, il déclenche également plusieurs mécanismes d'échappement immunitaire. Cette, couplée à la réponse immunitaire adaptative retardée et à la longue période nécessaire pour éliminer le virus, provoque une lymphopénie. En favorisant la prolifération des lymphocytes T et grâce à son activité adjuvante sur les lymphocytes T helper de type 1 (Th1), L'AG augmente la réponse immunitaire au SRAS-CoV-2.
Deuxièmement, GA provoque l'apoptose des cellules hôtes infectées qui contiennent le virus latent, ce qui pourrait aider à empêcher la propagation du virus.
La cytokine sécrétée par Th1 appelée facteur de stimulation des colonies de granulocytes et de macrophages (GM-CSF) est impliquée dans la libération de facteurs inflammatoires et l'apparition rapide de la pneumonie. Cela implique l'expression de l'interleukine 6 (IL-6), peut-être par l'hyperactivation du facteur nucléaire-κB (NF-κB), qui induit une cascade vicieuse de libération de médiateurs inflammatoires.
Le SRAS-CoV-2 peut se lier aux antigènes lipopolysaccharidiques (LPS), intensifiant encore cette réponse NF-κB, et conduisant ainsi à la tempête de cytokines et au SDRA. En inhibant l'expression de NF-κB, L'AG pourrait prévenir les phénomènes hyper-inflammatoires dans le COVID-19.
GA peut également se lier au groupe haute mobilité box-1 (HMGB1), qui est un biomarqueur associé aux lésions pulmonaires aiguës (ALI) observées de manière caractéristique dans les cas graves de COVID-19, ainsi que d'inflammation systémique sévère. HMGB1 réduit la réponse antimicrobienne du corps et augmente ainsi le risque de décès, ainsi que favorise l'invasion et la réplication du SRAS-CoV-2. Ainsi, L'AG peut également perturber ces voies dommageables, empêchant ainsi l'inflammation et le SDRA.
Le diabète est un facteur de risque de COVID-19 sévère, car il favorise l'absorption du cholestérol dans les radeaux lipidiques, ou des microdomaines membranaires cellulaires riches en lipides. Ces radeaux sont des points d'attache pour le virus, favorisant ainsi l'entrée virale dans les cellules hôtes. GA semble réduire l'invasion du SRAS-CoV-2 en réduisant la taille du radeau lipidique.
Le cholestérol s'accumule dans l'endothélium dans l'hypertension et l'hypercholestérolémie, ce qui peut favoriser la formation de caillots sanguins. Le cholestérol entraîne également l'agrégation plaquettaire et la formation de caillots.
GA peut réduire la taille du domaine du cholestérol sur la membrane des cellules endothéliales, inhibant ainsi ces effets. Étant donné que l'AG peut provoquer un pseudoaldostéronisme et une hypertension après son utilisation à long terme, la spironolactone peut être nécessaire chez ces patients.
Dans le syndrome métabolique, une constellation clinique comprenant l'obésité, hyperglycémie, hypertension, et dyslipidémie, le risque de COVID-19 sévère et de SDRA est élevé, tandis que les niveaux de LPS dans le sang sont augmentés. Ainsi, L'AG peut jouer un rôle majeur dans la prévention de cette détérioration.
GA inhibe également le facteur de nécrose tumorale (TNF)-α, qui peut prévenir une inflammation intestinale sévère chez les patients atteints de COVID-19 et du syndrome du côlon irritable. Plus loin, GA peut protéger le système nerveux grâce à sa capacité à inhiber l'apoptose et l'activité HMGB1, ce qui peut prévenir l'inflammation et les lésions ischémiques du cerveau.
Facteur de transcription activant 2 (ATF2), qui est un médiateur inflammatoire, médie la douleur associée à l'inflammation. GA semble inhiber l'ATF2 en aval de son activité sur P38, modulant ainsi la douleur associée au COVID-19.
L'AG peut réduire le métabolisme des stéroïdes, ce qui peut augmenter le taux plasmatique de stéroïdes, évitant ainsi les chocs, comme démontré dans des modèles animaux. Ainsi, les corticostéroïdes et l'AG pourraient être une approche thérapeutique synergique pour COVID-19.
Les diabétiques sont plus à risque de COVID-19; cependant, Le diabète d'apparition récente survient chez environ un patient COVID-19 sur sept. Peut-être que le SRAS-CoV-2 cause des dommages aux îlots pancréatiques, avec échec résultant de la sécrétion d'insuline et du diabète. Certains des médicaments utilisés pour traiter cette infection peuvent également contribuer ou provoquer le diabète en raison de leur propension à provoquer une maladie auto-immune des îlots pancréatiques.
GA a une activité antidiabétique, ce qui renforce son attractivité dans cet état. De plus, ce composé peut réguler positivement la production de l'enzyme oxyde nitrique synthase inductible (iNOS), favorisant ainsi la production de NO. C'est important, car le NO réduit la réplication virale et l'ALI en raison de l'inflammation, ainsi que détend les vaisseaux sanguins pulmonaires.
Cette activité par GA peut conduire à l'élimination du liquide extracellulaire du lit pulmonaire, réduire la résistance dans le lit vasculaire pulmonaire, et finalement atténuer le SDRA.
L'AG protège également le foie, et peut ainsi prévenir les lésions hépatiques des différents médicaments utilisés actuellement pour traiter le COVID-19, ce qui en fait un ajout précieux à de tels protocoles.
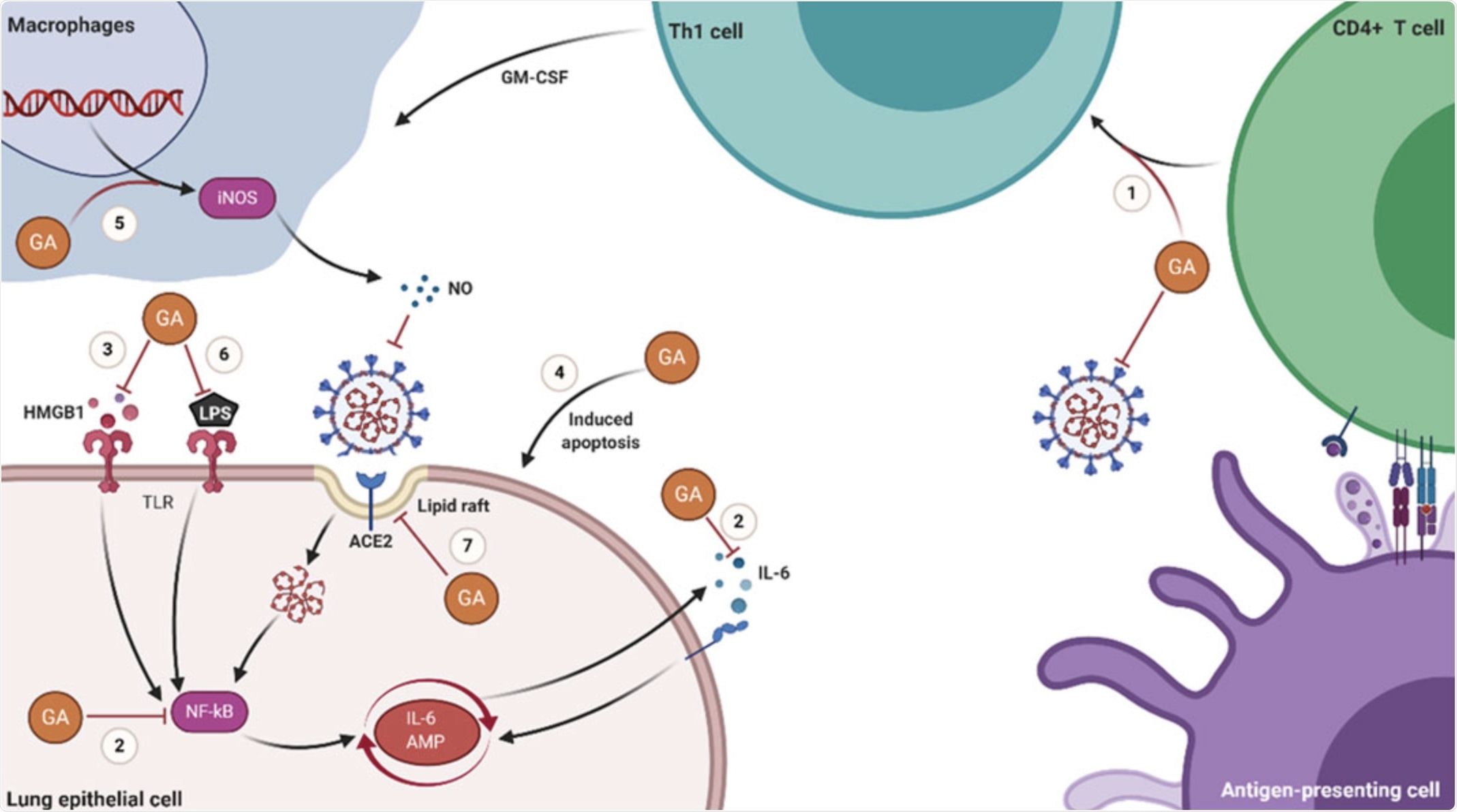 Diagramme schématique des mécanismes moléculaires de l'AG dans le traitement du COVID-19. (1) GA favorise la prolifération des cellules T et a une activité d'adjuvant immunitaire des cellules Th1. (2) GA inhibe la production d'IL-6 et l'activation de NF-kB. (3) GA inhibe l'activité du HMGB1 et la transduction du signal du HMGB1-TLR
Diagramme schématique des mécanismes moléculaires de l'AG dans le traitement du COVID-19. (1) GA favorise la prolifération des cellules T et a une activité d'adjuvant immunitaire des cellules Th1. (2) GA inhibe la production d'IL-6 et l'activation de NF-kB. (3) GA inhibe l'activité du HMGB1 et la transduction du signal du HMGB1-TLR
L'AG est utilisée depuis longtemps en MTC comme composé antiviral et anti-inflammatoire. Des recherches récentes montrent sa capacité à supprimer l'invasion et la réplication du SRAS-CoV-2.
GA semble se lier à de nombreuses protéines du SRAS-CoV-2 tout en ayant également la capacité de supprimer la réplication virale. Sa capacité à aider à la réponse immunitaire aux virus pendant la période d'incubation, amortir la libération excessive de cytokines, et moduler le métabolisme des stéroïdes rendent ce médicament digne d'être étudié dans les tentatives actuelles de traiter plus efficacement le COVID-19.
 Les étiquettes des produits commerciaux à base de kéfir indiquent-elles correctement les niveaux microbiens ?
Les étiquettes des produits commerciaux à base de kéfir indiquent-elles correctement les niveaux microbiens ?
 La composition et la structure du microbiome nasopharyngé sont liées à la gravité de la maladie COVID-19
La composition et la structure du microbiome nasopharyngé sont liées à la gravité de la maladie COVID-19
 Pourquoi ai-je besoin d'une coloscopie?
Pourquoi ai-je besoin d'une coloscopie?
 Les femmes sont-elles plus susceptibles de développer un COVID long ?
Les femmes sont-elles plus susceptibles de développer un COVID long ?
 Un régime à base de plantes pourrait guérir votre polyarthrite rhumatoïde
Un régime à base de plantes pourrait guérir votre polyarthrite rhumatoïde
 E. coli superbactérie se propageant par une mauvaise hygiène des toilettes,
E. coli superbactérie se propageant par une mauvaise hygiène des toilettes,
 Une variante génétique commune explique pourquoi l'immunothérapie échoue souvent dans la maladie de Crohn
La raison pour laquelle une gamme de médicaments couramment utilisés nest pas efficace chez certains patients vivant avec la maladie de Crohn na pas encore été identifiée. Cependant, une collaboration
Une variante génétique commune explique pourquoi l'immunothérapie échoue souvent dans la maladie de Crohn
La raison pour laquelle une gamme de médicaments couramment utilisés nest pas efficace chez certains patients vivant avec la maladie de Crohn na pas encore été identifiée. Cependant, une collaboration
 Les composés antiviraux dérivés des microalgues pourraient-ils combattre le SRAS-CoV-2 et d'autres virus ?
Avec lémergence de la pandémie actuelle de la maladie à coronavirus 2019 (COVID-19), causée par le coronavirus 2 du syndrome respiratoire aigu sévère (SARS-CoV-2), une recherche effrénée dantiviraux e
Les composés antiviraux dérivés des microalgues pourraient-ils combattre le SRAS-CoV-2 et d'autres virus ?
Avec lémergence de la pandémie actuelle de la maladie à coronavirus 2019 (COVID-19), causée par le coronavirus 2 du syndrome respiratoire aigu sévère (SARS-CoV-2), une recherche effrénée dantiviraux e
 La respiration d'hydrogène ne vient pas de l'atoll de Bikini
En ces jours avec tous les discours stupides sur la guerre nucléaire, quand vous voyez le mot hydrogène, vous pouvez immédiatement penser à cette pauvre petite île du Pacifique, Atoll de Bikini, où il
La respiration d'hydrogène ne vient pas de l'atoll de Bikini
En ces jours avec tous les discours stupides sur la guerre nucléaire, quand vous voyez le mot hydrogène, vous pouvez immédiatement penser à cette pauvre petite île du Pacifique, Atoll de Bikini, où il