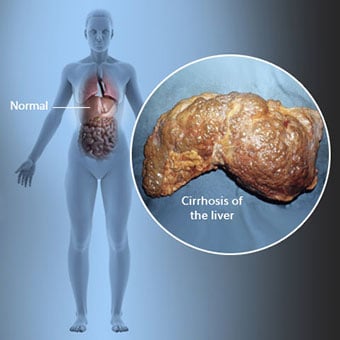
 Kirroosi on maksasairauden komplikaatio, johon liittyy maksasolujen menetys ja maksan peruuttamaton arpeutuminen.
Kirroosi on maksasairauden komplikaatio, johon liittyy maksasolujen menetys ja maksan peruuttamaton arpeutuminen. Kirroosia sairastavilla henkilöillä voi olla vähän tai ei ollenkaan maksasairauden oireita ja merkkejä. Jotkut oireista voivat olla epäspesifisiä, eli ne eivät viittaa siihen, että maksa olisi niiden syy. Jotkut yleisimmistä kirroosin oireista ja merkeistä ovat:
Kirroosia sairastaville henkilöille kehittyy myös oireita ja merkkejä kirroosin komplikaatioista.
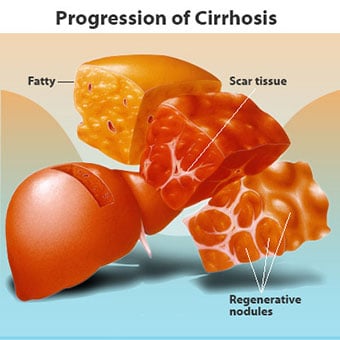 Kirroosiin on monia syitä, mukaan lukien kemikaalit (kuten alkoholi, rasva ja tietyt lääkkeet), virukset ja myrkylliset metallit ja autoimmuuni maksasairaus, jossa elimistön immuunijärjestelmä hyökkää maksaa.
Kirroosiin on monia syitä, mukaan lukien kemikaalit (kuten alkoholi, rasva ja tietyt lääkkeet), virukset ja myrkylliset metallit ja autoimmuuni maksasairaus, jossa elimistön immuunijärjestelmä hyökkää maksaa. Kirroosi on monien maksasairauksien komplikaatio, joille on ominaista epänormaali maksan rakenne ja toiminta. Kirroosiin johtavat sairaudet tekevät niin, koska ne vahingoittavat ja tappavat maksasoluja, minkä jälkeen kuoleviin maksasoluihin liittyvä tulehdus ja korjaus aiheuttavat arpikudoksen muodostumista. Maksasolut, jotka eivät kuole, lisääntyvät yrittäessään korvata kuolleet solut. Tämä johtaa vasta muodostuneiden maksasolujen (regeneratiivisten kyhmyjen) ryhmittymiin arpikudoksessa. Kirroosiin on monia syitä, mukaan lukien kemikaalit (kuten alkoholi, rasva ja tietyt lääkkeet), virukset, myrkylliset metallit (kuten rauta ja kupari, jotka kerääntyvät maksaan geneettisten sairauksien seurauksena) ja autoimmuuni maksasairaus, jossa elimistön immuunijärjestelmä hyökkää maksaa vastaan.
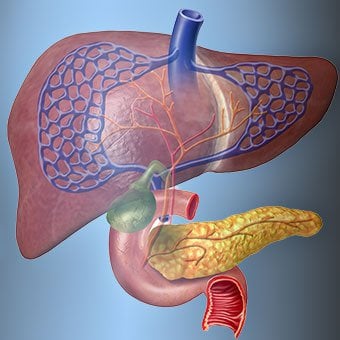
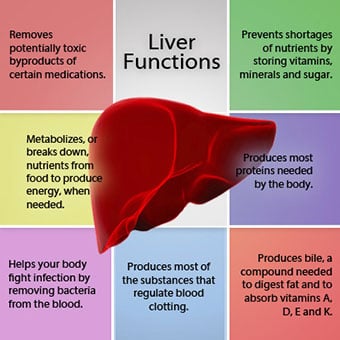 Maksan suhde vereen on ainutlaatuinen.
Maksan suhde vereen on ainutlaatuinen. Maksa on tärkeä elin kehossa. Se suorittaa monia kriittisiä toimintoja, joista kaksi on elimistön tarvitsemien aineiden tuottamista, esimerkiksi veren hyytymisen kannalta välttämättömien proteiinien hyytymistä ja keholle haitallisten myrkyllisten aineiden, kuten lääkkeiden, poistamista. . Maksalla on myös tärkeä rooli glukoosin (sokerin) ja lipidien (rasva) saannin säätelyssä, joita keho käyttää polttoaineena. Näiden kriittisten toimintojen suorittamiseksi maksasolujen on toimittava normaalisti ja niiden on oltava lähellä verta, koska maksan lisäämät tai poistamat aineet kulkeutuvat veren mukana maksaan ja sieltä pois.
Maksan suhde vereen on ainutlaatuinen. Toisin kuin useimmat kehon elimet, vain pieni määrä verta toimitetaan maksaan valtimoiden kautta. Suurin osa maksan verestä tulee suoliston suonista, kun veri palaa sydämeen. Päälaskimoa, joka palauttaa verta suolistosta, kutsutaan portaalilaskimoksi. Kun porttilaskimo kulkee maksan läpi, se hajoaa yhä pienemmiksi ja pienemmiksi laskimoiksi. Pienimmät suonet (joita kutsutaan sinusoideiksi niiden ainutlaatuisen rakenteen vuoksi) ovat läheisessä kosketuksessa maksasolujen kanssa. Maksasolut asettuvat riviin sinusoidien pituudella. Tämä läheinen suhde maksasolujen ja porttilaskimosta tulevan veren välillä antaa maksasoluille mahdollisuuden poistaa ja lisätä aineita vereen. Kun veri on kulkenut poskionteloiden läpi, se kerääntyy yhä suurempiin ja suurempiin suoniin, jotka lopulta muodostavat yhden suonen, maksalaskimon, joka palauttaa veren sydämeen.
Kirroosissa veren ja maksasolujen välinen suhde tuhoutuu. Vaikka selviytyneet tai vasta muodostuneet maksasolut saattavat kyetä tuottamaan ja poistamaan aineita verestä, niillä ei ole normaalia, läheistä suhdetta veren kanssa, mikä häiritsee maksasolujen kykyä lisätä tai poistaa aineita. verestä. Lisäksi maksakirroosissa oleva arpeutuminen estää veren virtauksen maksan läpi ja maksasoluihin. Veren virtauksen maksan läpi tukoksen seurauksena veri "palautuu" porttilaskimoon ja paine porttilaskimossa kasvaa, tila, jota kutsutaan portaaliverenpaineeksi. Virtauksen tukkeutumisen ja porttilaskimon korkeiden paineiden vuoksi porttilaskimossa oleva veri etsii muita laskimoita, joista palaa sydämeen, laskimoihin, joiden paineet ovat alhaisemmat ja jotka ohittavat maksan. Valitettavasti maksa ei pysty lisäämään tai poistamaan verestä aineita, jotka ohittavat sen. Se on yhdistelmä maksasolujen vähentymisestä, maksan läpi kulkevan veren ja maksasolujen välisen normaalin kontaktin menettämisestä ja maksan ohittamisesta, mikä johtaa moniin kirroosin oireisiin.
Toinen syy kirroosin aiheuttamiin ongelmiin on häiriintynyt maksasolujen ja sapen virtauskanavien välinen suhde. Sappi on maksasolujen tuottama neste, jolla on kaksi tärkeää tehtävää:ruuansulatuksen edistäminen ja myrkyllisten aineiden poistaminen elimistöstä. Maksasolujen tuottama sappi erittyy hyvin pieniin kanaviin, jotka kulkevat sinusoideja ympäröivien maksasolujen välissä, joita kutsutaan canaliculiksi. Kanalikulit tyhjenevät pieniksi kanaviksi, jotka sitten liittyvät yhteen muodostaen yhä suurempia kanavia. Kaikki kanavat yhdistyvät yhdeksi kanavaksi, joka menee ohutsuoleen, jossa se voi auttaa ruoansulatuksessa. Samaan aikaan sapen sisältämät myrkylliset aineet pääsevät suolistoon ja poistuvat sitten ulosteesta. Kirroosissa kanavat ovat epänormaaleja ja maksasolujen ja kanaalien välinen suhde tuhoutuu, aivan kuten maksasolujen ja veren välinen suhde sinusoideissa. Tämän seurauksena maksa ei pysty poistamaan myrkyllisiä aineita normaalisti, ja ne voivat kertyä elimistöön. Pienessä määrin ruoansulatus myös suolistossa heikkenee.
 Kirroosin yleisiä oireita ja merkkejä ovat keltaisuus, väsymys, heikkous, ruokahaluttomuus, kutina ja helposti syntyvät mustelmat.
Kirroosin yleisiä oireita ja merkkejä ovat keltaisuus, väsymys, heikkous, ruokahaluttomuus, kutina ja helposti syntyvät mustelmat. Kirroosia sairastavilla ihmisillä voi olla vähän tai ei ollenkaan maksasairauden oireita ja merkkejä. Jotkut oireista voivat olla epäspesifisiä eivätkä viittaa maksan syynä. Kirroosin yleisiä oireita ja merkkejä ovat:
Maksakirroosia sairastaville ihmisille kehittyy myös oireita ja merkkejä taudin komplikaatioista.
Kirroosi itsessään on jo maksavaurion myöhäinen vaihe. Maksasairauden alkuvaiheessa on maksatulehdus. Jos tätä tulehdusta ei hoideta, se voi johtaa arpeutumiseen (fibroosiin). Tässä vaiheessa maksa on vielä mahdollista parantua hoidolla.
Jos maksafibroosia ei hoideta, se voi johtaa kirroosiin. Tässä vaiheessa arpikudos ei voi parantua, mutta arpeutumisen etenemistä voidaan estää tai hidastaa. Kirroosia sairastaville, joilla on merkkejä komplikaatioista, voi kehittyä loppuvaiheen maksasairaus (ESLD), ja ainoa hoito tässä vaiheessa on maksansiirto.
 Turvotus, askites ja bakteeriperäisen peritoniitin komplikaatiot
Turvotus, askites ja bakteeriperäisen peritoniitin komplikaatiot Kun maksakirroosi muuttuu vakavaksi, munuaisiin lähetetään signaaleja suolan ja veden säilyttämiseksi kehossa. Ylimääräinen suola ja vesi kerääntyvät ensin nilkkojen ja jalkojen ihon alla olevaan kudokseen painovoiman vaikutuksesta seistessä tai istuessa. Tätä nesteen kertymistä kutsutaan perifeeriseksi turvotukseksi tai pisteturvotukseksi. (Pitkäturvotus viittaa siihen, että sormenpään painaminen lujasti nilkkaa tai jalkaa vasten, jossa on turvotus, aiheuttaa ihoon painuman, joka säilyy jonkin aikaa paineen vapautumisen jälkeen. Kaikenlainen paine, kuten sukan kuminauhasta , voi riittää aiheuttamaan pistesyöpymistä.) Turvotus on usein pahempi päivän lopussa seisomisen tai istumisen jälkeen ja voi vähentyä yön aikana makuulla. Kun maksakirroosi pahenee ja suolaa ja vettä kerääntyy enemmän, nestettä voi myös kertyä vatsaonteloon vatsan seinämän ja vatsan elinten väliin (kutsutaan askitekseksi), mikä aiheuttaa vatsan turvotusta, epämukavuutta vatsassa ja painon nousua.
Neste vatsaontelossa (askites) on täydellinen paikka bakteereille kasvaa. Normaalisti vatsaontelo sisältää hyvin pienen määrän nestettä, joka kestää hyvin infektioita, ja vatsaan (yleensä suolistosta) tulevat bakteerit kuolevat tai pääsevät porttilaskimoon ja maksaan, jossa ne kuolevat. Kirroosissa vatsaan kertynyt neste ei pysty normaalisti vastustamaan infektiota. Lisäksi enemmän bakteereja löytää tiensä suolistosta askitekseen. Vatsan sisällä ja askites-infektio, jota kutsutaan spontaaniksi bakteeriperäiseksi peritoniitiksi tai SBP:ksi, esiintyy todennäköisesti. SBP on henkeä uhkaava komplikaatio. Joillakin SBP-potilailla ei ole oireita, kun taas toisilla on kuumetta, vilunväristyksiä, vatsakipua ja arkuutta, ripulia ja pahenevaa askitesta.
 Verenvuoto ja pernan komplikaatiot
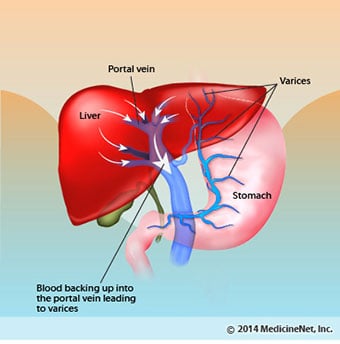
Verenvuoto ja pernan komplikaatiot Maksakirroosissa arpikudos estää suolistosta sydämeen palaavan veren virtauksen ja nostaa painetta portaalilaskimossa (portaalihypertensio). Kun paine porttilaskimossa nousee riittävän korkeaksi, se saa veren virtaamaan maksan ympärille suonten kautta, joiden paine on alhaisempi ja saavuttaa sydämen. Yleisimmät suonet, joiden kautta veri ohittaa maksan, ovat ruokatorven alaosaa ja mahalaukun yläosaa ympäröivät suonet.
Lisääntyneen verenvirtauksen ja siitä johtuvan paineen nousun seurauksena ruokatorven alaosan ja vatsan yläosan suonet laajenevat, ja niitä kutsutaan sitten ruokatorven ja mahalaukun suonikohjuiksi; Mitä korkeampi portaalipaine, sitä suurempia suonikohjuja on ja sitä todennäköisemmin potilas vuotaa verta suonikohjuista ruokatorveen tai vatsaan.
Suonikohjujen aiheuttama verenvuoto on vakavaa ja ilman välitöntä hoitoa voi olla kohtalokasta. Suonikohjujen aiheuttaman verenvuodon oireita ovat veren oksentelu (se voi näkyä punaisena verenä, johon on sekoitettu hyytymiä tai "kahviporoa"), uloste, joka on musta ja tervamainen johtuen veren muutoksista, kun se kulkee suolen läpi (melena) ja ortostaattinen uloste. huimaus tai pyörtyminen (johtuu verenpaineen laskusta erityisesti makuuasennosta noustessa).
Verenvuotoa voi harvoin esiintyä muualle suolistoon, esimerkiksi paksusuoleen, muodostuvista suonikohjuista. Potilailla, jotka joutuvat sairaalaan aktiivisesti verenvuotoa aiheuttavien ruokatorven suonikohjujen vuoksi, on suuri riski saada spontaani bakteeriperäinen vatsakalvotulehdus, vaikka syitä tähän ei vielä tunneta.
Perna toimii normaalisti suodattimena, joka poistaa vanhemmat punasolut, valkosolut ja verihiutaleet (pieniä hiukkasia, jotka ovat tärkeitä veren hyytymiselle). Veri, joka valuu pernasta, liittyy vereen portaalilaskimossa suolistosta. Kun paine porttilaskimossa nousee kirroosissa, se estää yhä enemmän veren virtausta pernasta. Pernaan kertyy veri, ja perna turpoaa kooltaan, ja tätä tilaa kutsutaan splenomegaliaksi. Joskus perna on niin laajentunut, että se aiheuttaa vatsakipua.
Kun perna suurenee, se suodattaa yhä enemmän verisoluja ja verihiutaleita, kunnes niiden määrä veressä vähenee. Hypersplenismi on termi, jota käytetään kuvaamaan tätä tilaa, ja se liittyy alhaiseen punasolujen määrään (anemia), alhaiseen valkosolujen määrään (leukopenia) ja/tai alhaiseen verihiutaleiden määrään (trombosytopenia). Anemia voi aiheuttaa heikkoutta, leukopenia voi johtaa infektioihin ja trombosytopenia voi heikentää veren hyytymistä ja johtaa pitkittyneeseen verenvuotoon
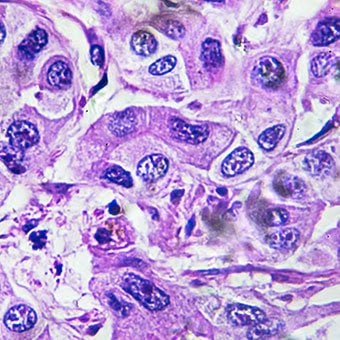 Maksan (maksa) komplikaatiot
Maksan (maksa) komplikaatiot Mistä tahansa syystä johtuva kirroosi lisää primaarisen maksasyövän (hepatosellulaarisen karsinooman) riskiä. Ensisijainen viittaa siihen, että kasvain on peräisin maksasta. Toissijainen maksasyövä on syöpä, joka on peräisin muualta kehosta ja leviää (metastasoituu) maksaan.
Primaarisen maksasyövän yleisimmät oireet ja merkit ovat vatsakipu ja turvotus, maksan suureneminen, laihtuminen ja kuume. Lisäksi maksasyövät voivat tuottaa ja vapauttaa useita aineita, mukaan lukien aineita, jotka lisäävät punasolujen määrää (erytrosytoosi), matalaa verensokeria (hypoglykemiaa) ja korkeaa veren kalsiumia (hyperkalsemiaa).
Osa ruoassa olevista proteiineista, jotka pakenevat ruoansulatusta ja imeytymistä, käyttävät bakteerit, joita normaalisti esiintyy suolistossa. Kun bakteerit käyttävät proteiinia omiin tarkoituksiinsa, ne tuottavat aineita, joita ne vapauttavat suolistoon imeytyäkseen elimistöön. Joillakin näistä aineista, kuten ammoniakki, voi olla myrkyllisiä vaikutuksia aivoihin. Tavallisesti nämä myrkylliset aineet kulkeutuvat suolesta porttilaskimossa maksaan, jossa ne poistetaan verestä ja myrkyttömät.
Kun maksakirroosi on läsnä, maksasolut eivät voi toimia normaalisti joko siksi, että ne ovat vaurioituneet tai koska ne ovat menettäneet normaalin suhteensa vereen. Lisäksi osa porttilaskimossa olevasta verestä ohittaa maksan muiden suonien kautta. Näiden poikkeavuuksien seurauksena maksasolut eivät pysty poistamaan myrkyllisiä aineita, vaan ne kerääntyvät vereen.
Kun myrkyllisiä aineita kertyy vereen riittävästi, aivojen toiminta heikkenee, tila, jota kutsutaan maksaenkefalopatiaksi. Nukkuminen päivällä yön sijaan (normaalin unirytmin kääntyminen) on maksaenkefalopatian varhainen oire. Muita oireita ovat ärtyneisyys, kyvyttömyys keskittyä tai suorittaa laskelmia, muistin menetys, sekavuus tai masentunut tajunnan taso. Lopulta vaikea hepaattinen enkefalopatia aiheuttaa kooman ja kuoleman.
Myrkylliset aineet tekevät myös maksakirroosipotilaiden aivoista erittäin herkkiä lääkkeille, jotka normaalisti suodattavat ja puhdistavat maksan. Monien lääkkeiden, erityisesti rauhoittavien lääkkeiden ja nukahtamista edistävien lääkkeiden, annoksia saatetaan joutua pienentämään, jotta vältetään myrkyllinen kertymä kirroosissa. Vaihtoehtoisesti voidaan käyttää lääkkeitä, joita ei tarvitse poistaa myrkyistä tai eliminoida elimistöstä maksan kautta, kuten munuaisten kautta eliminoituvia lääkkeitä.
Potilaille, joilla on paheneva kirroosi, voi kehittyä hepatorenaalinen oireyhtymä. Tämä oireyhtymä on vakava komplikaatio, jossa munuaisten toiminta on heikentynyt. Se on toiminnallinen ongelma munuaisissa, mikä tarkoittaa, että munuaisille ei ole fyysistä vauriota. Sen sijaan heikentynyt toiminta johtuu muutoksista tavassa, jolla veri virtaa itse munuaisten läpi. Hepatorenaalinen oireyhtymä määritellään munuaisten progressiiviseksi epäonnistumiseksi puhdistaa aineita verestä ja tuottaa riittävästi virtsaa samalla kun muut munuaisten tärkeät toiminnot, kuten suolan pidättyminen, säilyvät. Jos maksan toiminta paranee tai hepatorenaalista oireyhtymää sairastavalle potilaalle siirretään terve maksa, munuaiset alkavat yleensä toimia taas normaalisti. Tämä viittaa siihen, että munuaisten heikentynyt toiminta johtuu joko myrkyllisten aineiden kerääntymisestä vereen tai epänormaalista maksan toiminnasta, kun maksa ei toimi. Hepatorenaalista oireyhtymää on kahta tyyppiä. Yksi tyyppi esiintyy vähitellen kuukausien aikana. Toinen tapahtuu nopeasti viikossa tai kahdessa.
Joillekin potilaille, joilla on pitkälle edennyt kirroosi, voi harvoin kehittyä hepatopulmonaalinen oireyhtymä. Näillä potilailla voi olla hengitysvaikeuksia, koska tietyt pitkälle edenneen kirroosin aiheuttamat hormonit aiheuttavat keuhkojen epänormaalia toimintaa. Keuhkojen perusongelma on, että keuhkojen pienten verisuonten läpi, jotka ovat kosketuksissa keuhkojen keuhkorakkuloihin (ilmapusseihin), ei virtaa tarpeeksi verta. Keuhkojen läpi virtaava veri ohjautuu keuhkorakkuloiden ympärille, eikä se pysty poimimaan tarpeeksi happea keuhkorakkuloiden ilmasta. Tämän seurauksena potilas kokee hengenahdistusta, erityisesti rasituksessa.
 Kirroosille on 12 yleistä syytä.
Kirroosille on 12 yleistä syytä. Yleiset syyt of cirrhosis of the liver include:
Less common causes of cirrhosis include:
In certain parts of the world (particularly Northern Africa), infection of the liver with a parasite (schistosomiasis) is the most common cause of liver disease and cirrhosis.
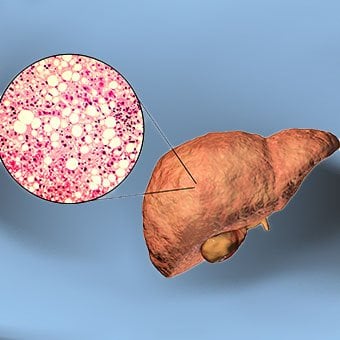 Alcohol and nonalcoholic fatty liver disease are common causes of cirrhosis.
Alcohol and nonalcoholic fatty liver disease are common causes of cirrhosis. Alcohol is a very common cause of cirrhosis, particularly in the Western world. Chronic, high levels of alcohol consumption injure liver cells. Thirty percent of individuals who drink daily at least eight to sixteen ounces of hard liquor or the equivalent for fifteen or more years will develop cirrhosis. Alcohol causes a range of liver diseases, which include simple and uncomplicated fatty liver (steatosis), more serious fatty liver with inflammation (steatohepatitis or alcoholic hepatitis), and cirrhosis.
Nonalcoholic fatty liver disease (NAFLD) refers to a wide spectrum of liver diseases that, like alcoholic liver disease, range from simple steatosis, to nonalcoholic steatohepatitis (NASH), to cirrhosis. All stages of NAFLD have in common the accumulation of fat in liver cells. The term nonalcoholic is used because NAFLD occurs in individuals who do not consume excessive amounts of alcohol, yet in many respects the microscopic picture of NAFLD is similar to what can be seen in liver disease that is due to excessive alcohol. NAFLD is associated with a condition called insulin resistance, which, in turn, is associated with metabolic syndrome and diabetes mellitus type 2. Obesity is the main cause of insulin resistance, metabolic syndrome, and type 2 diabetes. NAFLD is the most common liver disease in the United States and is responsible for up to 25% of all liver disease. The number of livers transplanted for NAFLD-related cirrhosis is on the rise. Public health officials are worried that the current epidemic of obesity will dramatically increase the development of NAFLD and cirrhosis in the population.
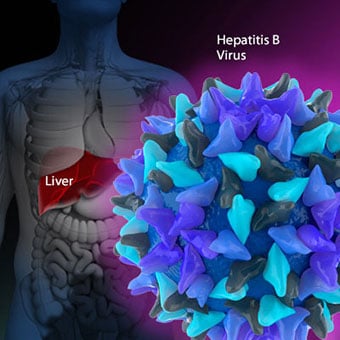 Primary biliary cirrhosis (PBC) is a liver disease caused by an abnormality of the immune system that is found predominantly in women.
Primary biliary cirrhosis (PBC) is a liver disease caused by an abnormality of the immune system that is found predominantly in women. Chronic viral hepatitis is a condition in which hepatitis B or hepatitis C virus infects the liver for years. Most patients with viral hepatitis will not develop chronic hepatitis and cirrhosis. The majority of patients infected with hepatitis A recover completely within weeks, without developing chronic infection. In contrast, some patients infected with hepatitis B virus and most patients infected with hepatitis C virus develop chronic hepatitis, which, in turn, causes progressive liver damage and leads to cirrhosis, and, sometimes, liver cancers.
Autoimmune hepatitis is a liver disease found more commonly in women that is caused by an abnormality of the immune system. The abnormal immune activity in autoimmune hepatitis causes progressive inflammation and destruction of liver cells (hepatocytes), leading ultimately to cirrhosis.
Primary biliary cirrhosis (PBC) is a liver disease caused by an abnormality of the immune system that is found predominantly in women. The abnormal immunity in PBC causes chronic inflammation and destruction of the small bile ducts within the liver. The bile ducts are passages within the liver through which bile travels to the intestine. Bile is a fluid produced by the liver that contains substances required for digestion and absorption of fat in the intestine, as well as other compounds that are waste products, such as the pigment bilirubin. (Bilirubin is produced by the breakdown of hemoglobin from old red blood cells.). Along with the gallbladder, the bile ducts make up the biliary tract. In PBC, the destruction of the small bile ducts blocks the normal flow of bile into the intestine. As the inflammation continues to destroy more of the bile ducts, it also spreads to destroy nearby liver cells. As the destruction of the hepatocytes proceeds, scar tissue (fibrosis) forms and spreads throughout the areas of destruction. The combined effects of progressive inflammation, scarring, and the toxic effects of accumulating waste products culminates in cirrhosis.
Primary sclerosing cholangitis (PSC) is an uncommon disease frequently found in patients with Crohn's disease and ulcerative colitis. In PSC, the large bile ducts outside of the liver become inflamed, narrowed, and obstructed. Obstruction to the flow of bile leads to infections of the bile ducts and jaundice, eventually causing cirrhosis. In some patients, injury to the bile ducts (usually because of surgery) also can cause obstruction and cirrhosis of the liver.
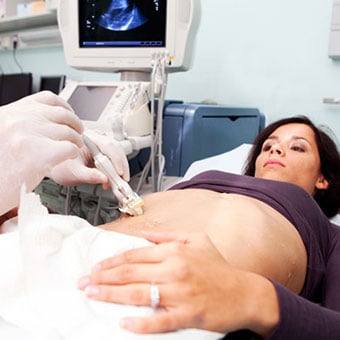 Different liver diseases should be diagnosed by specialists and different tests such as liver blood test, biopsy, and others.
Different liver diseases should be diagnosed by specialists and different tests such as liver blood test, biopsy, and others. Inherited (genetic) disorders that result in the accumulation of toxic substances in the liver, which leads to tissue damage and cirrhosis. Examples include the abnormal accumulation of iron (hemochromatosis) or copper (Wilson disease). In hemochromatosis, patients inherit a tendency to absorb an excessive amount of iron from food. Over time, iron accumulation in different organs throughout the body causes cirrhosis, arthritis, heart muscle damage leading to heart failure, and testicular dysfunction causing loss of sexual drive. Treatment is aimed at preventing damage to organs by removing iron from the body through phlebotomy (removing blood). In Wilson disease, there is an inherited abnormality in one of the proteins that control copper in the body. Over time, copper accumulates in the liver, eyes, and brain. Cirrhosis, tremor, psychiatric disturbances, and other neurological difficulties occur if the condition is not treated early. Treatment is with oral medication, which increases the amount of copper that is eliminated from the body in the urine.
Cryptogenic cirrhosis (cirrhosis due to unidentified causes) is a common reason for liver transplantation. It is termed called cryptogenic cirrhosis because for many years doctors have been being unable to explain why a proportion of patients developed cirrhosis. Doctors now believe that cryptogenic cirrhosis is due to NASH (nonalcoholic steatohepatitis) caused by long-standing obesity, type 2 diabetes, and insulin resistance. The fat in the liver of patients with NASH is believed to disappear with the onset of cirrhosis, and this has made it difficult for doctors to make the connection between NASH and cryptogenic cirrhosis for a long time. One important clue that NASH leads to cryptogenic cirrhosis is the finding of a high occurrence of NASH in the new livers of patients undergoing liver transplant for cryptogenic cirrhosis. Finally, a study from France suggests that patients with NASH have a similar risk of developing cirrhosis as patients with long-standing infection with hepatitis C virus. (See discussion that follows.) However, the progression to cirrhosis from NASH is thought to be slow and the diagnosis of cirrhosis typically is made in people in their sixties.
Infants can be born without bile ducts (biliary atresia) and ultimately develop cirrhosis. Other infants are born lacking vital enzymes for controlling sugars that lead to the accumulation of sugars and cirrhosis. On rare occasions, the absence of a specific enzyme can cause cirrhosis and scarring of the lung (alpha-1 antitrypsin deficiency).
Less common causes of cirrhosis include unusual reactions to some drugs and prolonged exposure to toxins, as well as chronic heart failure (cardiac cirrhosis). In certain parts of the world (particularly Northern Africa), infection of the liver with a parasite (schistosomiasis) is the most common cause of liver disease and cirrhosis.
 Different liver diseases should be diagnosed by specialists and different tests such as liver blood test, biopsy, and others.
Different liver diseases should be diagnosed by specialists and different tests such as liver blood test, biopsy, and others. The single best test for diagnosing cirrhosis is a biopsy of the liver. Liver biopsies carry a small risk for serious complications, and biopsy often is reserved for those patients in whom the diagnosis of the type of liver disease or the presence of cirrhosis is not clear. The history, physical examination, or routine testing may suggest the possibility of cirrhosis. If cirrhosis is present, other tests can be used to determine the severity of the cirrhosis and the presence of complications. Tests also may be used to diagnose the underlying disease that is causing the cirrhosis. Examples of how doctors diagnose and evaluate cirrhosis are:
 There are four types of treatment of cirrhosis.
There are four types of treatment of cirrhosis. Treatment of cirrhosis includes
Consume a balanced diet and one multivitamin daily. Patients with PBC with impaired absorption of fat-soluble vitamins may need additional vitamins D and K.
Avoid drugs (including alcohol) that cause liver damage. All patients with cirrhosis should avoid alcohol. Most patients with alcohol-induced cirrhosis experience an improvement in liver function with abstinence from alcohol. Even patients with chronic hepatitis B and C can substantially reduce liver damage and slow the progression towards cirrhosis with abstinence from alcohol.
Avoid nonsteroidal anti-inflammatory drugs (NSAIDs, e.g., ibuprofen). Patients with cirrhosis can experience worsening of liver and kidney function with NSAIDs.
Eradicate hepatitis B and hepatitis C virus by using anti-viral medications. Not all patients with cirrhosis due to chronic viral hepatitis are candidates for drug treatment. Some patients may experience serious deterioration in liver function and/or intolerable side effects during treatment. Thus, decisions to treat viral hepatitis have to be individualized, after consulting with doctors experienced in treating liver diseases (hepatologists).
Remove blood from patients with hemochromatosis to reduce the levels of iron and prevent further damage to the liver. In Wilson's disease, medications can be used to increase the excretion of copper in the urine to reduce the levels of copper in the body and prevent further damage to the liver.
Suppress the immune system with drugs such as prednisone and azathioprine (Imuran) to decrease inflammation of the liver in autoimmune hepatitis.
Treat patients with PBC with a bile acid preparation, ursodeoxycholic acid (UDCA), also called ursodiol (Actigall). Results of an analysis that combined the results from several clinical trials showed that UDCA increased survival among PBC patients during 4 years of therapy. The development of portal hypertension also was reduced by the UDCA. It is important to note that despite producing clear benefits, UDCA treatment primarily retards progression and does not cure PBC. Other medications such as colchicine and methotrexate also may have benefits in subsets of patients with PBC.
Immunize patients with cirrhosis against infection with hepatitis A and B to prevent a serious deterioration in liver. There are currently no vaccines available for immunizing against hepatitis C.
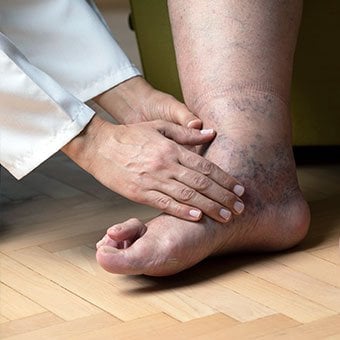 Treatment for edema, ascites, and hypersplenism complications.
Treatment for edema, ascites, and hypersplenism complications. Retaining salt and water can lead to swelling of the ankles and legs (edema) or abdomen (ascites) in patients with cirrhosis. Doctors often advise patients with cirrhosis to restrict dietary salt (sodium) and fluid to decrease edema and ascites. The amount of salt in the diet usually is restricted to 2 grams per day and fluid to 1.2 liters per day. In most patients with cirrhosis, salt and fluid restriction is not enough and diuretics have to be added.
Diuretics are medications that work in the kidneys to promote the elimination of salt and water into the urine. A combination of the diuretics spironolactone (Aldactone) and furosemide (Lasix) can reduce or eliminate the edema and ascites in most patients. During treatment with diuretics, it is important to monitor the function of the kidneys by measuring blood levels of blood urea nitrogen (BUN) and creatinine to determine if too much diuretic is being used. Too much diuretic can lead to kidney dysfunction that is reflected in elevations of the BUN and creatinine levels in the blood.
Sometimes, when the diuretics do not work (in which case the ascites is said to be refractory), a long needle or catheter is used to draw out the ascitic fluid directly from the abdomen, a procedure called abdominal paracentesis. It is common to withdraw large amounts (liters) of fluid from the abdomen when the ascites is causing painful abdominal distension and/or difficulty breathing because it limits the movement of the diaphragms.
Another treatment for refractory ascites is a procedure called transjugular intravenous portosystemic shunting (TIPS).
The spleen normally acts as a filter to remove older red blood cells, white blood cells, and platelets (small particles important for the clotting of blood). The blood that drains from the spleen joins the blood in the portal vein from the intestines. As the pressure in the portal vein rises in cirrhosis, it increasingly blocks the flow of blood from the spleen. The blood "backs-up," accumulating in the spleen, and the spleen swells in size, a condition referred to as splenomegaly. Sometimes, the spleen is so enlarged it causes abdominal pain.
As the spleen enlarges, it filters out more and more of the blood cells and platelets until their numbers in the blood are reduced. Hypersplenism is the term used to describe this condition, and it is associated with a low red blood cell count (anemia), low white blood cell count (leukopenia), and/or a low platelet count (thrombocytopenia). Anemia can cause weakness, leucopenia can lead to infections, and thrombocytopenia can impair the clotting of blood and result in prolonged bleeding.
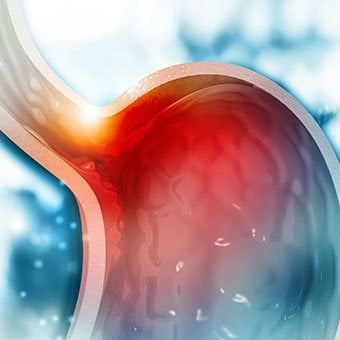 Once varices have bled, they tend to rebleed and the probability that a patient will die from each bleeding episode is high (30% to 35%). Treatment is necessary to prevent the first bleeding episode as well as rebleeding.
Once varices have bled, they tend to rebleed and the probability that a patient will die from each bleeding episode is high (30% to 35%). Treatment is necessary to prevent the first bleeding episode as well as rebleeding. If large varices develop in the esophagus or upper stomach, patients with cirrhosis are at risk for serious bleeding due to rupture of these varices. Once varices have bled, they tend to rebleed and the probability that a patient will die from each bleeding episode is high (30% to 35%). Treatment is necessary to prevent the first bleeding episode as well as rebleeding. Treatments include medications and procedures to decrease the pressure in the portal vein and procedures to destroy the varices.
 Hepatic encephalopathy usually should be treated with a low protein diet and oral lactulose.
Hepatic encephalopathy usually should be treated with a low protein diet and oral lactulose. Patients with an abnormal sleep cycle, impaired thinking, odd behavior, or other signs of hepatic encephalopathy usually should be treated with a low protein diet and oral lactulose. Dietary protein is restricted because it is a source of toxic compounds that cause hepatic encephalopathy. Lactulose, which is a liquid, traps toxic compounds in the colon so they cannot be absorbed into the bloodstream, and thus cause encephalopathy. Lactulose is converted to lactic acid in the colon, and the acidic environment that results is believed to trap the toxic compounds produced by the bacteria. To be sure adequate lactulose is present in the colon at all times, the patient should adjust the dose to produce 2 to 3 semiformed bowel movements a day. Lactulose is a laxative, and the effectiveness of treatment can be judged by loosening or increasing the frequency of stools. Rifaximin (Xifaxan) is an antibiotic taken orally that is not absorbed into the body but rather remains in the intestines. It is the preferred mode of treatment of hepatic encephalopathy. Antibiotics work by suppressing the bacteria that produce the toxic compounds in the colon.
 Most patients with spontaneous bacterial peritonitis are hospitalized and treated with intravenous antibiotics.
Most patients with spontaneous bacterial peritonitis are hospitalized and treated with intravenous antibiotics. Patients suspected of having spontaneous bacterial peritonitis usually will undergo paracentesis. The fluid that is removed is examined for white blood cells and cultured for bacteria. Culturing involves inoculating a sample of the ascites into a bottle of nutrient-rich fluid that encourages the growth of bacteria, thus facilitating the identification of even small numbers of bacteria. Blood and urine samples also are often obtained for culturing because many patients with spontaneous bacterial peritonitis also will have infections in their blood and urine. Many doctors believe the infection may have begun in the blood and the urine and spread to the ascitic fluid to cause spontaneous bacterial peritonitis. Most patients with spontaneous bacterial peritonitis are hospitalized and treated with intravenous antibiotics such as cefotaxime (Claforan). Patients usually treated with antibiotics include:
Spontaneous bacterial peritonitis is a serious infection. It often occurs in patients with advanced cirrhosis whose immune systems are weak, but with modern antibiotics and early detection and treatment, the prognosis of recovering from an episode of spontaneous bacterial peritonitis is good.
In some patients, oral antibiotics (norfloxacin [Noroxin] or sulfamethoxazole and trimethoprim [Bactrim]) can be prescribed to prevent spontaneous bacterial peritonitis. Not all patients with cirrhosis and ascites should be treated with antibiotics to prevent spontaneous bacterial peritonitis, but some patients are at high risk for developing spontaneous bacterial peritonitis and warrant preventive treatment.
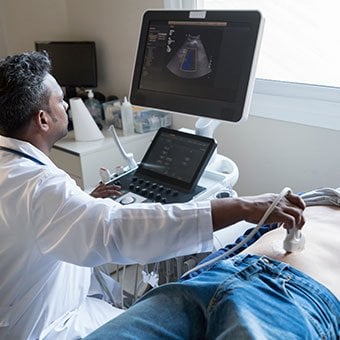 The prognosis and life expectancy for cirrhosis of the liver varies and depends on the cause, the severity, any complications, and any underlying diseases.
The prognosis and life expectancy for cirrhosis of the liver varies and depends on the cause, the severity, any complications, and any underlying diseases. Several types of liver disease that cause cirrhosis (such as hepatitis B and C) are associated with a high incidence of liver cancer. It is useful to screen for liver cancer in patients with cirrhosis, as early surgical treatment or transplantation of the liver can cure the patient of cancer. The difficulty is that the methods available for screening are only partially effective, identifying at best only half of patients at a curable stage of their cancer. Despite the partial effectiveness of screening, most patients with cirrhosis, particularly hepatitis B and C, are screened yearly or every six months with ultrasound examination of the liver and measurements of cancer-produced proteins in the blood, for example, alpha-fetoprotein.
Cirrhosis is irreversible. Liver function usually gradually worsens despite treatment, and complications of cirrhosis increase and become difficult to treat. When cirrhosis is far advanced liver transplantation often is the only option for treatment. Recent advances in surgical transplantation and medications to prevent infection and rejection of the transplanted liver have greatly improved survival after transplantation. On average, more than 80% of patients who receive transplants are alive after five years. Not everyone with cirrhosis is a candidate for transplantation. Furthermore, there is a shortage of livers to transplant, and they're usually is a long (months to years) wait before a liver for transplanting becomes available. Measures to slow the progression of liver disease, and treat and prevent complications of cirrhosis are vitally important.
The prognosis and life expectancy for cirrhosis of the liver varies and depends on the cause, the severity, any complications, and any underlying diseases.
Progress in the management and prevention of cirrhosis continues. Research is ongoing to determine the mechanism of scar formation in the liver and how this process of scarring can be interrupted or even reversed. Newer and better treatments for viral liver disease are being developed to prevent the progression to cirrhosis. Prevention of viral hepatitis by vaccination, which is available for hepatitis B, is being developed for hepatitis C. Treatments for the complications of cirrhosis are being developed or revised, and tested continually. Finally, research is being directed at identifying new proteins in the blood that can detect liver cancer early or predict which patients will develop liver cancer.
 Kortisoliongelmat laukaisevat vuotavan suoliston (ja aiheuttavat aivoongelmia)
Kortisoliongelmat laukaisevat vuotavan suoliston (ja aiheuttavat aivoongelmia)
 Autoimmuunisairauden geneettinen riski voi liittyä suoliston mikrobiomin eroihin
Autoimmuunisairauden geneettinen riski voi liittyä suoliston mikrobiomin eroihin
 Laajentuneen pernan (splenomegalia) oireet, merkit, syyt ja hoito
Laajentuneen pernan (splenomegalia) oireet, merkit, syyt ja hoito
 Kuinka pysäytän veren virtsassani?
Kuinka pysäytän veren virtsassani?
 Mikä on Braunin enteroesterostomia?
Mikä on Braunin enteroesterostomia?
 Poista SCD-harjoituspyörät luomalla elintarviketurvallinen vyöhyke
Poista SCD-harjoituspyörät luomalla elintarviketurvallinen vyöhyke
 Viskeraalinen yliherkkyys ja IBS
Jos koet sisäelinten yliherkkyyttä, se tarkoittaa, että vatsakivun ja -epämukavuuden kynnys on alhainen vasteena vatsan paineelle, stimulaatiolle tai turvotukselle. Viskeraalinen yliherkkyys (viskeraa
Viskeraalinen yliherkkyys ja IBS
Jos koet sisäelinten yliherkkyyttä, se tarkoittaa, että vatsakivun ja -epämukavuuden kynnys on alhainen vasteena vatsan paineelle, stimulaatiolle tai turvotukselle. Viskeraalinen yliherkkyys (viskeraa
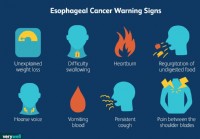 Mikä on ruokatorven syöpä?
Ruokotorven syöpä on harvinainen, ja se muodostaa noin 1 % diagnosoiduista syövistä Yhdysvalloissa. Aiemmin ruokatorven okasolusyöpä, joka liittyi tupakointiin ja liialliseen alkoholin käyttöön, oli y
Mikä on ruokatorven syöpä?
Ruokotorven syöpä on harvinainen, ja se muodostaa noin 1 % diagnosoiduista syövistä Yhdysvalloissa. Aiemmin ruokatorven okasolusyöpä, joka liittyi tupakointiin ja liialliseen alkoholin käyttöön, oli y
 Kuinka psykologian avulla voita kaikki SCD:n takaiskut
Tänään on perseestä. Tänään en voi hyvin. Olen ollut SCD-dieetillä melkein kaksi vuotta ja minulla on edelleen huonoja päiviä aina silloin tällöin. Minun on esitettävä, että ruoansulatukseni on ollu
Kuinka psykologian avulla voita kaikki SCD:n takaiskut
Tänään on perseestä. Tänään en voi hyvin. Olen ollut SCD-dieetillä melkein kaksi vuotta ja minulla on edelleen huonoja päiviä aina silloin tällöin. Minun on esitettävä, että ruoansulatukseni on ollu