El intestino es una ruta de infección bien establecida y el objetivo del daño viral por el coronavirus 2 del síndrome respiratorio agudo severo (SARS-CoV-2), el agente causante de COVID-19. Esto está respaldado por la observación clínica de que aproximadamente la mitad de los pacientes con COVID-19 presentan síntomas gastrointestinales (GI).
Los pacientes hospitalizados con COVID-19 crítico también suelen tener complicaciones intestinales. Además de lo anterior, se informa tromboembolismo venoso o arterial de los vasos mesentéricos e isquemia del intestino delgado, especialmente en pacientes hospitalizados por períodos más prolongados.
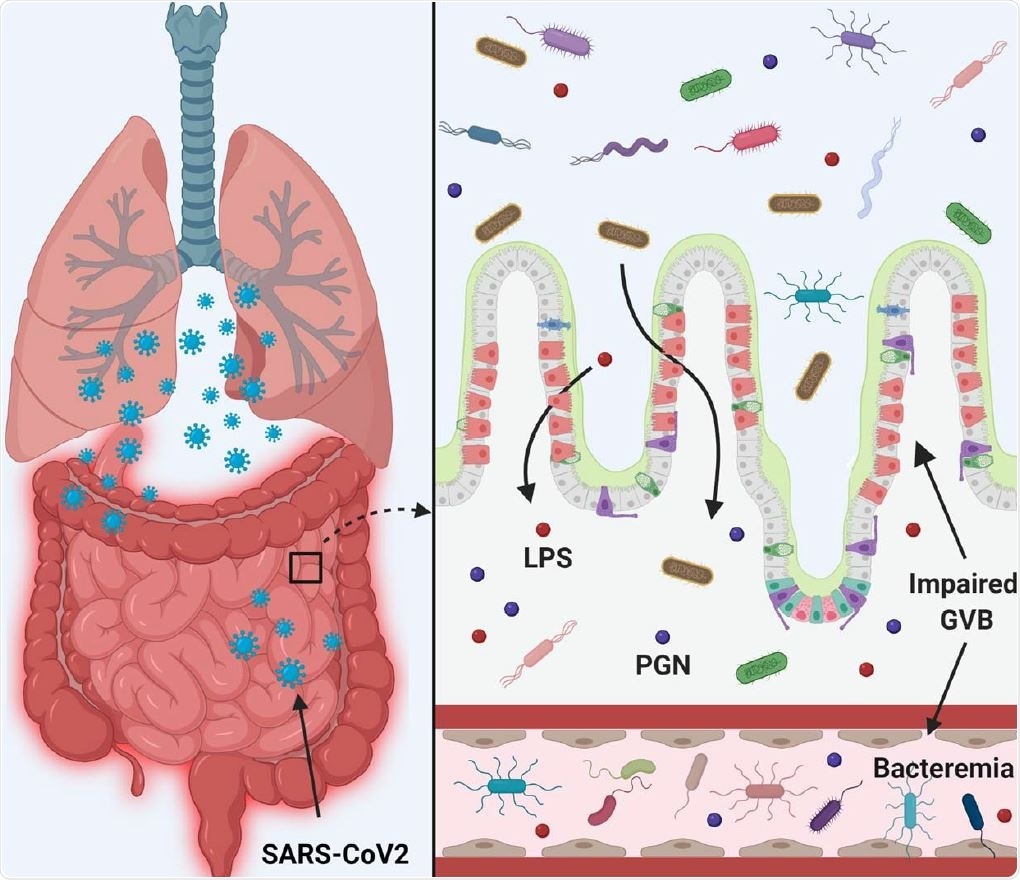 La infección por SARS-CoV-2 altera la barrera intestinal y conduce a la elevación del lipopolisacárido bacteriano sistémico y peptidoglicano y sirve para mejorar la inflamación sistémica. Por lo tanto, el intestino permeable y la disbiosis microbiana podrían contribuir a la tormenta de citocinas en pacientes gravemente enfermos con COVID -19.
La infección por SARS-CoV-2 altera la barrera intestinal y conduce a la elevación del lipopolisacárido bacteriano sistémico y peptidoglicano y sirve para mejorar la inflamación sistémica. Por lo tanto, el intestino permeable y la disbiosis microbiana podrían contribuir a la tormenta de citocinas en pacientes gravemente enfermos con COVID -19. El estudio actual, con sede en Birmingham, Alabama, en los EE.UU, dirigido a capturar la presencia de biomarcadores en plasma que indican rupturas de la barrera epitelial intestinal, y la presencia de microbios intestinales en el plasma.
Desafortunadamente, ambos no pudieron probarse en el mismo subconjunto de pacientes debido al pequeño volumen de plasma disponible.
De los 30 pacientes incluidos en el estudio con infección confirmada por SARS-CoV-2, todos tenían diarrea y náuseas junto con fiebre y dificultad para respirar. La mediana de edad fue de 63 años. Solo dos pacientes tenían una enfermedad crítica.
Más de un tercio eran diabéticos, y la mitad experimentó coágulos de sangre. De los 30, 23 pacientes tenían sobrepeso. Cinco pacientes tuvieron un desenlace fatal en el hospital.
Se observaron linfopenia y anemia en la mitad, y dos tercios de los pacientes, junto con altos recuentos de monocitos. Los neutrófilos también estaban elevados, en el 60% de los hombres frente al 45% de las mujeres. Esto es importante ya que son los primeros en responder a cualquier infección.
El recuento total de leucocitos se elevó en aproximadamente el 40% de las personas con COVID-19, pero se observaron anomalías en el recuento de plaquetas sólo en el 17% de los sujetos. Solo dos pacientes mostraron niveles altos de péptido natriurético cerebral (BNP), probablemente debido a insuficiencia cardíaca.
Péptido C-reactivo, un marcador inflamatorio, estaba elevado en todos los pacientes, con seis pacientes que muestran niveles consistentes con inflamación severa. Ocho sujetos mostraron niveles altos de ferritina, y la mitad de ellos tienen niveles indicativos de inflamación.
Casi todos los pacientes tenían niveles elevados de glucosa en ayunas y lactato deshidrogenasa (LDH). Aproximadamente dos tercios tenían anemia, Aumento de los niveles de troponina-I, sugiriendo lesión cardíaca, se encontraron en el 80% de los sujetos masculinos, vs solo un sujeto femenino.
Las 14 muestras de plasma enviadas para la evaluación de la presencia de bacterias arrojaron más de 150, 000 lecturas de secuenciación, con la señal que indica una fuerte presencia bacteriana en dos tercios de las muestras. La población microbiana total fue comparable entre los pacientes con COVID-19.
Usando la reacción en cadena de la polimerasa, Se llegó a un índice de disbiosis para medir la abundancia de grupos bacterianos en cada muestra. Las nueve muestras que indicaron la presencia de bacterias mostraron los mismos tres filos principales, Proteobacterias , Firmicutes , y Actinobacterias , con un paciente que muestra bacterias desconocidas en números más significativos entre los 14.
Estos son los mismos que se han encontrado en plasma sano, así como.
El filo más enriquecido fue Proteobacterias , tiempo Bacteroides estaban presentes en un número muy limitado. Entre los dos pacientes con un resultado fatal de COVID-19, el número de Firmicutes fue bajo. Quizás la abundancia de este filo pueda ser un biomarcador de la gravedad de la enfermedad.
Tanto bacterias Gram negativas como lipopolisacáridos (LPS), que es una endotoxina importante que se origina en la pared celular de estas bacterias, son mayores en las muestras de plasma de pacientes con COVID-19.
La presencia de microbios intestinales en el plasma puede sugerir defectos en la barrera epitelial intestinal. permitiendo que las bacterias migren a través de las células epiteliales hacia los vasos sanguíneos sistémicos. Este es un componente importante en la inflamación sistémica y subyace en la progresión de COVID-19 en estos pacientes.
Como marcador de la permeabilidad intestinal, Se midieron los niveles de proteína 2 de unión a ácidos grasos (FABP2), ya que esta es una proteína que se encuentra dentro de las células epiteliales intestinales para unirse a los ácidos grasos libres, colesterol, y retinoides. Como tal, su elevación en plasma indica daño de las mucosas en el intestino.
Como se esperaba, Los niveles de FABP2 eran altos en el plasma de los pacientes con COVID-19 en relación con los individuos sanos.
Los péptidos microbianos intestinales en el plasma son tóxicos porque desencadenan vías inflamatorias y provocan daño sistémico. Como medida de este fenómeno, los investigadores observaron niveles más altos de peptidoglicano (PGN) y LPS en plasma COVID-19, en casi el doble de los niveles de los controles sanos.
La translocación de microbios intestinales, normalmente se encuentra solo en las heces, en la circulación sistémica es un determinante fundamental de la función inmunológica y el metabolismo. La presencia de microbios intestinales en el plasma puede desencadenar y también exacerbar las vías de señalización inflamatoria en el cuerpo.
La inflamación es clave para la patogenia del COVID-19 grave y crítico. Los hallazgos de este estudio pueden respaldar la teoría de que esto es impulsado por el movimiento de las bacterias intestinales hacia la circulación del cuerpo en estos pacientes. Esta, Sucesivamente, podría deberse a una mayor permeabilidad intestinal debido a la disfunción de la barrera epitelial.
Se ha descubierto que la diseminación del virus en las heces persiste hasta un mes después de que se resuelven los síntomas pulmonares. lo que indica que la colonización viral del intestino puede ser de mayor duración que la de las vías respiratorias.
Los pacientes con COVID-19 en esta muestra tenían más probabilidades de ser diabéticos y obesos en comparación con los controles. En tales pacientes, las bacterias comensales Lactobacillus son menos abundantes, y esta reducción se encontró en un pequeño grupo de nueve pacientes evaluados al comienzo de la hospitalización en este estudio.
La mayoría de las muertes por COVID-19 se deben a sepsis. En este estudio, la abundancia de múltiples especies patógenas como Acinetobacter y Pseudomona estaba más alto en el intestino. Incluso después de que la infección se resolvió, persistió la disbiosis, lo que indica que el intestino puede sufrir los efectos de esta enfermedad a largo plazo.
El metaboloma plasmático está vinculado al microbioma intestinal en la patogenia de muchas enfermedades. La falla de la barrera intestinal conduce a la detección de productos metabólicos bacterianos en el plasma, en condiciones como la colitis ulcerosa.
El estudio sugiere, " L El intestino débil y la disbiosis microbiana podrían contribuir a la tormenta de citocinas en pacientes gravemente enfermos con COVID -19. . "
bioRxiv publica informes científicos preliminares que no son revisados por pares y, por lo tanto, no debe considerarse concluyente, orientar la práctica clínica / comportamiento relacionado con la salud, o tratada como información establecida.
 Infliximab puede obstaculizar la eficacia de algunas vacunas COVID-19
Infliximab puede obstaculizar la eficacia de algunas vacunas COVID-19
 La disbiosis en la microbiota intestinal puede causar una infección secundaria grave en pacientes con COVID-19
La disbiosis en la microbiota intestinal puede causar una infección secundaria grave en pacientes con COVID-19
 Microbios relacionados con ataques cardíacos hallan estudio
Microbios relacionados con ataques cardíacos hallan estudio
 La apoptosis es un mediador importante de la patogénesis en la infección por coronavirus animal
La apoptosis es un mediador importante de la patogénesis en la infección por coronavirus animal
 Un hongo común que se encuentra en la piel puede causar enfermedad inflamatoria intestinal
Un hongo común que se encuentra en la piel puede causar enfermedad inflamatoria intestinal
 La investigación muestra cómo los microbios intestinales afectan la gripe estomacal
La investigación muestra cómo los microbios intestinales afectan la gripe estomacal
 Es seguro alimentar a las mascotas con alimentos crudos,
encuentra un nuevo estudio Un gran estudio multinacional muestra que los dueños de mascotas no creen que la alimentación con alimentos crudos aumente el riesgo de infección para los miembros del hogar
Es seguro alimentar a las mascotas con alimentos crudos,
encuentra un nuevo estudio Un gran estudio multinacional muestra que los dueños de mascotas no creen que la alimentación con alimentos crudos aumente el riesgo de infección para los miembros del hogar
 La investigación dice que en la infección canina SARS-CoV-2,
transmisión improbable Un nuevo estudio publicado en el servidor de preimpresión bioRxiv * en septiembre de 2020 muestra que los perros de compañía se enfermaron y murieron de una misteriosa infecci
La investigación dice que en la infección canina SARS-CoV-2,
transmisión improbable Un nuevo estudio publicado en el servidor de preimpresión bioRxiv * en septiembre de 2020 muestra que los perros de compañía se enfermaron y murieron de una misteriosa infecci
 El intestino permeable y la disbiosis microbiana podrían contribuir a la tormenta de citocinas en casos de COVID-19 gravemente enfermos
A medida que el mundo se acerca al sombrío hito de tres millones de muertes por la enfermedad COVID-19, un nuevo trabajo de investigación preimpreso publicado en el bioRxiv * servidor muestra que la
El intestino permeable y la disbiosis microbiana podrían contribuir a la tormenta de citocinas en casos de COVID-19 gravemente enfermos
A medida que el mundo se acerca al sombrío hito de tres millones de muertes por la enfermedad COVID-19, un nuevo trabajo de investigación preimpreso publicado en el bioRxiv * servidor muestra que la