Estos virus se denominan bacteriófagos, literalmente, comedores de bacterias - y fagos para abreviar. Si bien los fagos han existido durante mucho tiempo, estos nuevos fagos son sorprendentes en términos de su tamaño y sistemas biológicamente complejos. Muchos de sus genes se encuentran generalmente en bacterias y se utilizan para atacar a las bacterias hospedadoras.
¿Dónde encontraron los científicos estos raros fagos enormes? Estudiaron minuciosamente una vasta base de datos de secuencias de ADN obtenidas de una amplia y diversa gama de entornos en la tierra. Estos casi 30 microbiomas abarcan el espectro de una fuente termal en el Tíbet, a través de biorreactores en Sudáfrica, al intestino de una mujer que lleva un bebé en su útero. Otras ubicaciones incluyen agujeros subterráneos, océanos lagos y el intestino de un bebé prematuro.
La investigadora Jill Banfield ha estado haciendo esto durante más de una década y media. Ella calcula las secuencias de todos los bits de ADN en cualquier muestra que obtenga de un lugar en la tierra. Luego encaja las piezas del rompecabezas para obtener la secuencia genómica.
En la mayoría de los casos, obtiene un borrador del genoma, pero se ha confirmado que algunos son genomas de microbios completamente nuevos. Algunos de estos microbios están regulados por pequeños genomas que, Por supuesto, parece incapaz de sostener la vida de forma independiente, y en cambio dependen completamente de otras formas de vida, a saber, arqueas y bacterias.
Hace un año que informó del hallazgo de grandes fagos, que ella llamó fagos Lak, en el intestino y la boca humanos. Estos fagos comen bacterias en la saliva y el intestino.
En el nuevo periódico ella informa el aislamiento de más de 350 fagos muy grandes con genomas que son, en longitudes de 200, 000 bases, cuatro veces más grande que la secuencia genética promedio de cualquier bacteriófago conocido hasta ahora (50 kb). Banfield comenta, "Estamos explorando los microbiomas de la Tierra, ya veces surgen cosas inesperadas ".
El más grande secuenciado hasta ahora tiene un genoma que abarca unos asombrosos 735, 000 pares de bases, que es aproximadamente 15 veces el tamaño del genoma del fago promedio, y de hecho, notablemente más grande que muchos genomas bacterianos. Pero podría ser aún mayor, ya que solo han secuenciado 175 de estos grandes fagos hasta ahora.
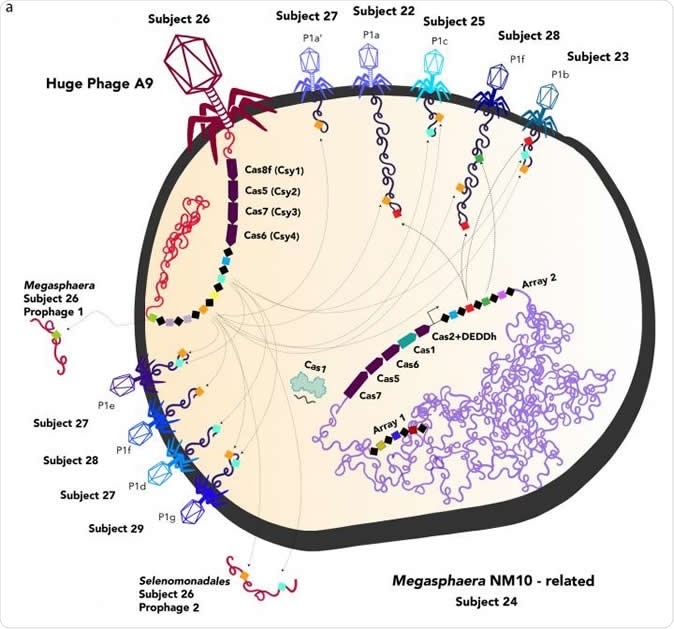 Representación de fagos enormes (rojo, izquierda) y fagos normales que infectan una célula bacteriana. El enorme fago inyecta su ADN en la célula huésped, donde las proteínas Cas, parte del sistema inmunológico CRISPR que generalmente se encuentra solo en bacterias y arqueas, manipulan la respuesta de la célula huésped a otros virus. El equipo de UC Berkeley aún no ha fotografiado ningún fago enorme, por lo que todos se representan como el tipo más común de fago, T4. Crédito de la imagen:UC Berkeley imagen cortesía del laboratorio de Jill Banfield
Representación de fagos enormes (rojo, izquierda) y fagos normales que infectan una célula bacteriana. El enorme fago inyecta su ADN en la célula huésped, donde las proteínas Cas, parte del sistema inmunológico CRISPR que generalmente se encuentra solo en bacterias y arqueas, manipulan la respuesta de la célula huésped a otros virus. El equipo de UC Berkeley aún no ha fotografiado ningún fago enorme, por lo que todos se representan como el tipo más común de fago, T4. Crédito de la imagen:UC Berkeley imagen cortesía del laboratorio de Jill Banfield Estos grandes fagos se clasificaron en diez clados o grupos. Cada uno ha sido llamado "Gran fago" aunque usa diferentes lenguajes, o diferentes palabras en el mismo idioma. Los idiomas son los del país de origen de los investigadores. Por lo tanto, hay un clado Mahaphage, un Biggiephage, un judafago, un Kaempephage, un Dakhmphage un Jabbarphage y un Kabirphage, así como un Enormephage, Whopperphage, y clado Kyodaiphage - en sánscrito, Inglés australiano, Chino, Danés, Árabe (los tres siguientes), Francés, Inglés americano, ¡y japonés!
Los genes bacterianos dentro de estos fagos contienen algunos elementos CRISPR, segmentos de codificación de proteínas de edición de genes, que utilizan las bacterias para resistir el ataque viral. Los científicos creen que estos elementos están destinados a convertirse en parte del sistema CRISPR del anfitrión, empoderando a las bacterias para resistir otros virus para que estos grandes fagos puedan disfrutar de su comida sin interrupciones. Otro investigador, Basem Al-Shayeb, explica que estos fagos usan este sistema para su propio beneficio, "para alimentar la guerra entre estos virus".
Otro elemento fascinante en uno de estos nuevos fagos es una proteína que juega el mismo papel que la proteína Cas-9, una parte integral de la herramienta de edición de genes CRISPR-Cas9 ampliamente utilizada presentada por primera vez por Doudna y Charpentier. Esta nueva proteína se ha llamado CasØ - la letra Ø, o phi (en griego), es el símbolo de un fago. Esto es parte de la familia Cas-12, pero estos fagos también tienen otros elementos CRISPR bacterianos como Cas-9, Cas-X, y proteínas Cas-Y.
Algunos de estos fagos también tienen matrices CRISPR muy grandes. Esto se refiere a la presencia de matrices compuestas por fragmentos de ADN viral, matrices de memoria que permiten el reconocimiento rápido de un ataque repetido por cualquiera de estos virus. Esta, Sucesivamente, desencadena reacciones instantáneas de Cas, permitiendo la focalización específica de estos virus.
Otro hallazgo sorprendente fue la aparición de genes que codifican proteínas ribosómicas. El ribosoma es el orgánulo celular que lee el ARNm y lo usa para producir proteínas específicas. Esta es una de las primeras apariciones de genes ribosomales en virus.
También encontraron genes que codifican la transferencia de ARN, que son las moléculas que recogen los aminoácidos correctos para incorporarlos a la secuencia de proteínas. Hay genes reguladores para los ARNt, genes para activar el proceso de síntesis de proteínas, e incluso algunos segmentos ribosomales. Estos genes se encuentran solo en formas de vida, ya que tienen que ver con la fabricación de componentes proteicos, que es diferente a lo que puede hacer cualquier otro virus. y que es una capacidad que deletrea la vida.
El investigador Rohan Sachdeva dice que esta es "una de las principales características definitorias que separan los virus y las bacterias, la no vida y la vida ". Él llama a esto" difuminar un poco la línea ".
¿Por qué están ahí estos genes? Los investigadores creen que podrían usarse para secuestrar los ribosomas y comenzar a replicar proteínas virales en lugar de proteínas bacterianas del huésped. Un hallazgo adicional es la presencia de códigos genéticos alternativos, o el uso de más de un código genético para denotar el mismo aminoácido. Esta característica bien podría desviar al ribosoma bacteriano y engañarlo para que decodifique el ARN viral en lugar del ARN del propio huésped.
El descubrimiento de nuevas herramientas utilizadas en la lucha entre bacterias y virus ofrece muchas posibilidades para encontrar nuevas herramientas de edición de genes. Muchos de los nuevos genes aún están por explorar por sus funciones, y bien podría ser que estas nuevas proteínas sean útiles en diversas aplicaciones en la industria, las ciencias médicas, o en agricultura.
Hay peligros también. Los virus transfieren genes de una bacteria a otra, algunos de los cuales podrían ser responsables de la resistencia a los antibióticos o de la virulencia (la capacidad de causar enfermedades). Esta propiedad de los fagos recién descubiertos podría significar que existe el riesgo de transferir algunos de estos genes dañinos al microbioma humano, ya que los fagos ocurren junto con las bacterias.
Dado que el número de genes transportados por estos grandes fagos es notablemente mayor que el de los fagos ordinarios, tienen una mayor capacidad para moverse alrededor de genes que pueden dañar otras células. Sucesivamente, esto aumenta el riesgo de que algunos de estos genes sean adquiridos por genes en el entorno humano.
En total, los investigadores están fascinados por la presencia de fagos con genomas enormes en una variedad de microbiomas en la tierra. La relación entre estos grandes fagos se interpreta en el sentido de que provienen de una antigua familia de virus de genoma grande.
Dice Banfield, "Tener genomas grandes es una estrategia exitosa para la existencia. Estos virus de bacterias son parte de la biología, de entidades replicantes, de la que sabemos muy poco ".
Suficientemente cierto. Estos fagos son de un tamaño que los hace encajar en algún lugar del espacio entre las arqueas (los primeros parientes de las bacterias), y fagos ordinarios que parecen seres no vivos. Banfield los describe como "estrategias exitosas de existencia que son híbridos entre lo que consideramos virus tradicionales y organismos vivos tradicionales".
 Los productos de limpieza pueden aumentar el riesgo de asma infantil, según un estudio
Los productos de limpieza pueden aumentar el riesgo de asma infantil, según un estudio
 La investigación dice que en la infección canina SARS-CoV-2,
La investigación dice que en la infección canina SARS-CoV-2,
 DeNovix anuncia el ganador del espectrofotómetro / fluorómetro Platinum DS11 FX +
DeNovix anuncia el ganador del espectrofotómetro / fluorómetro Platinum DS11 FX +
 La respiración de hidrógeno no es del atolón Bikini
La respiración de hidrógeno no es del atolón Bikini
 Bacterias intestinales vinculadas a músculos más fuertes en personas mayores
Bacterias intestinales vinculadas a músculos más fuertes en personas mayores
 Los científicos convierten la sangre tipo A en tipo O universal,
Los científicos convierten la sangre tipo A en tipo O universal,
 Humanos versus virus:¿podemos evitar la extinción en un futuro próximo?
El experto sostiene que los cambios causados por el hombre en el medio ambiente pueden conducir a la aparición de patógenos, no solo desde el exterior sino también desde nuestro propio microbioma, q
Humanos versus virus:¿podemos evitar la extinción en un futuro próximo?
El experto sostiene que los cambios causados por el hombre en el medio ambiente pueden conducir a la aparición de patógenos, no solo desde el exterior sino también desde nuestro propio microbioma, q
 Pruebas utilizadas para el diagnóstico de ERGE
En algunos pacientes, podemos sospechar enfermedad por reflujo gastroesofágico, pero los síntomas del paciente pueden ser atípicos. O puede que simplemente necesitemos confirmar nuestro diagnóstico. P
Pruebas utilizadas para el diagnóstico de ERGE
En algunos pacientes, podemos sospechar enfermedad por reflujo gastroesofágico, pero los síntomas del paciente pueden ser atípicos. O puede que simplemente necesitemos confirmar nuestro diagnóstico. P
 Diagnóstico de infecciones virales mediante tecnologías a micro y nanoescala
La necesidad de que toda la población rápido, sensible, y las pruebas de diagnóstico rentables han aumentado significativamente como resultado del síndrome respiratorio agudo severo coronavirus 2 (SAR
Diagnóstico de infecciones virales mediante tecnologías a micro y nanoescala
La necesidad de que toda la población rápido, sensible, y las pruebas de diagnóstico rentables han aumentado significativamente como resultado del síndrome respiratorio agudo severo coronavirus 2 (SAR