 Ny Coronavirus SARS-CoV-2 Färgad skanningselektronmikrograf av en apoptotisk cell (grön) kraftigt infekterad med SARS-COV-2-viruspartiklar (orange), isolerat från ett patientprov. Bild på NIAID Integrated Research Facility (IRF) i Fort Detrick, Maryland. Upphovsman:NIAID
Ny Coronavirus SARS-CoV-2 Färgad skanningselektronmikrograf av en apoptotisk cell (grön) kraftigt infekterad med SARS-COV-2-viruspartiklar (orange), isolerat från ett patientprov. Bild på NIAID Integrated Research Facility (IRF) i Fort Detrick, Maryland. Upphovsman:NIAID SARS-CoV-2, en orsakande orsak till den disruptiva coronavirus-pandemin (COVID-19), ses främst som en respiratorisk patogen; dock, bevisen tyder på att viruset oberoende kan replikera i tarmen, öka sannolikheten för fekal-oral överföring.
Detta kan verkligen vara en viktig fråga vid fekal mikrobiotatransplantation, vilket är processen att överföra avföringen från en frisk givare till en patients tarm för att återställa tarmmikrobiomet. För närvarande, detta tillvägagångssätt rekommenderas för frekventa sjukhusförvärvade infektioner med Clostridioides difficile och utforskas för närvarande som ett experimentellt tillvägagångssätt för många andra förhållanden.
Dock, trots konsensus om att fetala mikrobiotagivare ska screenas för SARS-CoV-2, den optimala strategin för att upptäcka asymptomatisk transport bland givare är fortfarande svårfånglig, medan kombinationen av tester ännu inte har bedömts eller jämförts.
Därav, forskarna från OpenBiome (dvs. en ideell organisation i Massachusetts, som driver en offentlig pallbank och stöder human mikrobiomutvecklad forskning) utvecklat en matematisk modell av SARS-CoV-2-infektion bland fekaltransplantatgivare som simulerar effekten av olika teststrategier.
Kortfattat, dessa forskare byggde en abstrakt modell av donatorer av fekal mikrobiotatransplantation, simulera sitt donationsschema, infektionsförekomsten med SARS-CoV-2, samt kursen COVID-19.
Olika screeningstrategier lagrades ovanpå dessa simuleringar-med hänsyn till suboptimal känslighet och specificitet för varje test-för att uppskatta hur många virusnegativa och viruspositiva donationer som skulle lämnas på lämpligt eller oönskat sätt, respektive.
Följaktligen, den utformade modellen presenterade två resultat:antalet "sanna negativa, "virusnegativa donationer släpptes, och antalet "falskt negativt, "viruspositiva donationer släpps.
Följaktligen, en önskvärd screeningmetod skulle frigöra många virusnegativa donationer och endast en handfull eller inga viruspositiva donationer; å andra sidan, en dålig strategi skulle i onödan förstöra ett brett spektrum av virusnegativa donationer eller släppa en uppsjö av viruspositiva donationer.
"Modellen kvantifierar effekten av strängare tester på den önskvärda minskningen av potentiellt infektiösa, viruspositiva donationer bearbetade till fekalt mikrobiotatransplantationsmaterial och släpps ut för användning, liksom den oönskade minskningen av virus-negativa donationer som släpps ", studieförfattare sammanfattar deras metodiska tillvägagångssätt.
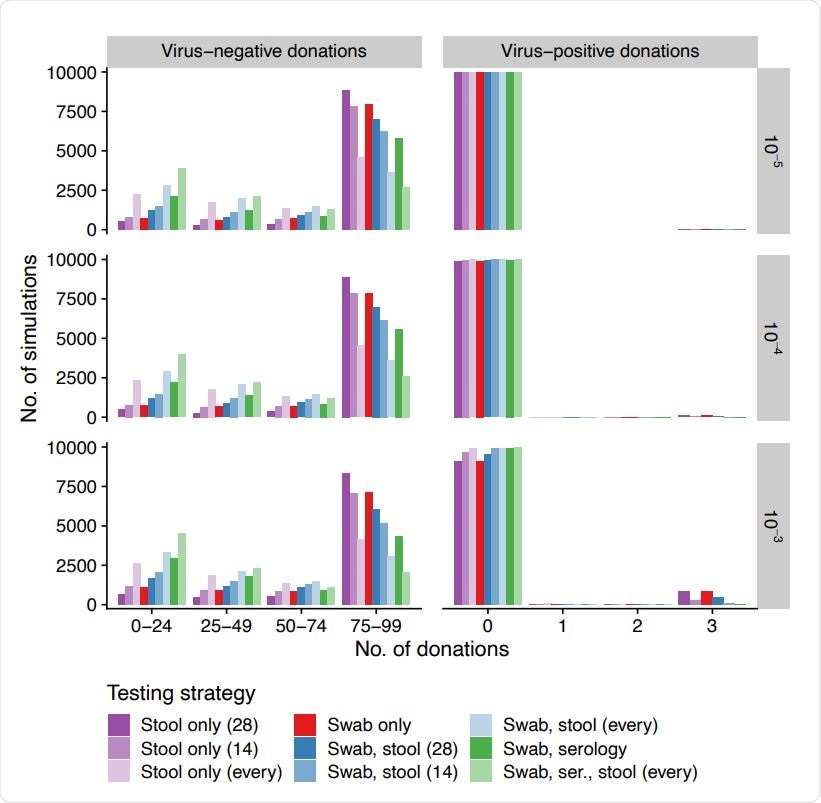 Antal virus -negativa och -positiva donationer som släppts (kolumner, x-axel) över simuleringar (y-axel) för olika dagliga incidenter (rader, infektioner per person och dag) vid användning av olika teststrategier (färger). Pinnar är alltid med 14-dagars intervall och serologi är alltid med 60-dagars intervall. Avföringstester utförs med 14-dagars intervall, 28-dagars intervaller, eller för varje donation.
Antal virus -negativa och -positiva donationer som släppts (kolumner, x-axel) över simuleringar (y-axel) för olika dagliga incidenter (rader, infektioner per person och dag) vid användning av olika teststrategier (färger). Pinnar är alltid med 14-dagars intervall och serologi är alltid med 60-dagars intervall. Avföringstester utförs med 14-dagars intervall, 28-dagars intervaller, eller för varje donation. Antalet viruspositiva och virusnegativa donationer som släpptes skilde sig från simuleringar och var beroende av teststrategi och infektionsincidens. Kortfattat, de mest känsliga strategierna var också de minst specifika.
"I allmänhet, de mer känsliga strategierna släppte färre viruspositiva donationer men tog också bort givare tidigt på grund av falska positiva och släppte därför färre virusnegativa donationer per donator, "ytterligare förtydligade studieförfattare.
Dessutom, riskskillnaden för frigjort viruspositivt material när de mest och minst strängaste strategierna jämfördes motsvarade effekten av en 100-faldig förändring av daglig SARS-CoV-2-incidens.
När känslighetsanalys genomfördes, parametrarna som var starkt förknippade med de två resultaten som nämns ovan var donationsintervall (dvs. längre intervall gav färre virusnegativa donationer), egenskaperna hos de tre testerna (dvs. mer virusnegativa donationer som frigörs med användning av specifika test), och SARS-CoV-2-incidens (dvs. högre förekomst korrelerade med fler viruspositiva donationer som släpptes).
Styrkan i denna analys ligger i dess kvantitativa behandling av en brinnande klinisk fråga. Fortfarande, alla kvantitativa förutsägelser från modellen bör ses som riktlinjer för kliniska resonemang snarare än tydliga och entydiga prognoser.
Vidare, att verifiera denna modell kan visa sig vara ganska utmanande, eftersom möjligheten till SARS-CoV-2 fekal-oral överföring inte har bekräftats, och det finns ingen "guldstandard" för att detektera detta virala medel i avföringsprover. Också, många antaganden i modellen kanske inte längre är tillämpliga.
"Även om dessa resultat är uppmuntrande, vi varnar återigen för att de är beroende av ett antal antaganden om kvalitetskontroll och SARS-CoV-2-epidemiologi som kommer att förfinas under de kommande månaderna ", säger studieförfattare.
Ändå, metoden är verkligen värdefull för att bedöma överföringsriskerna i denna pågående pandemi. Förutom, detta tillvägagångssätt kan användas som en mall för att utvärdera teststrategier för andra patogena mikroorganismer eller behandlingar som härrör från människor bortom fekal mikrobiotatransplantation.
bioRxiv publicerar preliminära vetenskapliga rapporter som inte är fackgranskade och, därför, ska inte betraktas som avgörande, vägleda klinisk praxis/hälsorelaterat beteende, eller behandlas som etablerad information.
 Forskare hoppas att blodprov som exakt diagnostiserar fibromyalgi kan vara tillgängligt inom fem år
Forskare hoppas att blodprov som exakt diagnostiserar fibromyalgi kan vara tillgängligt inom fem år
 Kronisk hosta kan lindras med nytt läkemedel
Kronisk hosta kan lindras med nytt läkemedel
 Mikrobiotmodulering och återupprättande av eubios kan hjälpa till att begränsa COVID-19-komplikationer
Mikrobiotmodulering och återupprättande av eubios kan hjälpa till att begränsa COVID-19-komplikationer
 Genetik kan påverka sammansättningen av mikrobiomet mer än miljöfaktorer
Genetik kan påverka sammansättningen av mikrobiomet mer än miljöfaktorer
 Goda nyheter för IBS -drabbade när forskare identifierar "tarmklåda"
Goda nyheter för IBS -drabbade när forskare identifierar "tarmklåda"
 Matsmältningsmanifestationer vanliga men milda bland sjukhusvistade covid-19-patienter
Matsmältningsmanifestationer vanliga men milda bland sjukhusvistade covid-19-patienter
 Forskare utvinner fullständigt mänskligt genom från ett tusentals år gammalt "tuggummi"
Det verkar som att tuggummi inte är en ny trend! Forskare har hittat tuggummi som är 5, 700 år gammal och den har gett ledtrådar angående forntida DNA. En studie med resultaten publicerades i tidskrif
Forskare utvinner fullständigt mänskligt genom från ett tusentals år gammalt "tuggummi"
Det verkar som att tuggummi inte är en ny trend! Forskare har hittat tuggummi som är 5, 700 år gammal och den har gett ledtrådar angående forntida DNA. En studie med resultaten publicerades i tidskrif
 Nyfödd musmodell ger ledtrådar till orsaken till förödande tarmsjukdom i anemiska preemier
Läkare har länge misstänkt att transfusioner av röda blodkroppar som ges till för tidigt födda barn med anemi kan sätta dem i fara för att utveckla nekrotiserande enterokolit, eller NEC, en potentiell
Nyfödd musmodell ger ledtrådar till orsaken till förödande tarmsjukdom i anemiska preemier
Läkare har länge misstänkt att transfusioner av röda blodkroppar som ges till för tidigt födda barn med anemi kan sätta dem i fara för att utveckla nekrotiserande enterokolit, eller NEC, en potentiell
 Genetik kan påverka sammansättningen av mikrobiomet mer än miljöfaktorer
Forskare som studerar möss vid Technion-Israel Institute of Technology har funnit att mikrobiomet påverkas av genetik mycket mer än det är av moderns födelsemiljö. Kateryna Kon | Shuttersto
Genetik kan påverka sammansättningen av mikrobiomet mer än miljöfaktorer
Forskare som studerar möss vid Technion-Israel Institute of Technology har funnit att mikrobiomet påverkas av genetik mycket mer än det är av moderns födelsemiljö. Kateryna Kon | Shuttersto