Ezek a mikrobiológiai különbségek segíthetnek megmagyarázni, hogy az idősebb emberek és férfiak miért hajlamosabbak a koronavírus-betegség 19 (COVID-19) kialakulására, összehasonlítva a fiatalabb személyekkel és nőkkel, - mondja a csapat.
Rob Knight (Kaliforniai Egyetem, San Diego) és kollégái szerint a tanulmány bizonyítékokat szolgáltat arra, hogy az emberi mikrobiom közvetíti a SARS-CoV-2 fertőzőképességét azáltal, hogy módosítja a glikozikalyx nevű, a gazda plazmamembránját körülvevő vastag réteget.
A kutatók azt sugallják, hogy a gazdaszervezet-mikrobiális közösségek összetételében bekövetkező változások megértése segíthet a betegek kockázati rétegzettségének javításában, valamint a megelőzés és a kezelés lehetséges megközelítéseiben.
A cikk nyomtatott verziója elérhető a kiszolgálón bioRxiv* , míg a cikk szakértői értékelésen megy keresztül.
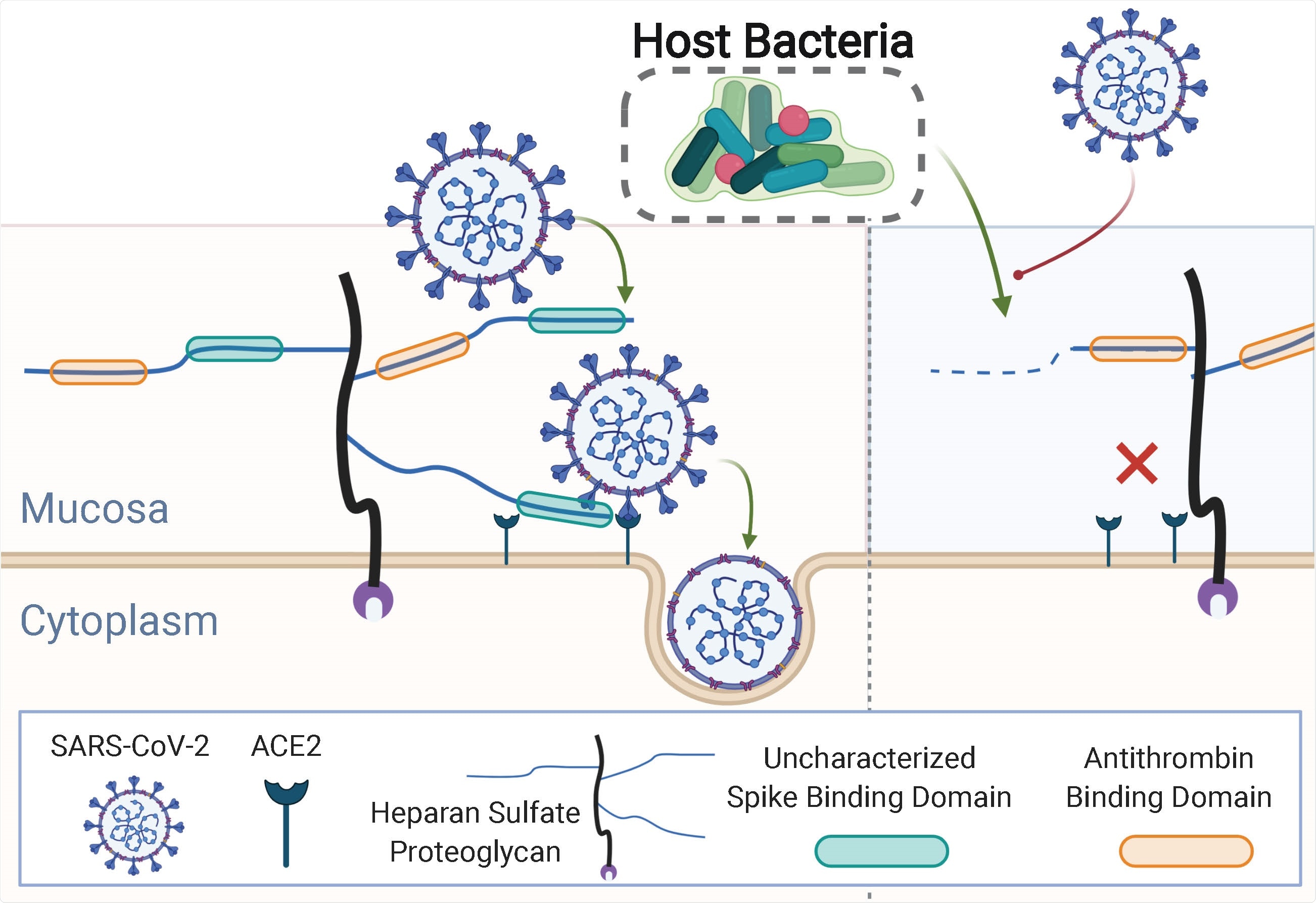
A glikokalix gazdag glikán- és glikokonjugátum -hálózatból épül fel, amelyhez számos vírus kórokozó kötődik, hogy átjusson a védő glikokalixrétegen, és a gazdasejt plazmamembránján lévő fehérje receptorokhoz kapcsolódjon.
SARS-CoV-2 esetén, egy „tüske” nevű vírusos felszíni fehérje a heparán -szulfát (HS) nevű glikozaminoglikánt (GAG) célozza meg. A vírus megkötéséhez a HS-hez kell kötődnie ahhoz, hogy megköthesse a gazdasejt felszíni receptorának angiotenzin-konvertáló enzimet 2 (ACE2), amely lehetővé teszi a vírusmembrán tapadását és a gazdasejt bejutását.
„A SARS-CoV-2 tüskefehérje és a gazdasejt HS közötti kölcsönhatás csökkentése, ezért, vonzó megközelítés a vírus dokkolás és az azt követő fertőzés csökkentésére, ”Írja Knight és csapata.
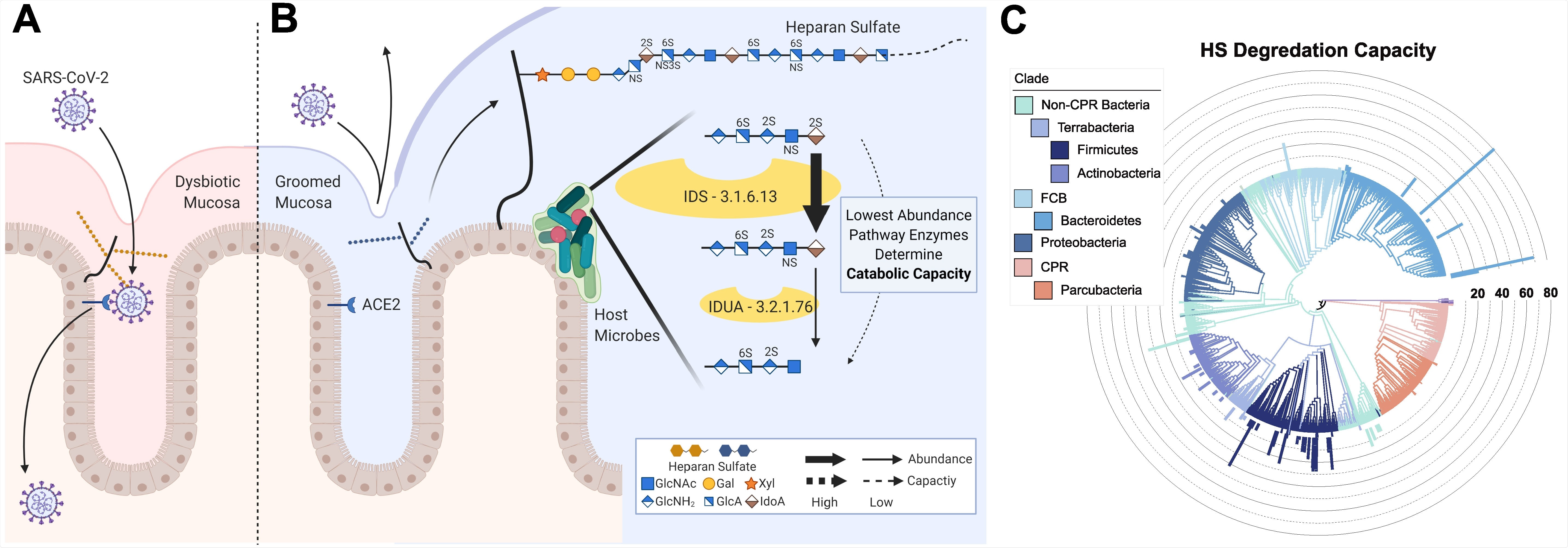
Számos bakteriális taxon ismert enzimeket termel, amelyek módosítják a GAG bizonyos típusait, beleértve a HS -t, és sok kutatást végeztek a GAG -ok tisztított bakteriális enzimek alkalmazásával.
Most, Knight és munkatársai kifejlesztettek egy számítási modellt a HS katabolizmusára, hogy felmérjék az emberi mikrobák HS -lebontó képességét.
A csapat megállapította, hogy a közönséges emberrel kapcsolatos kommenális baktériumok genomjai kódolják a HS-t lebontó enzimeket.
Ezen HS-módosító baktériumok jelenléte alacsonyabb volt a COVID-19-es betegektől vett bronchoalveolaris lavage fluid (BALF) mintákban, mint az egészséges kontrollokból vett mintákban.
A kutatók azt is megállapították, hogy két független bél mikrobiom adatkészletben, A HS-módosító baktériumok szintje az életkor előrehaladtával csökkent, a nőkben pedig a férfiakhoz képest.
Az idősebb kor és a férfi nem egyaránt ismert módosíthatatlan kockázati tényezők a COVID-19 kialakulásához a SARS-CoV-2 fertőzést követően, és ez a megállapítás segíthet megmagyarázni ezt a fokozott érzékenységet, - mondja a csapat.
 BALF RNS-seq adatok összehasonlítása a vizsgálatok között. RNS-seq vizsgálatok (x-tengelyek) összehasonlítva az előre jelzett HS-módosító fajok log-arányával (y-tengely) a nem-HSmodifikáló (A) -hoz viszonyítva, HSase a háztartási készlethez képest (B), és N-acetil-glükózamin-6-O-szulfatáz a (C) háztartási készlethez képest.
BALF RNS-seq adatok összehasonlítása a vizsgálatok között. RNS-seq vizsgálatok (x-tengelyek) összehasonlítva az előre jelzett HS-módosító fajok log-arányával (y-tengely) a nem-HSmodifikáló (A) -hoz viszonyítva, HSase a háztartási készlethez képest (B), és N-acetil-glükózamin-6-O-szulfatáz a (C) háztartási készlethez képest. Végül, a csapat kimutatta, hogy a HS-módosító kommenálisok képesek voltak megakadályozni a SARS-CoV-2 tüskefehérje gazdasejtekhez való kötődését.
„Bizonyítékokat szolgáltatunk az emberi mikrobiomnak a SARS-CoV-2 fertőzőképesség közvetítésében betöltött szerepére, a gazdaszervezet glikokalix módosításával, ” - írja Knight és munkatársai. „Az emberi mikrobiális közösségekben a HS-módosító baktériumok szabályozhatják a vírusok tapadását, és ezeknek a kommenálisoknak a elvesztése hajlamossá teheti az egyéneket a fertőzésre. ”
Bár a pontos védőmechanizmus még nem ismert, a Bacteroide törzsek Bacteroides ovatus és Bacteroides thetaiotaomicron , amelyek nagyon gyakoriak az emberi bélbaktériumokban, korábban kimutatták, hogy katalizálják a HS -t, - mondják a kutatók.
Valóban, a csapat ezt megmutatta in vitro a H1299 humán tüdősejtek kezelése B. ovatus és B. thetaiotaomicron katabolizált sejtfelszíni HS és 20-30-szorosára csökkentette a SARS-CoV-2 fehérjekötődést, összehasonlítva a kezeletlen H1299 sejtekkel.
 A heparán -szulfát (HS) -lizázt (HSase) kódoló baktériumfajok kimerültek a COVID -betegekben a kontrollokhoz képest. BALF RNS-seq adatok egészséges alanyokból (kontroll) és COVID-19 betegekből (COVID) (x-tengelyek) összehasonlítva az előrejelzett HS-módosító fajok log-arányával (y-tengelye) a nem-HS-módosító (A) -hoz viszonyítva, HSase a háztartási készlethez képest (B), és N-acetil-glükózamin-6-O-szulfatáz a (C) háztartási készlethez képest. A szignifikanciát t-teszttel értékeltük, és a hibasávok az átlag standard hibáját jelentik. A bemutatott p-értékek párosítatlan kétirányú t-tesztből származnak.
A heparán -szulfát (HS) -lizázt (HSase) kódoló baktériumfajok kimerültek a COVID -betegekben a kontrollokhoz képest. BALF RNS-seq adatok egészséges alanyokból (kontroll) és COVID-19 betegekből (COVID) (x-tengelyek) összehasonlítva az előrejelzett HS-módosító fajok log-arányával (y-tengelye) a nem-HS-módosító (A) -hoz viszonyítva, HSase a háztartási készlethez képest (B), és N-acetil-glükózamin-6-O-szulfatáz a (C) háztartási készlethez képest. A szignifikanciát t-teszttel értékeltük, és a hibasávok az átlag standard hibáját jelentik. A bemutatott p-értékek párosítatlan kétirányú t-tesztből származnak. „Ez a jelentés bizonyítékokat szolgáltat a glikokalix-mikrobiota kölcsönhatások szerepére, mint új versenyképes mechanizmusra a SARS-CoV-2 elleni küzdelemben, ” - írják a kutatók.
Azt mondják, hogy további munkára van szükség az eredmények transzlációs következményeinek tisztázásához, mivel továbbra sem világos, hogy mely mikrobiális enzimek bontják le a GAG-kat, hogy megakadályozzák a SARS-CoV-2 kötődését. Az sem világos, hogy ezek az enzimek felhasználhatók -e a vírus terjedésének korlátozására aktív fertőzés során.
Mindazonáltal, „Az itt bemutatott elemzések egy kulcsfontosságú mechanizmust írnak le, amellyel a gazdaszervezet mikrobiómái szerepet játszhatnak a SARS-CoV-2 fertőzésben, magyarázatot adhat a korcsoportok közötti egészségügyi különbségekre a COVID-19 betegségben, és rávilágít annak fontosságára, hogy jellemezni kell az emberek és vírusok közötti potenciális jövőbeli molekuláris fegyverkezési versenyt, ” - mondják a kutatók.
„A gazda-mikrobák és a vírusfertőzés közötti hatalmas kölcsönhatás feltárása lehetővé teheti a kockázatok jobb rétegződését, megelőzés, és a beavatkozás, ” - fejezik be.
bioRxiv előzetes tudományos jelentéseket tesz közzé, amelyeket nem vizsgálnak felül, és ezért, nem tekinthető döntőnek, irányítja a klinikai gyakorlatot/az egészséggel kapcsolatos viselkedést, vagy megállapított információként kezelik.
 A bél mikrobiota megjósolhatja a COVID-19 súlyosságát
A bél mikrobiota megjósolhatja a COVID-19 súlyosságát
 Az OTC antacidok savsemlegesítő képességének meghatározása
Az OTC antacidok savsemlegesítő képességének meghatározása
 A hüvelyi mikrobiom befolyásolhatja a HIV megelőző terápia hatékonyságát
A hüvelyi mikrobiom befolyásolhatja a HIV megelőző terápia hatékonyságát
 Kevés bizonyíték az mRNS COVID-19 vakcinával összefüggő thrombocytopeniára,
Kevés bizonyíték az mRNS COVID-19 vakcinával összefüggő thrombocytopeniára,
 Keskeny nyelőcső megnyitása
Keskeny nyelőcső megnyitása
 A kutatók fágterápiát alkalmaznak az alkoholos májbetegség sikeres kezelésére
A kutatók fágterápiát alkalmaznak az alkoholos májbetegség sikeres kezelésére
 Hogyan lehet erősíteni az immunrendszert a koronavírus elleni küzdelemben
Miközben a világ küzd a koronavírus -járvánnyal, egyre többen próbálnak minden eszközzel védekezni a vírus ellen. Jelenleg nincs vakcina a súlyos akut légzőszervi szindróma 2 koronavírus (SARS-CoV-2)
Hogyan lehet erősíteni az immunrendszert a koronavírus elleni küzdelemben
Miközben a világ küzd a koronavírus -járvánnyal, egyre többen próbálnak minden eszközzel védekezni a vírus ellen. Jelenleg nincs vakcina a súlyos akut légzőszervi szindróma 2 koronavírus (SARS-CoV-2)
 Neil Bell -t nevezték ki az Avacta Life Sciences fejlesztési igazgatójává
Avacta Group plc, az Affimer fejlesztője ® bioterápiás szerek és reagensek, örömmel jelenti be Neil Bell kinevezését az Avacta Life Sciences fejlesztési igazgatójává, azonnali hatállyal. Neil lesz f
Neil Bell -t nevezték ki az Avacta Life Sciences fejlesztési igazgatójává
Avacta Group plc, az Affimer fejlesztője ® bioterápiás szerek és reagensek, örömmel jelenti be Neil Bell kinevezését az Avacta Life Sciences fejlesztési igazgatójává, azonnali hatállyal. Neil lesz f
 A szívrohamhoz kapcsolódó mikrobák tanulmányt találnak
A múlt hétvégén Párizsban megrendezett 2019 -es ESC kongresszuson kiderült, hogy a szervezet kóros mikrobapopulációja a stabil koszorúér -plakkok károsodásához vezethet, és szívrohamhoz vezethet. Az a
A szívrohamhoz kapcsolódó mikrobák tanulmányt találnak
A múlt hétvégén Párizsban megrendezett 2019 -es ESC kongresszuson kiderült, hogy a szervezet kóros mikrobapopulációja a stabil koszorúér -plakkok károsodásához vezethet, és szívrohamhoz vezethet. Az a