Ces différences de microbiome peuvent aider à expliquer pourquoi les personnes âgées et les hommes sont plus susceptibles de développer la maladie à coronavirus 19 (COVID-19), par rapport aux personnes plus jeunes et aux femmes, dit l'équipe.
Rob Knight (Université de Californie, San Diego) et ses collègues affirment que l'étude fournit des preuves que le microbiome humain médie l'infectiosité du SRAS-CoV-2 en modifiant une couche épaisse entourant la membrane plasmique de l'hôte appelée glycocalyx.
Les chercheurs suggèrent que la compréhension des changements dans la composition des communautés hôtes-microbiennes pourrait aider à améliorer la stratification des risques des patients et les approches potentielles de prévention et de traitement.
Une version pré-imprimée de l'article est disponible sur le serveur bioRxiv* , tandis que l'article est soumis à un examen par les pairs.
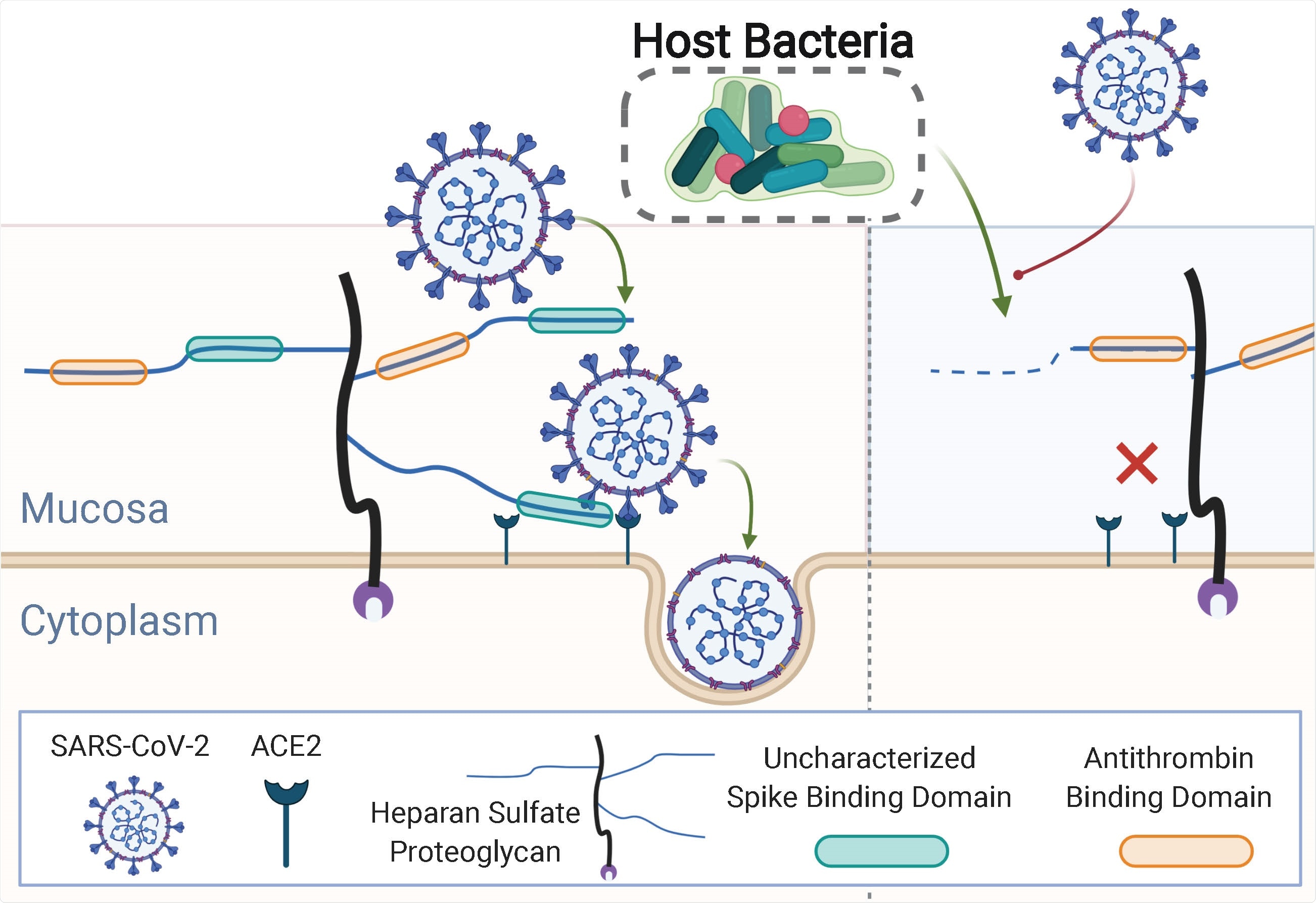
Le glycocalyx est constitué d'un riche réseau de glycanes et de glycoconjugués auxquels de nombreux agents pathogènes viraux se lient pour traverser la couche protectrice de glycocalyx et se fixer aux récepteurs protéiques de la membrane plasmique de la cellule hôte.
Dans le cas du SRAS-CoV-2, une protéine de surface virale appelée « pic » cible un glycosaminoglycane (GAG) appelé héparane sulfate (HS). Le virus doit être attaché à HS afin de se lier au récepteur de surface de la cellule hôte, l'enzyme de conversion de l'angiotensine 2 (ACE2), qui permet l'adhésion à la membrane virale et l'entrée de la cellule hôte.
« Réduire l'interaction entre la protéine de pointe SARS-CoV-2 et la cellule hôte HS est, donc, une approche attrayante pour réduire l'amarrage viral et l'infection ultérieure, ” écrivent Knight et son équipe.
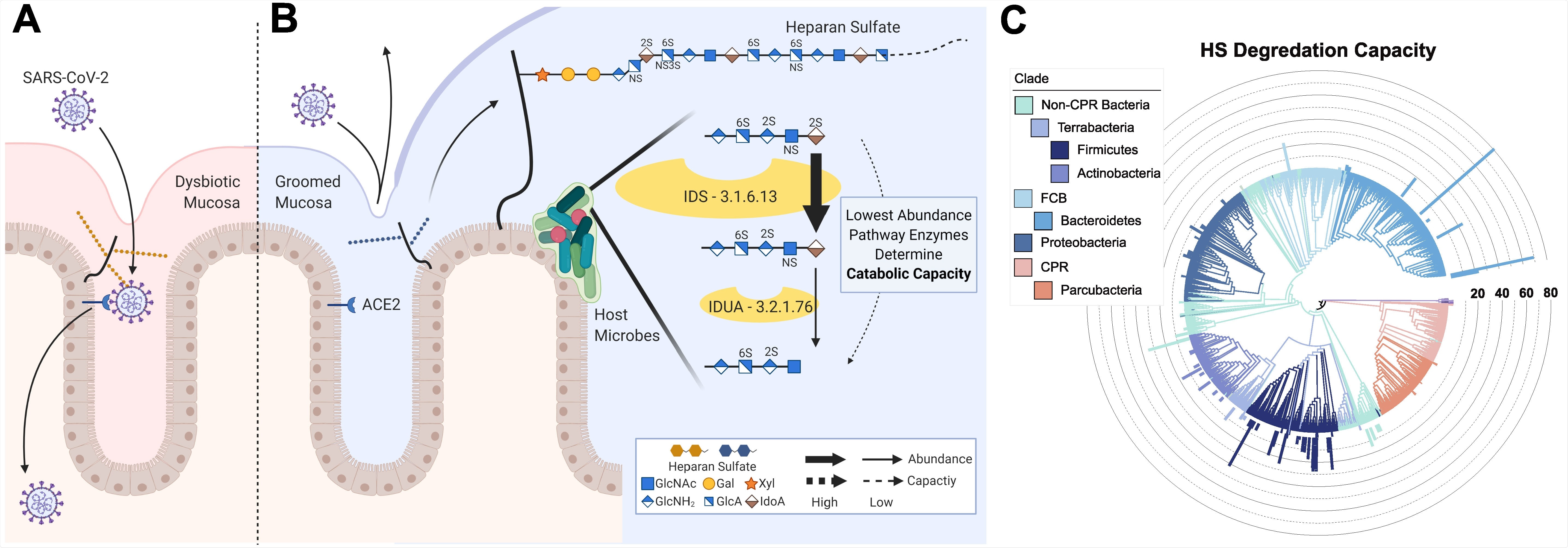
Plusieurs taxons bactériens sont connus pour produire des enzymes qui modifient certains types de GAG, y compris SH, et de nombreuses recherches sur les GAG ont été avancées en utilisant des enzymes bactériennes purifiées.
Maintenant, Knight et ses collègues ont développé un modèle informatique du catabolisme de l'HS pour évaluer la capacité des microbes humains à dégrader l'HS.
L'équipe a découvert que les génomes des bactéries commensales communes associées à l'homme codent pour des enzymes qui dégradent l'HS.
La présence de ces bactéries modifiant le HS était plus faible dans les échantillons de liquide de lavage bronchoalvéolaire (BALF) prélevés sur des patients atteints de COVID-19 que parmi les échantillons prélevés sur des témoins sains.
Les chercheurs ont également découvert que dans deux ensembles de données indépendants sur le microbiome intestinal, les niveaux de bactéries modificatrices de HS diminuaient avec l'âge et augmentaient chez les femmes par rapport aux hommes.
L'âge plus avancé et le sexe masculin sont tous deux des facteurs de risque non modifiables connus pour le développement de COVID-19 suite à une infection par le SRAS-CoV-2, et ce résultat peut aider à expliquer cette susceptibilité accrue, dit l'équipe.
 Données BALF RNA-seq comparées entre les études. Études d'ARN-seq (axes des abscisses) comparées par les rapports logarithmiques (axes des ordonnées) des espèces prédites modifiant l'HS par rapport aux non modifiant l'HS (A), HSase relative à l'ensemble de ménage (B), et N-acétylglucosamine-6-O-sulfatase par rapport à l'ensemble de ménage (C).
Données BALF RNA-seq comparées entre les études. Études d'ARN-seq (axes des abscisses) comparées par les rapports logarithmiques (axes des ordonnées) des espèces prédites modifiant l'HS par rapport aux non modifiant l'HS (A), HSase relative à l'ensemble de ménage (B), et N-acétylglucosamine-6-O-sulfatase par rapport à l'ensemble de ménage (C). Finalement, l'équipe a montré que les commensaux modifiant le HS étaient capables d'empêcher la liaison de la protéine de pointe SARS-CoV-2 aux cellules hôtes.
"Nous fournissons des preuves d'un rôle du microbiome humain dans la médiation de l'infectivité du SRAS-CoV-2 via la modification du glycocalyx de l'hôte, », écrit Knight et ses collègues. « Les bactéries modifiant l'HS dans les communautés microbiennes humaines peuvent réguler l'adhésion virale, et la perte de ces commensaux pourrait prédisposer les individus à l'infection.
Bien que le mécanisme de protection sous-jacent précis ne soit pas encore connu, les souches Bacteroide Bacteroides ovatus et Bacteroides thetaiotaomicron , qui sont très répandus dans les bactéries intestinales humaines, ont déjà été montrés connus pour cataboliser l'HS, disent les chercheurs.
En effet, l'équipe a ensuite montré que in vitro traitement des cellules pulmonaires humaines H1299 avec B. ovatus et B. thetaiotaomicron a catabolisé l'HS à la surface des cellules et réduit de 20 à 30 fois la liaison aux protéines du SRAS-CoV-2, par rapport aux cellules H1299 non traitées.
 Les espèces de bactéries codant pour l'héparane sulfate (HS) lyase (HSase) sont épuisées chez les patients COVID par rapport aux témoins. Données BALF RNA-seq de sujets sains (contrôle) et de patients COVID-19 (COVID) (axes x) comparées par les rapports logarithmiques (axes y) des espèces prédites modifiant l'HS par rapport aux non modifiant l'HS (A), HSase relative à l'ensemble de ménage (B), et N-acétylglucosamine-6-O-sulfatase par rapport à l'ensemble de ménage (C). La signification a été évaluée par un test t et les barres d'erreur représentent l'erreur standard de la moyenne. Les valeurs p présentées proviennent du test t bilatéral non apparié.
Les espèces de bactéries codant pour l'héparane sulfate (HS) lyase (HSase) sont épuisées chez les patients COVID par rapport aux témoins. Données BALF RNA-seq de sujets sains (contrôle) et de patients COVID-19 (COVID) (axes x) comparées par les rapports logarithmiques (axes y) des espèces prédites modifiant l'HS par rapport aux non modifiant l'HS (A), HSase relative à l'ensemble de ménage (B), et N-acétylglucosamine-6-O-sulfatase par rapport à l'ensemble de ménage (C). La signification a été évaluée par un test t et les barres d'erreur représentent l'erreur standard de la moyenne. Les valeurs p présentées proviennent du test t bilatéral non apparié. « Ce rapport fournit des preuves du rôle des interactions glycocalyx-microbiote en tant que nouveau mécanisme compétitif dans la lutte contre le SRAS-CoV-2, », écrivent les chercheurs.
Ils disent que des travaux supplémentaires sont nécessaires pour clarifier les implications traductionnelles des résultats, car il reste difficile de savoir quelles enzymes microbiennes particulières dégradent les GAG pour empêcher la liaison du SRAS-CoV-2. Il n'est pas clair non plus si ces enzymes pourraient être utilisées pour limiter la propagation virale lors d'une infection active.
Néanmoins, « les analyses présentées ici décrivent un mécanisme clé par lequel les microbiomes de l'hôte pourraient jouer un rôle dans l'infection par le SRAS-CoV-2, fournir une explication potentielle des disparités de santé entre les groupes d'âge dans la maladie COVID-19 et souligner l'importance de caractériser la future course aux armements moléculaires potentielle entre les humains et les virus, », disent les chercheurs.
« L'exploration de la vaste interaction entre l'hôte-microbes et l'infection virale pourrait permettre une meilleure stratification des risques, la prévention, et intervention, », concluent-ils.
bioRxiv publie des rapports scientifiques préliminaires qui ne sont pas évalués par des pairs et, donc, ne doit pas être considéré comme concluant, guider la pratique clinique/le comportement lié à la santé, ou traités comme des informations établies.
 La migration affecte le microbiote intestinal qui à son tour affecte la santé
La migration affecte le microbiote intestinal qui à son tour affecte la santé
 Bonne nouvelle pour les personnes souffrant du SII alors que les chercheurs identifient une « démangeaison intestinale »
Bonne nouvelle pour les personnes souffrant du SII alors que les chercheurs identifient une « démangeaison intestinale »
 Le microbiome intestinal change avec la cuisson des aliments végétaux,
Le microbiome intestinal change avec la cuisson des aliments végétaux,
 La composition et la structure du microbiome nasopharyngé sont liées à la gravité de la maladie COVID-19
La composition et la structure du microbiome nasopharyngé sont liées à la gravité de la maladie COVID-19
 Des scientifiques développent une pilule imprimée en 3D qui échantillonne les bactéries trouvées dans l'intestin
Des scientifiques développent une pilule imprimée en 3D qui échantillonne les bactéries trouvées dans l'intestin
 Un régime à base de plantes pourrait guérir votre polyarthrite rhumatoïde
Un régime à base de plantes pourrait guérir votre polyarthrite rhumatoïde
 Des chercheurs découvrent un nouveau moyen de se protéger contre la maladie dans un modèle de SEP
Des chercheurs du Brigham and Womens Hospital ont trouvé un moyen nouveau et inattendu de prévenir la maladie dans un modèle préclinique de sclérose en plaques (SEP). Crédit dimage :Lightsp
Des chercheurs découvrent un nouveau moyen de se protéger contre la maladie dans un modèle de SEP
Des chercheurs du Brigham and Womens Hospital ont trouvé un moyen nouveau et inattendu de prévenir la maladie dans un modèle préclinique de sclérose en plaques (SEP). Crédit dimage :Lightsp
 Cryptosporidiose aggravée par les probiotiques couramment utilisés
Les chercheurs ont découvert que linfection par le parasite intestinal Cryptosporidium parvum est aggravée chez les souris qui ont reçu un probiotique. Crédit dimage :Alpha Tauri 3D Grap
Cryptosporidiose aggravée par les probiotiques couramment utilisés
Les chercheurs ont découvert que linfection par le parasite intestinal Cryptosporidium parvum est aggravée chez les souris qui ont reçu un probiotique. Crédit dimage :Alpha Tauri 3D Grap
 La supplémentation en acides gras à chaîne courte améliore la récupération de l'AVC,
une étude sur des souris montre La supplémentation en acides gras à chaîne courte du corps peut améliorer la récupération après un AVC, selon des recherches sur des souris récemment publiées dans JNeu
La supplémentation en acides gras à chaîne courte améliore la récupération de l'AVC,
une étude sur des souris montre La supplémentation en acides gras à chaîne courte du corps peut améliorer la récupération après un AVC, selon des recherches sur des souris récemment publiées dans JNeu