Теперь, группа ученых разработала новый метод быстрого и полномасштабного анализа всех типов бактерий в кишечнике, а также список видов, обнаруженных в здоровом кишечнике человека, по типу и количеству (GutFeelingKB), и новый шаблон отчета под названием «Отчет о популяции фекального биома» (FecalBiome), который упростит понимание того, что именно происходит в кишечнике.
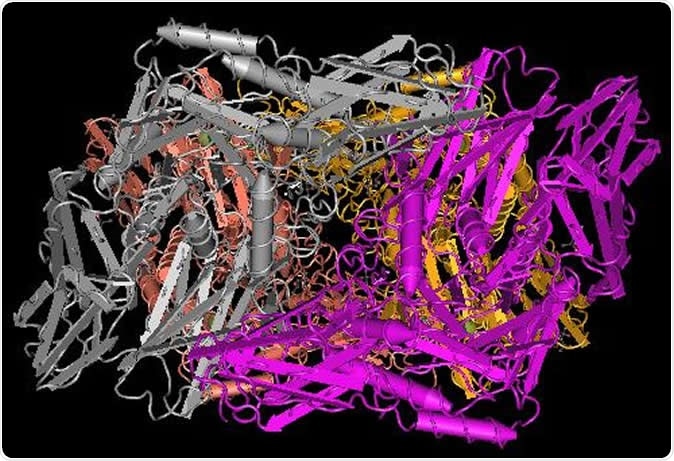 Кристаллическая структура предполагаемой бета-галактозидазы из Bacteroides fragilis. Изображение предоставлено:Национальные институты здравоохранения.
Кристаллическая структура предполагаемой бета-галактозидазы из Bacteroides fragilis. Изображение предоставлено:Национальные институты здравоохранения. Микроорганизмы, или микробы, существуют уже очень давно, и формируют как внешнюю, так и внутреннюю среду человека. Слово «микробиом» было придумано Джошуа Ледербергом в 2001 году. как способ привлечь внимание ученых к множественным взаимодействиям между микробами, обитающими в наших телах, и их взаимодействие с нашей человеческой физиологией. Этот термин теперь определяется как «многовидовое сообщество микроорганизмов в любой среде:хозяин, естественная среда, или экосистема ». Далеко не просто захватчики, стремящиеся к нашему уничтожению, микробиом человека включает в себя целый живой мир, принося полный и очень разнообразный набор генов, которые взаимодействуют и изменяются, а также влияют на здоровье человека. Эта микробная генетическая смесь называется метагеномом. Проект «Микробиом человека» (HMP) стартовал в 2008 году и помог активизировать более детальную характеристику и понимание того, как функционируют эти сообщества.
Исследование микробиома кишечника требует сбора и анализа точных данных с высокой пропускной способностью. а также средства для организованной интеграции обработанных данных для хранения, обмен и доступ среди исследовательских групп. Большинство более ранних исследований было сосредоточено на конкретных генах или группах организмов, исключая большие сегменты микробного генома. Также, различные эталоны привели к множеству заявлений о составе кишечника.
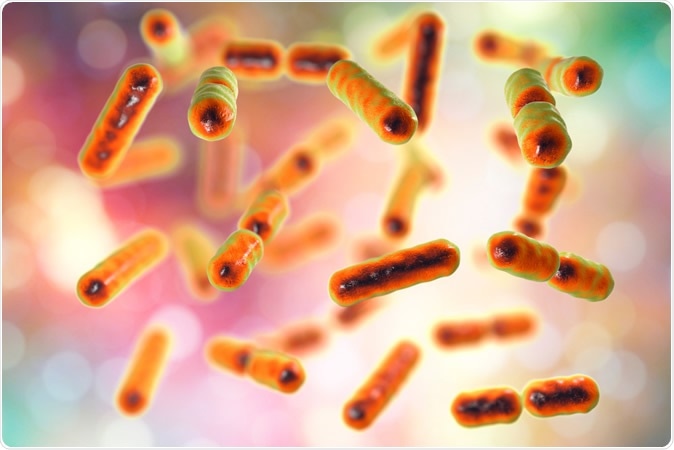 Бактерии Bacteroides fragilis, один из основных компонентов нормального микробиома кишечника человека, 3D-иллюстрация Кредит:Катерина Кон / Shutterstock
Бактерии Bacteroides fragilis, один из основных компонентов нормального микробиома кишечника человека, 3D-иллюстрация Кредит:Катерина Кон / Shutterstock По факту, в большинстве исследований метагенома используется только небольшой эталонный набор последовательностей нуклеиновых кислот из уже выбранных микробов или микробных генов. Это связано с трудностью сопоставления экспериментальных данных с полной базой данных нуклеотидов, доступной с помощью NCBI (NCBI-nt). Тем не мение, новые алгоритмы теперь могут использовать последний, чтобы позволить более точный анализ экспериментальных данных, чтобы получить профиль микробной численности.
Настоящая работа строится на этом фундаменте, чтобы сформировать базу знаний по ощущениям кишечника - GutFeelingKB - с образцами от здоровой группы участников. Эти образцы кишечной микробиоты были секвенированы, чтобы получить представление о том, как выглядит здоровый метагеном кишечника. Номер образца был заполнен с использованием еще 50 последовательностей, выбранных случайным образом из HMP.
Исследователи также собрали собранные смежные последовательности, или контиги, которые не соответствуют какой-либо последовательности NCBI-nt, но могут быть обнаружены в образцах здоровых фекалий. Таким образом, контиги - это темная материя, не распознается какой-либо известной последовательностью нуклеиновой кислоты, но которые можно объединить в последовательности по 10, 000 нуклеотидов или больше. Эта длина была выбрана для уменьшения количества посторонних (искусственных) контигов темной материи, в то же время включая микробную темную материю. Таким образом, GutFeelingKB представляет собой обширную базу знаний о здоровом микробиоме кишечника человека.
Затем это было использовано в качестве справочного материала для создания стандартного шаблона отчетности, в котором можно сообщать об отдельных микробиомах, чтобы позволить прямое сравнение результатов между исследованиями и образцами.
Ученые также создали новый рабочий процесс, используя несколько компьютерных программ и базу данных отфильтрованных микробных последовательностей кишечника под названием Filtered-nt, содержащий почти 35, 000, 000 последовательностей, которые позволяют биологически релевантную интерпретацию последовательностей образцов, обеспечивая при этом уверенность в том, что включено все известное пространство последовательностей.
Таким образом, GutFeelingKB представляет собой тщательно подобранную коллекцию нуклеотидных последовательностей с метаданными от 157 организмов 60 родов.
Таким образом, микробиом здорового человека состоит из представителей 8 типов, 18 семей, 60 родов и 109 видов, в основном из филы Firmicutes (40%) и Bacteroidetes (20%). Еще 20% происходят от актинобактерий. Среди фирмикутов, более половины - Clostridia, за ними следуют Bacteroides, Бифидобактерии, Энтеробактерии и лактобациллы.
Все пробы были положительными на 84 из 109 организмов, что, возможно, представляет собой основной список видов.
Тем не мение, важно отметить, что во всем мире были нанесены на карту определенные организмы, которых нет в GutFeelingKB, такие как Fusobacteria, некоторые виды Actinobacter и Bacteroides. Функция этой платформы будет действовать как стартовая площадка для сравнения результатов анализа образцов от здоровых людей. и дать больше информации об изменениях, наблюдаемых под влиянием диетических факторов, болезни и лекарства.
Bacteroides - единственный наиболее многочисленный род во многих странах, в здоровье. Обычно они полезны внутри кишечника, но если они ускользнут, они используют шанс вызвать инфекции, которые часто устойчивы к лекарствам и могут привести к 20% летальности. Тем не мение, в кишечнике они защищают от других патогенов и помогают расщеплять углеводы в рационе.
Сходным образом, Бифидобактерии - одни из первых поселенцев кишечника, часто встречаются в пробиотиках, и продуцируют важный ацетат короткоцепочечных жирных кислот (SCFA), который укрепляет эпителиальный барьер кишечника против инфекции. Один штамм Bifidobacterium longum был обнаружен у одного человека в группе особенно долгожителей в Китае.
Число бифидобактерий увеличивается с повышенным потреблением белка, и особенно с растительным белком. Пищевая растворимая клетчатка также способствует ее росту. Аккермансия связана с насыщенными жирами и линолевой кислотой, но отрицательно связаны с полиненасыщенными жирными кислотами (ПНЖК). Число Bacteroides ovatus увеличивается с увеличением количества потребляемой пищи, ожирение и окружность талии. Эти примеры помогают нам понять, как эти цифры могут быть использованы для принятия мер в отношении здоровья для исправления дисбаланса микробиома в будущем.
Шаблон отчетности, опубликованный в данном исследовании, призван заменить нестандартные форматы, используемые различными коммерческими и исследовательскими группами, что затрудняет их интерпретацию и сравнение. Он преобразует данные исследования в клинический отчет, помогая сделать его незамедлительным.
FecalBiome имеет три домена:Образец, Пациент и результат, напоминающий отчет метаболической панели. Это также позволяет сотрудникам быстро обмениваться большим объемом информации, когда исследования проводятся в самых разных местах. Порог для отчетности может быть установлен индивидуально в соответствии с целью исследования. Он сообщает об изобилии, средняя численность и информация о присутствующих микробах.
Таким образом, настоящий отчет позволяет связать исследования кишечных бактерий с понятной информацией о здоровье. делая его актуальным для медицинской практики и пациента. Это также позволяет легко сравнивать исследования. Это поможет быстрее пересмотреть продукты, заменяющие кишечник, и способствовать прогрессу доказательной медицины.
Исследование было опубликовано 11 сентября. 2019, в PLOS ONE .
 Пересадка вагинальной жидкости может помочь в лечении рецидивирующего бактериального вагиноза
Пересадка вагинальной жидкости может помочь в лечении рецидивирующего бактериального вагиноза
 Ученые разрабатывают подход к вакцинации от воспаления кишечника
Ученые разрабатывают подход к вакцинации от воспаления кишечника
 Анализ крови на микробную ДНК может предупредить о раке
Анализ крови на микробную ДНК может предупредить о раке
 Клещи теперь переносят множество болезней,
Клещи теперь переносят множество болезней,
 Математическая модель выявляет риск заражения SARS-CoV-2 после трансплантации фекальной микробиоты
Математическая модель выявляет риск заражения SARS-CoV-2 после трансплантации фекальной микробиоты
 Мужчины, которые едят йогурт два раза в неделю, реже заболевают раком кишечника.
Мужчины, которые едят йогурт два раза в неделю, реже заболевают раком кишечника.
 Биологическая терапия может снизить риск тяжелой формы COVID-19
Недавнее обсервационное исследование испанских исследователей, в настоящее время доступно на medRxiv * сервер препринтов, предполагает, что пациенты с иммуноопосредованными заболеваниями, получающие
Биологическая терапия может снизить риск тяжелой формы COVID-19
Недавнее обсервационное исследование испанских исследователей, в настоящее время доступно на medRxiv * сервер препринтов, предполагает, что пациенты с иммуноопосредованными заболеваниями, получающие
 Perfectus Biomed примет участие в конференции IPS в Ливерпуле
Команда Perfectus Biomed примет участие в конференции Общества профилактики инфекций (IPS) в Ливерпуле в этом месяце. Конференция состоится в арене и конференц-центре Ливерпуля с 22 по 24 сентября 201
Perfectus Biomed примет участие в конференции IPS в Ливерпуле
Команда Perfectus Biomed примет участие в конференции Общества профилактики инфекций (IPS) в Ливерпуле в этом месяце. Конференция состоится в арене и конференц-центре Ливерпуля с 22 по 24 сентября 201
 Антибиотик Х-206 эффективен против SARS-CoV-2 in vitro
Пандемия COVID-19 продолжает вызывать множество серьезных и смертельных случаев легочных заболеваний. часто заканчивается полиорганной дисфункцией и сердечно-сосудистым коллапсом. Без вакцины или пров
Антибиотик Х-206 эффективен против SARS-CoV-2 in vitro
Пандемия COVID-19 продолжает вызывать множество серьезных и смертельных случаев легочных заболеваний. часто заканчивается полиорганной дисфункцией и сердечно-сосудистым коллапсом. Без вакцины или пров